Fontos dokumentumok
N1268
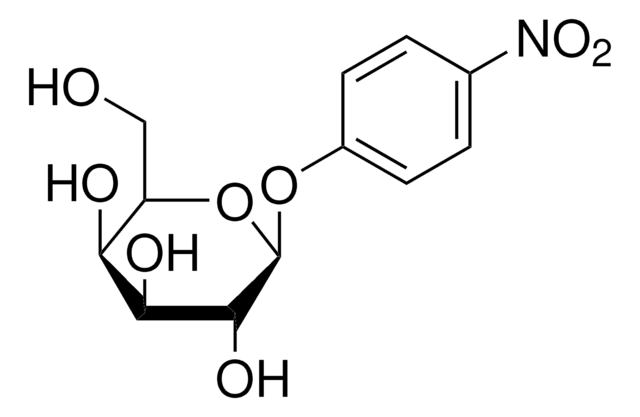
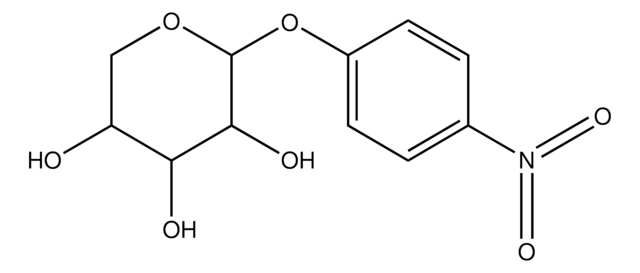
4-Nitrophenyl β-D-mannopyranoside
≥98%, powder
Szinonimák:
p-Nitrophenyl β-D-mannopyranoside
About This Item
Javasolt termékek
Terméknév
4-Nitrophenyl β-D-mannopyranoside, ≥98%
Minőségi szint
Teszt
≥98%
Forma
powder
oldhatóság
water: 10 mg/mL, clear, colorless to very faintly green
tárolási hőmérséklet
−20°C
SMILES string
OC[C@H]1O[C@@H](Oc2ccc(cc2)[N+]([O-])=O)[C@@H](O)[C@@H](O)[C@@H]1O
InChI
1S/C12H15NO8/c14-5-8-9(15)10(16)11(17)12(21-8)20-7-3-1-6(2-4-7)13(18)19/h1-4,8-12,14-17H,5H2/t8-,9-,10+,11+,12-/m1/s1
Nemzetközi kémiai azonosító kulcs
IFBHRQDFSNCLOZ-LDMBFOFVSA-N
Looking for similar products? Látogasson el ide Útmutató a termékösszehasonlításhoz
Alkalmazás
- as a substrate to analyze the action mechanism of Pyrococcus furiosus thermostable glycosidase (PFTG) and kinetic parameters by isothermal titration calorimetry (ITC)
- as a substrate for GH1-glucosidase (EaBgl1A) enzyme
- as a substrate for screening cucumber enzymes
Biokémiai/fiziológiai hatások
Tárolási osztály kódja
11 - Combustible Solids
WGK
WGK 3
Lobbanási pont (F)
Not applicable
Lobbanási pont (C)
Not applicable
Egyéni védőeszköz
Eyeshields, Gloves, type N95 (US)
Válasszon a legfrissebb verziók közül:
Már rendelkezik ezzel a termékkel?
Az Ön által nemrégiben megvásárolt termékekre vonatkozó dokumentumokat a Dokumentumtárban találja.
Az ügyfelek ezeket is megtekintették
Tudóscsoportunk valamennyi kutatási területen rendelkezik tapasztalattal, beleértve az élettudományt, az anyagtudományt, a kémiai szintézist, a kromatográfiát, az analitikát és még sok más területet.
Lépjen kapcsolatba a szaktanácsadással