C4874
Calmodulin bovine
recombinant, expressed in E. coli, lyophilized powder, ≥98% (SDS-PAGE)
Szinonimák:
CaM, Phosphodiesterase 3:5-cyclic nucleotide activator, Phosphodiesterase 3′:5′-cyclic nucleotide activator
About This Item
Javasolt termékek
biológiai forrás
bovine
Minőségi szint
rekombináns
expressed in E. coli
Teszt
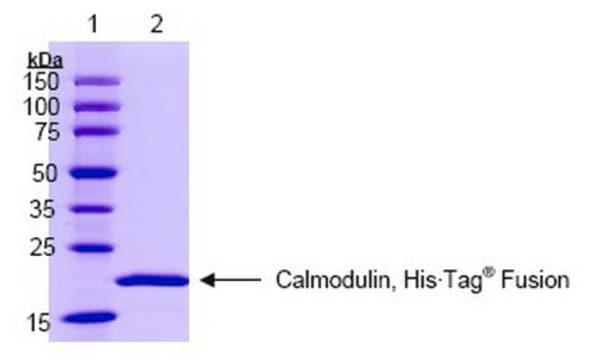
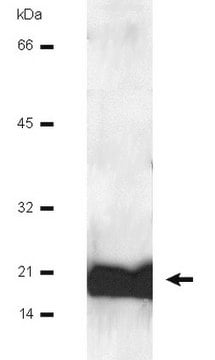
≥98% (SDS-PAGE)
form
lyophilized powder
molekulatömeg
Mw 19000.9 by amino acid sequence
összetétel
Protein, ≥85%
UniProt elérési szám
tárolási hőmérséklet
−20°C
Géninformáció
bovine ... CALM(100297344)
Általános leírás
Alkalmazás
Biokémiai/fiziológiai hatások
Fizikai tulajdonságok
MGSSHHHHHHSSGLVPRGSHMADQLTEEQIAEFKEAFSLFDKDGDGTITTKELGTVMRSLGQNPTEAELQDMINEVDADGNGTIDFPEFLTMMARKMKDTDSEEEIREAFRVFDKDGNGYISAAELRHVMTNLGEKLTDEEVDEMIREADIDGDGQVNYEEFVQMMTAK
Elkészítési megjegyzés
Tárolási osztály kódja
11 - Combustible Solids
WGK
WGK 3
Lobbanási pont (F)
Not applicable
Lobbanási pont (C)
Not applicable
Analitikai tanúsítványok (COA)
Analitikai tanúsítványok (COA) keresése a termék sarzs-/tételszámának megadásával. A sarzs- és tételszámok a termék címkéjén találhatók, a „Lot” vagy „Batch” szavak után.
Már rendelkezik ezzel a termékkel?
Az Ön által nemrégiben megvásárolt termékekre vonatkozó dokumentumokat a Dokumentumtárban találja.
Az ügyfelek ezeket is megtekintették
Tudóscsoportunk valamennyi kutatási területen rendelkezik tapasztalattal, beleértve az élettudományt, az anyagtudományt, a kémiai szintézist, a kromatográfiát, az analitikát és még sok más területet.
Lépjen kapcsolatba a szaktanácsadással