Katalyzátory Maruoka
Asymetrická katalýza fázového přenosu za použití Maruokových katalyzátorů se ukázala být ideální metodou pro enantioselektivní přípravu přírodních a nepřírodních α-alkylových a α,α-dialkyl-α-aminokyselin z derivátů glycinu. Zatímco pro tento typ transformace byly vyvinuty různé příbuzné katalyzátory, 677086 a 687596 jsou obzvláště pozoruhodné díky svému strukturně zjednodušenému skeletu. Kromě relativně jednodušší struktury si 677086 a 687596 také zachovávají srovnatelnou katalytickou aktivitu a schopnost dosahovat enantioselektivity ekvivalentní katalyzátorům dříve navrženým Maruokou a spolupracovníky.1,2,3
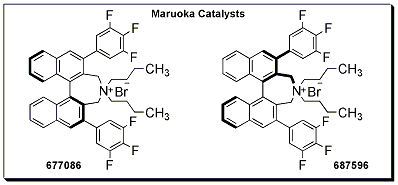
Výhody
- Provozně jednoduché
- Šetrné k životnímu prostředí
- Relativně mírné reakční podmínky
- Reakce probíhají ve vodném prostředí
- Kompatibilní s požadavky na rozšiřování
- Nízké zatížení katalyzátoru
Reprezentativní aplikace
Maruoka a spolupracovníci oznámili v roce 2005 další verzi svých katalyzátorů pro chirální fázový přenos, která využívala butylové skupiny místo bifenylových nebo nafthylových skupin na dusíku, čímž poskytla flexibilnější a polárnější katalyzátor, usnadňující výměnu, která musí probíhat mezi organickou a vodnou vrstvou dvoufázové směsi.2
Typický postup dvoufázové transformace vyžaduje použití organického rozpouštědla (toluenu) v kombinaci s vodným roztokem báze, katalyzátoru fázového přenosu, organického halogenidu a chráněné aminokyseliny (obvykle chráněné jako benzofenonový imin nebo p-chlorbenzaldehydový imin-tabulky 1 a 2). Většina reakcí probíhá s relativně krátkými reakčními časy při teplotách od -20 °C do 0 °C a poskytuje α-alkylové a α,α-dialkyl-α-aminokyseliny v dobrém celkovém výtěžku s vynikající enantioselektivitou.1,2,3
Původně se předpokládalo, že použití ekonomičtějšího p-chlorbenzaldehydového iminu bude omezeno na α-alkyl substituované deriváty z důvodu nižší pKa a obav z racemizace těchto aldiminových Schiffových bází; nicméně později se ukázalo, že p-Cl-fenylová ochranná skupina skutečně umožňuje účinnou transformaci na monoalkylační deriváty, jako jsou ty uvedené v tabulce 2.3
Metoda rovněž poskytuje α,α-dialkyl-α-aminokyseliny v dobrých výtěžcích s vynikající enantioselektivitou, pokud se použije Schiffova báze odvozená od alaninu, jak je uvedeno v Schématu 1.
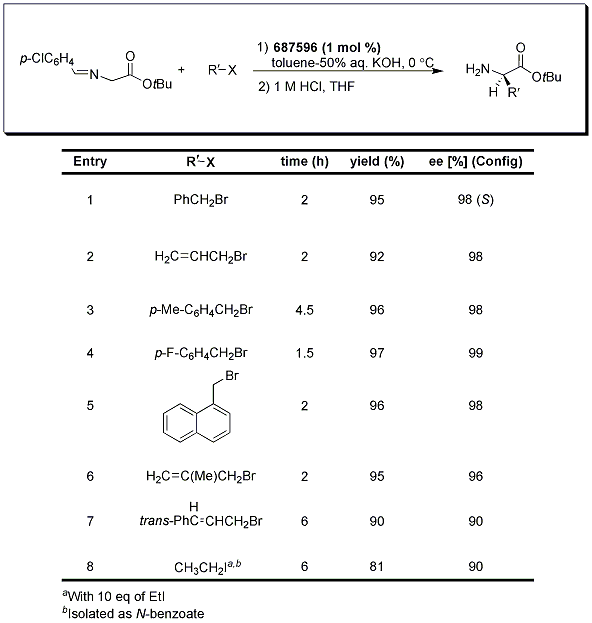
Tabulka 1.Benzofenon imin
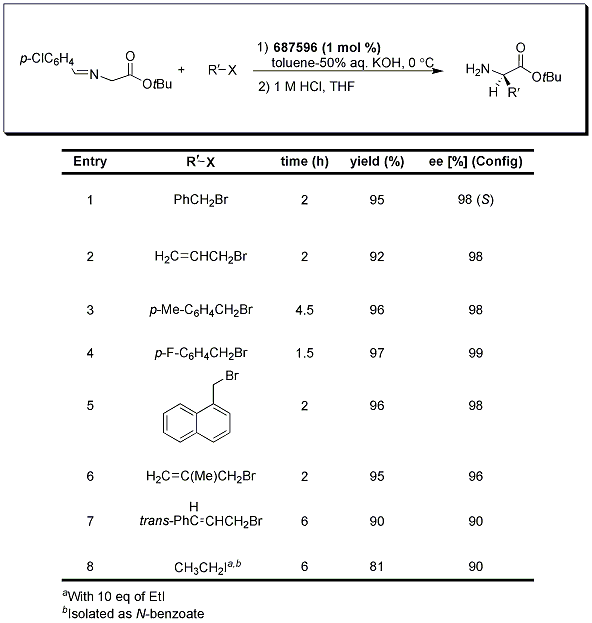
Tabulka 2.p-chlorbenzaldehyd imin
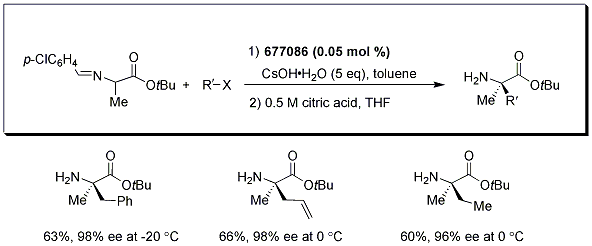
Schéma 1.Schiffova báze odvozená od alaninu
Odkazy
Abyste mohli pokračovat ve čtení, přihlaste se nebo vytvořte účet.
Nemáte účet?