Iontové kapaliny
Úvod
V tomto článku upozorňujeme na některé aplikace iontových kapalin. Představujeme více než 50 přírůstků do našeho portfolia více než 130 iontových kapalin, od dobře známých imidazolových a pyridiniových derivátů až po amoniové, pyrrolidiniové, fosfoniové a sulfoniové deriváty.
Iontové kapaliny jsou třídou čistě iontových materiálů podobných solím, které jsou kapalné při neobvykle nízkých teplotách. Definice iontových kapalin používá jako referenční bod bod varu vody: "Iontové kapaliny jsou iontové sloučeniny, které jsou kapalné při teplotě nižší než 100 °C." Častěji, mají iontové kapaliny teplotu tání nižší než pokojová teplota; některé z nich mají dokonce teplotu tání nižší než 0 °C. Tyto nové materiály jsou kapalné v širokém rozsahu teplot (300-400 °C) od teploty tání až po teplotu rozkladu iontové kapaliny. Iontové kapaliny jsou obecně považovány za bezpečnější alternativu tradičních organických rozpouštědel díky nízkému tlaku par, který vede ke snížení rizika inhalační expozice a znečištění ovzduší, nehořlavosti, která snižuje riziko nebezpečí požáru ve srovnání s těkavými organickými rozpouštědly, a biologické rozložitelnosti.
Pokud porovnáme typické iontové kapaliny, např, 1-ethyl-3-methylimidazolium ethylsulfát (m.p. <-20 °C), s typickou anorganickou solí, např. kuchyňskou solí (NaCl, m.p. 801 °C), je zřejmé, proč existuje rozdíl. Iontová kapalina má výrazně nižší symetrii! Navíc je náboj kationtu i náboj aniontu rezonancí rozložen na větší objem molekuly. V důsledku toho bude tuhnutí iontové kapaliny probíhat při nižších teplotách. V některých případech, zejména pokud se jedná o dlouhé alifatické postranní řetězce, se místo teploty tání pozoruje skelný přechod.
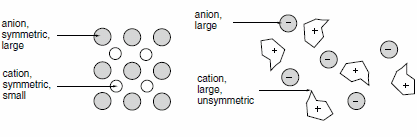
Silná iontová (Coulombova) interakce uvnitř těchto látek vede k zanedbatelnému tlaku par (pokud nedojde k rozkladu), nehořlavé látce a k vysoké tepelné, mechanické i elektrochemické stabilitě produktu. Kromě této velmi zajímavé kombinace vlastností nabízejí i další příznivé vlastnosti: například velmi atraktivní rozpouštěcí vlastnosti a nemísitelnost s vodou nebo organickými rozpouštědly, které vedou k bifázickým systémům.
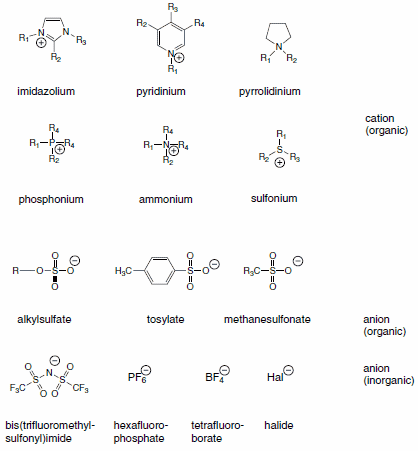
Výběr kationtu má silný vliv na vlastnosti iontové kapaliny a často určí její stabilitu. Chemické vlastnosti a funkčnost iontové kapaliny jsou obecně řízeny volbou aniontu. Kombinace široké škály kationtů a aniontů vede k teoreticky možnému počtu 1018 iontových kapalin. Reálný počet však bude mnohonásobně nižší. V současné době je v literatuře popsáno přibližně 1000 iontových kapalin a přibližně 300 je jich komerčně dostupných. Typické struktury kombinují organické kationty s anorganickými nebo organickými anionty:
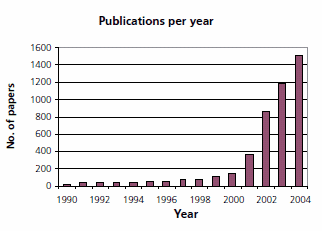
Rostoucí zájem akademické sféry a průmyslu o technologii iontových kapalin je reprezentován každoročním nárůstem počtu publikací (zdroj Sci-Finder™): od méně než 100 v roce 1990 až po více než 1 500 prací publikovaných v loňském roce.
Použití a aplikace
Důvodem nárůstu počtu publikací mohou být jedinečné vlastnosti těchto nových materiálů. Možné kombinace organických kationtů a aniontů v konečném důsledku staví chemiky do pozice, kdy mohou navrhovat a dolaďovat fyzikální a chemické vlastnosti zaváděním nebo kombinováním strukturních motivů, a tím umožňují vytvářet materiály a řešení na míru. Následující tabulka shrnuje důležité vlastnosti iontových kapalin a jejich potenciální a současné aplikace:1

Odpovídající aplikace iontových kapalin lze rozdělit na jejich použití jako procesních chemikálií a výkonných chemikálií. V roce 1948 tato třída elektricky vodivých materiálů (1-butylpyridiniumchlorid/AlCl3) poprvé upoutala pozornost pro své použití jako elektrolytů pro elektrodesikaci hliníku.2 Tato oblast je stále předmětem současného výzkumného úsilí. Dalšími důležitými aplikacemi v této souvislosti je jejich použití jako elektrolytů pro baterie a palivové články.
Významný průlom nastal s příchodem méně korozivních, na vzduchu stabilních materiálů v roce 1992. Wilkes a Zaworotko představili 1-ethyl-3-methylimidazolium tetrafluoroborát a zaměřili se na aplikace v rozpouštědlech.3 Ačkoli 1-butyl-3-methylimidazolium hexafluorofosfát a -tetrafluoroborát stále dominují současné literatuře, existují lepší volby s ohledem na výkon a manipulaci. Bylo prokázáno, že ve vodném prostředí dojde k rozkladu hexafluorfosforečnanového aniontu a tetrafluoroboritanového aniontu za vzniku HF, škodlivé a agresivní kyseliny.
Byly navrženy další zajímavé aplikace, odvozené od jedinečné kombinace fyzikálních vlastností. Například použití iontových kapalin jako tepelných kapalin kombinuje jejich tepelnou kapacitu s tepelnou stabilitou a zanedbatelným tlakem par. Lze zcela reálně očekávat, že potenciální uživatelé navrhnou mnoho dalších aplikací a některé z nich budou v budoucnu realizovány. Aby potenciální uživatelé mohli iontové kapaliny využívat, bude nutné poskytnout technologickou podporu a zpřístupnit řadu iontových kapalin k testování. Tato podpora zahrnuje také vypracování toxikologických údajů a oznámení požadovaných vládou, jakož i zavedení koncepce recyklace iontové kapaliny.
Odkazy
Abyste mohli pokračovat ve čtení, přihlaste se nebo vytvořte účet.
Nemáte účet?