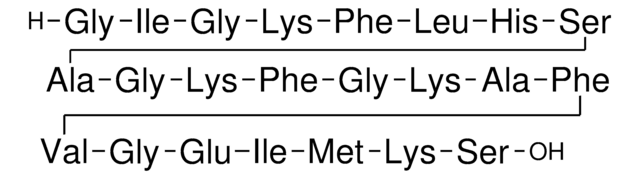Przejdź do
Wybierz wielkość
| Do Państwa/SKU | Dostępność | Cena netto |
|---|---|---|
0.1 mg | Skontaktuj się z Obsługą Klienta, aby uzyskać informacje na temat dostępności | 1040,00 zł 780,00 zł |
0.5 mg | Skontaktuj się z Obsługą Klienta, aby uzyskać informacje na temat dostępności | 3480,00 zł 2610,00 zł |
Informacje o tej pozycji
780,00 zł
Cena katalogowa1040,00 złZaoszczędź 25%Quality Segment
assay
≥97% (HPLC)
antibiotic activity spectrum
fungi, viruses
mode of action
cell membrane | interferes
storage temp.
−20°C
SMILES string
CC[C@H](C)[C@H](NC(=O)CN)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](Cc1ccccc1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](Cc2c[nH]cn2)C(=O)N[C@@H](CO)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](Cc3ccccc3)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C)C(=O)N[C@@H](Cc4ccccc4)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CO)C(O)=O
InChI
1S/C114H180N30O29S/c1-12-65(7)94(142-88(148)55-119)112(170)124-59-90(150)129-74(38-24-28-45-116)100(158)137-81(51-70-33-19-15-20-34-70)106(164)135-79(49-63(3)4)105(163)138-83(53-72-56-121-62-125-72)107(165)140-85(60-145)110(168)127-67(9)96(154)131-75(39-25-29-46-117)101(159)132-76(40-26-30-47-118)102(160)136-80(50-69-31-17-14-18-32-69)98(156)122-57-89(149)128-73(37-23-27-44-115)99(157)126-68(10)97(155)134-82(52-71-35-21-16-22-36-71)109(167)143-93(64(5)6)111(169)123-58-91(151)130-77(41-42-92(152)153)104(162)144-95(66(8)13-2)113(171)133-78(43-48-174-11)103(161)139-84(54-87(120)147)108(166)141-86(61-146)114(172)173/h14-22,31-36,56,62-68,73-86,93-95,145-146H,12-13,23-30,37-55,57-61,115-119H2,1-11H3,(H2,120,147)(H,121,125)(H,122,156)(H,123,169)(H,124,170)(H,126,157)(H,127,168)(H,128,149)(H,129,150)(H,130,151)(H,131,154)(H,132,159)(H,133,171)(H,134,155)(H,135,164)(H,136,160)(H,137,158)(H,138,163)(H,139,161)(H,140,165)(H,141,166)(H,142,148)(H,143,167)(H,144,162)(H,152,153)(H,172,173)/t65-,66-,67-,68-,73-,74-,75-,76-,77-,78-,79-,80-,81-,82-,83-,84-,85-,86-,93-,94-,95-/m0/s1
InChI key
MGIUUAHJVPPFEV-ABXDCCGRSA-N
General description
Biochem/physiol Actions
Other Notes
1 of 1
Ta pozycja | |||
|---|---|---|---|
| mode of action cell membrane | interferes | mode of action cell membrane | interferes | mode of action cell membrane | interferes | mode of action cell membrane | interferes |
| antibiotic activity spectrum fungi, viruses | antibiotic activity spectrum fungi, viruses | antibiotic activity spectrum Gram-positive bacteria | antibiotic activity spectrum fungi, viruses |
| Quality Level 200 | Quality Level 200 | Quality Level 200 | Quality Level 200 |
| assay ≥97% (HPLC) | assay ≥97% (HPLC) | assay ≥98% (HPLC) | assay ≥97% (HPLC) |
| storage temp. −20°C | storage temp. −20°C | storage temp. −20°C | storage temp. −20°C |
Klasa składowania
11 - Combustible Solids
wgk
WGK 3
flash_point_f
Not applicable
flash_point_c
Not applicable
ppe
Eyeshields, Gloves, type N95 (US)
Wybierz jedną z najnowszych wersji:
Masz już ten produkt?
Dokumenty związane z niedawno zakupionymi produktami zostały zamieszczone w Bibliotece dokumentów.