cataCXium® katalizátorok
Bevezetés
A keresztkapcsolási reakciók a katalitikus átalakulások fontos osztályát képezik, amelyek a polimerek tudományában, valamint a finomkémiai és gyógyszeriparban is alkalmazhatók. Az aril-kloridok használata ezekhez az átalakulásokhoz előnyös alacsony költségük és elérhetőségük miatt. A katalizátorok tervezésében elért óriási előrelépés ellenére azonban az e reakciókhoz szükséges Pd-terhelés
(1-3 mol%) megtiltja az iparnak, hogy kilogrammos méretekben használja őket. Az elmúlt 20 évben folyamatosan törekedtek arra, hogy nagyon alacsony töltéssel rendelkező, nagyon aktív katalizátort szintetizáljanak.
- Atomtakarékos módszer
- Nagy hozam
- Nagy forgalomszám
Suzuki-kapcsolás alacsony katalizátor-töltéssel
/b>Beller és munkatársai diadamantilalkil-foszfánokon alapuló, igen terjedelmes ligandumot fejlesztettek ki.1,2,3 A csoport által szintetizált ligandumok közül a diadamantil-n-butilfoszfán bizonyult a leghatékonyabbnak. 0,005 mol% Pd(OAc)2 és 0,01 mol% foszfin felhasználásával jó vagy kiváló hozamokat (58-100%) jelentettek (Séma 1). Fontos megjegyezni, hogy az aril-klorid orto-szubsztituenseit tolerálták, és csak az erősen elektrondonor szubsztituensek, mint például a metoxicsoport, vezettek a hozamok csökkenéséhez (60%) (1. táblázat).

Séma 1
Evonik Beller professzorral és munkatársaival együttműködve a foszfin-ligandumok egy új osztályát, a foszfino-szubsztituált N-aril-pirrolokat fejlesztette ki.4 Ezek a biaril ligandumok sztérikusan igényesek és elektronokban gazdagok. Különböző aril-kloridok fenil-boronsavval történő reakciójában alkalmazva, enyhe reakcióhőmérsékleten nagyon magas fordulatszámot mutattak. A különböző aril-kloridok fenil-bórsavval történő keresztkapcsolásához (2. séma) alacsony katalizátorterhelésre (0,05 mol%) volt szükség. Ennek a ligandumnak a felhasználása Pd(OAc)2 vagy Pd2(dba)3-val az elektronban gazdag és elektronhiányos arilkloridok átalakítására kiváló hozamokat eredményezett. A 2. táblázat összefoglalja a különböző aril-kloridok fenilboronsavval reagáltatott hozamát 0,01 mol% Pd2(dba)3 -mal 60 °C-on.

Séma 2
A foszfino-N-aril-pirrolok sikeres szintézisére építve Beller és munkatársai hasonló ligandumot fejlesztettek ki. Foszfino-N-fenilindol alapú ligandumokat szintetizáltak.5 E ligandumok reaktivitásának felmérésére elvégezték a klórbenzol és anilin keresztkapcsolási reakcióját (3. séma). Ez az új rendszer bizonyult a legjobbnak a Beller és munkatársai által kifejlesztett különböző ligandumok közül erre a speciális keresztkapcsolási reakcióra. Pd(OAc)2 és a tert-butil-foszfin-fenilindol ligandumot NaOtBu bázissal toluolban használva az aminok széles skáláját arilálták kiváló hozammal.
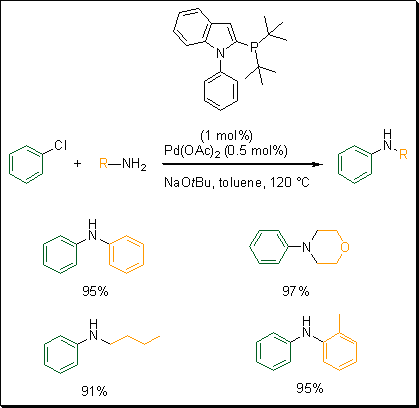
Séma 3
Hivatkozások
Keresztkapcsolási reakciók
A foszfor ligandumok új osztályát fejlesztették ki Plenio és munkatársai a fluorenilfoszfinok architektúráján alapulva.1 Ezen új ligandumok hatékonyságának tesztelésére a tudóscsoport több gyakori keresztkapcsolási reakciót hajtott végre: Suzuki, Sonogashira és Buchwald-Hartwig aminálás (1. ábra). A ligandum nagyon aktívnak bizonyult különböző aril-kloridok 4-metilfenil-bórsavval történő Suzuki-kapcsolásánál 0,05-0,5 mol% palládium töltet mellett. Az elektrondonor szubsztituens, mint például az OMe, nem befolyásolta a hozamokat, és a konverzió >99% volt. A Sonogashira-átalakítást különböző aril-kloridokkal végeztük fenilacetilénhez kapcsolva. A katalizátor 1 mol%-os betöltésével 44% és 94% közötti hozamot jelentettek. Végül a Buchwald-Hartwig-aminálás eredményei nagyon ígéretesek voltak, több reakció esetében már 0,1 mol% katalizátorbetöltéssel is mennyiségi konverziót jelentettek.
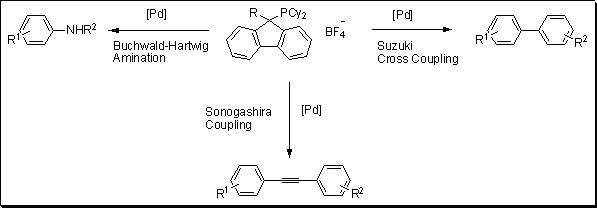
1. ábra.
Hivatkozások
Heck katalízis
Hermann és munkatársai a palládium katalizátorok egy új osztályát fejlesztették ki, az úgynevezett pallada-ciklusokat.1 Ezek a komplexek hőstabilak 100 °C-ig, és nagyon hatékonyak a Heck-katalízisben TON > 10 000. Tietze és munkatársai e katalizátor aktivitását a cephalostatin származékának szintézisére használták, egy olyan szteroidra, amely a rákos sejtek ellen mutatott hatékonyságot.2 A kettős kapcsolási reakciót 80%-os összhozammal hajtották végre.

Hivatkozások
Az olvasás folytatásához jelentkezzen be vagy hozzon létre egy felhasználói fiókot.
Még nem rendelkezik fiókkal?