SRP0182
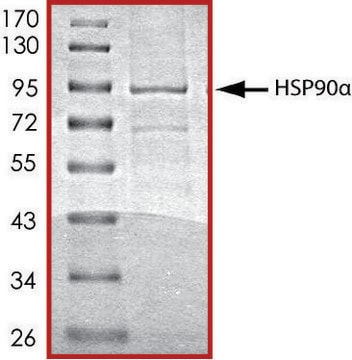
Hsp90a Active human
recombinant, expressed in E. coli, ≥80% (SDS-PAGE)
Szinonimák:
HSP86, HSPCAL3, Heat shock protein 90 kDa α, LAP2, NY-REN-38 (renal carcinoma antigen)
About This Item
Javasolt termékek
biológiai forrás
human
rekombináns
expressed in E. coli
Teszt
≥80% (SDS-PAGE)
form
aqueous solution
hatékonyság
≥8 nM
molekulatömeg
85.5 kDa
kiszerelés
pkg of 200 μg
tárolási körülmény
avoid repeated freeze/thaw cycles
koncentráció
>0.02 mg/mL
NCBI elérési szám
UniProt elérési szám
kiszállítva
dry ice
tárolási hőmérséklet
−70°C
Géninformáció
human ... HSP90AA2(3324)
Általános leírás
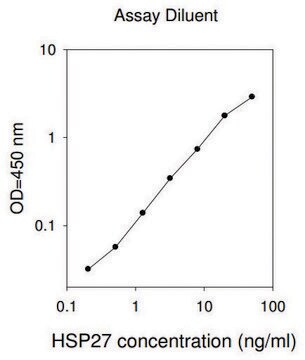
Alkalmazás
Biokémiai/fiziológiai hatások
Fizikai forma
Elkészítési megjegyzés
Figyelmeztetés
Danger
Figyelmeztető mondatok
Óvintézkedésre vonatkozó mondatok
Veszélyességi osztályok
Eye Irrit. 2 - Repr. 1B - Skin Irrit. 2
Tárolási osztály kódja
6.1C - Combustible acute toxic Cat.3 / toxic compounds or compounds which causing chronic effects
WGK
WGK 1
Analitikai tanúsítványok (COA)
Analitikai tanúsítványok (COA) keresése a termék sarzs-/tételszámának megadásával. A sarzs- és tételszámok a termék címkéjén találhatók, a „Lot” vagy „Batch” szavak után.
Már rendelkezik ezzel a termékkel?
Az Ön által nemrégiben megvásárolt termékekre vonatkozó dokumentumokat a Dokumentumtárban találja.
Tudóscsoportunk valamennyi kutatási területen rendelkezik tapasztalattal, beleértve az élettudományt, az anyagtudományt, a kémiai szintézist, a kromatográfiát, az analitikát és még sok más területet.
Lépjen kapcsolatba a szaktanácsadással