Fortfahren mit
Größe auswählen
| Packungsgröße | SKU | Verfügbarkeit | Preis |
|---|---|---|---|
| 1 mg | Warenkorb auf Verfügbarkeit prüfen | € 97,20 | |
| 5 mg | Warenkorb auf Verfügbarkeit prüfen | € 342,00 | |
| 25 mg | Warenkorb auf Verfügbarkeit prüfen | € 1.380,00 |
Über diesen Artikel
€ 97,20
Produktname
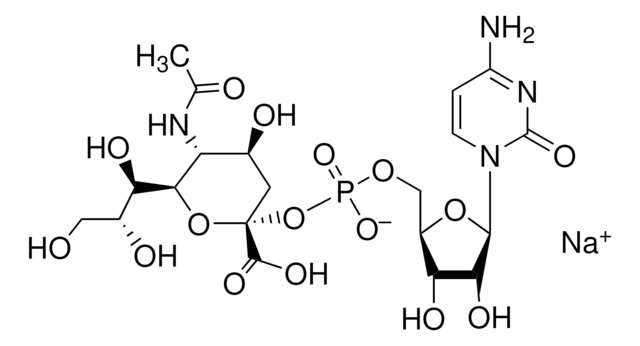
Cytidin-5′-Monophospho-N-Acetylneuraminsäure Natriumsalz, ≥85% (HPLC)
biological source
synthetic (organic)
Quality Segment
assay
≥85% (HPLC)
form
powder
solubility
water: 50 mg/mL, clear, colorless
storage temp.
−20°C
SMILES string
[Na+].CC(=O)N[C@@H]1[C@@H](O)C[C@@](O[C@@H]1[C@H](O)[C@H](O)CO)(OP([O-])(=O)OC[C@H]2O[C@H]([C@H](O)[C@@H]2O)N3C=CC(N)=NC3=O)C(O)=O
InChI
1S/C20H31N4O16P.Na/c1-7(26)22-12-8(27)4-20(18(32)33,39-16(12)13(29)9(28)5-25)40-41(35,36)37-6-10-14(30)15(31)17(38-10)24-3-2-11(21)23-19(24)34;/h2-3,8-10,12-17,25,27-31H,4-6H2,1H3,(H,22,26)(H,32,33)(H,35,36)(H2,21,23,34);/q;+1/p-1/t8-,9+,10+,12+,13+,14+,15+,16?,17+,20+;/m0./s1
InChI key
VFRHSOGUONIUOR-CTFMUGKASA-M
General description
Application
- als Standard bei der Hochleistungs-Anionenaustauschchromatographie mit gepulstem amperometrischem Nachweis (HPAEC-PAD) für die Analyse von Nukleotidzucker in Zellen von Patienten mit Joubert-Syndrom Typ 10 (JBTS10) und zur Kontrolle von dermalen Fibroblasten[1],
- als Substrat für die enzymatische Sialylierung von G2-Glykoformen[2], für Resialylierungs-Assays[3][4][5],
- für In-vitro-Sialyltransferase-Assays[6]
Biochem/physiol Actions
Preparation Note
CMP-NAN ist sehr säurelabil.
1 of 1
Dieser Artikel | |||
|---|---|---|---|
| biological source synthetic (organic) | biological source synthetic | biological source synthetic | biological source synthetic (organic) |
| Quality Level 200 | Quality Level 200 | Quality Level 100 | Quality Level 200 |
| assay ≥85% (HPLC) | assay ≥95% (HPLC) | assay ≥99.0% (HPLC) | assay ≥96% (HPLC) |
| form powder | form powder | form powder | form powder |
| storage temp. −20°C | storage temp. −20°C | storage temp. 2-8°C | storage temp. −20°C |
| solubility water: 50 mg/mL, clear, colorless | solubility water: 50 mg/mL, clear, colorless | solubility - | solubility H2O: 100 mg/mL |
Lagerklasse
11 - Combustible Solids
wgk
WGK 3
flash_point_f
Not applicable
flash_point_c
Not applicable
Hier finden Sie alle aktuellen Versionen:
Besitzen Sie dieses Produkt bereits?
In der Dokumentenbibliothek finden Sie die Dokumentation zu den Produkten, die Sie kürzlich erworben haben.
Artikel
Enzymatic glycosyltransferase specificity challenges the one enzyme-one linkage concept.
Understand sialic acid structure, function, signaling, and modifications. Easily find products for sialic acid research.
LC-MS/MS method quantifies similar polar nucleotide activated sugars using Supel™ Carbon LC column for simultaneous analysis.
Verwandter Inhalt
Explore tools for glycosyltransferase synthesis and modification of glycans, such as glycosyltransferases and nucleotide sugar donors.
Glycobiology and Glycoproteomics Brochure
Global Trade Item Number
| SKU | GTIN |
|---|---|
| C8271-5MG | 04061833522035 |
| C8271-25MG | 04061833522028 |
| C8271-1MG | 04061833522011 |