Kluczowe dokumenty
A6185
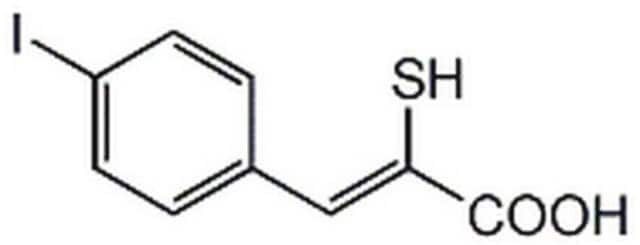
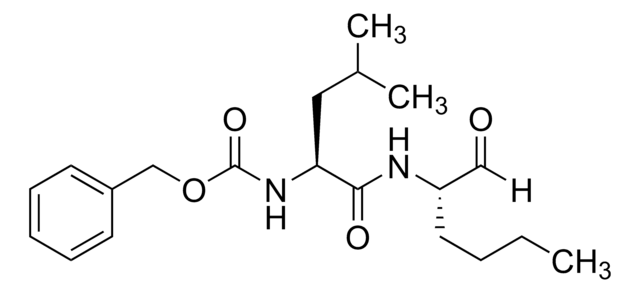
Calpain Inhibitor I
≥97% (TLC), powder
Synonim(y):
ALLN, Ac-LLnL-CHO, MG-101, N-Acetyl-L-leucyl-L-leucyl-L-norleucinal, N-Acetyl-Leu-Leu-Norleu-al
Wybierz wielkość
674,00 zł
Wybierz wielkość
About This Item
674,00 zł
Polecane produkty
pochodzenie biologiczne
synthetic (organic)
Poziom jakości
Próba
≥97% (TLC)
Formularz
powder
kolor
white
rozpuszczalność
DMSO: soluble
ethanol: soluble
temp. przechowywania
−20°C
ciąg SMILES
[H]C(=O)[C@H](CCCC)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(C)C)NC(C)=O
InChI
1S/C20H37N3O4/c1-7-8-9-16(12-24)22-19(26)18(11-14(4)5)23-20(27)17(10-13(2)3)21-15(6)25/h12-14,16-18H,7-11H2,1-6H3,(H,21,25)(H,22,26)(H,23,27)/t16-,17-,18-/m0/s1
Klucz InChI
FMYKJLXRRQTBOR-BZSNNMDCSA-N
informacje o genach
human ... CAPN1(823) , CTSB(1508) , PSMA1(5682)
Szukasz podobnych produktów? Odwiedź Przewodnik dotyczący porównywania produktów
Zastosowanie
Działania biochem./fizjol.
Kod klasy składowania
11 - Combustible Solids
Klasa zagrożenia wodnego (WGK)
WGK 3
Temperatura zapłonu (°F)
Not applicable
Temperatura zapłonu (°C)
Not applicable
Środki ochrony indywidualnej
Eyeshields, Gloves, type N95 (US)
Wybierz jedną z najnowszych wersji:
Masz już ten produkt?
Dokumenty związane z niedawno zakupionymi produktami zostały zamieszczone w Bibliotece dokumentów.
Klienci oglądali również te produkty
Produkty
DISCOVER Bioactive Small Molecules for Nitric Oxide & Cell Stress Research
Active Filters
Nasz zespół naukowców ma doświadczenie we wszystkich obszarach badań, w tym w naukach przyrodniczych, materiałoznawstwie, syntezie chemicznej, chromatografii, analityce i wielu innych dziedzinach.
Skontaktuj się z zespołem ds. pomocy technicznej