閱讀更多
Cas#:9004-54-0
結構
葡聚糖是氫葡萄糖的聚合物。它由大約 95% 的 alpha-D-(1-6)連結組成。1,2,3 有關分支長度的數據相互矛盾,這意味著平均分支長度少於三個葡萄糖單位。4,5 然而,其他方法表明存在超過 50 個葡萄糖單位的分支。6,7
已發現原生葡聚糖的分子量 (MW) 在 9 百萬到 5 億之間。8,9,10 較低 MW 的右旋糖酐會表現出稍少的支化4 並且有較窄的 MW 分佈範圍。11 MW 大於 10,000 的右旋糖酐表現得像是高度支化。7,12,13 MW為2,000至10,000的右旋糖酐分子表現出可擴展的線圈特性。12 在 MW 低於 2,000 的右旋糖酐更像棒狀。14
右旋糖酐的 MW 可使用下列一種或多種方法測量:低角度雷射光散射法15、尺寸排阻色層法16、 銅複合17、蒽酮試劑18 比色法測定還原糖和粘度12。
特定旋轉:[α]=+199° 11
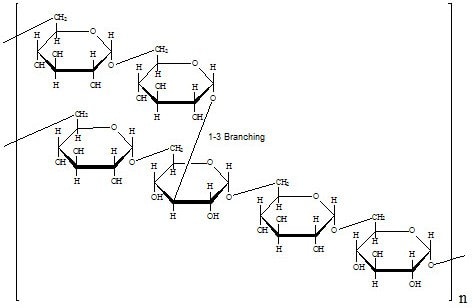
圖 1.特定旋轉
產品資訊
我們提供的右旋糖酐來自 Leuconostoc mesenteroides, strain B 512。 通過有限的水解和分餾生產出各種不同的 MW。我們供應商的確切方法為專利。分餾可透過尺寸排阻色譜法16或乙醇分餾法完成,其中最大 MW 的右旋糖酐會先析出。19
製備說明
除了最高 MW 的右旋糖酐 D5501(MW 範圍 = 5 百萬到 4 千萬)之外,右旋糖酐都非常易溶於水。
右旋糖酐也可自由溶於 DMSO、甲酰胺、乙二醇和甘油。11
中性右旋糖酐水溶液可在 110-115 °C 下高壓滅菌 30 至 45 分鐘。11右旋糖酐可在高溫下被強酸水解。在鹼性溶液中,右旋糖酐的末端還原基可被氧化。
Procedure
Dextran 是一種高分子量、惰性、水溶性聚合物,已廣泛應用於生物醫學領域。
未改性右旋糖酐的應用:
血漿擴展劑
右旋糖酐溶液已被用作血漿擴展劑。20
10%的葡聚糖溶液(MW 40,000)施加的胶体渗透压略高于血浆蛋白。
10% 的葡聚糖(MW 40,000)溶液在 0.9%氯化鈉或5%葡萄糖中的10%右旋糖酐(MW 40,000)溶液,有報導稱其可用作術後血栓栓塞性疾病的短期血漿擴張劑。 輸注後,約70%的右旋糖酐(MW 40,000)會在24小時後隨尿液排出體外,維持不變。
6% 的右旋糖酐 (MW 70,000) 溶液會產生與血漿蛋白類似的膠體滲透壓。MW 大於 50,000 的右旋糖酐傾向於緩慢地擴散穿過毛細管壁,並緩慢地新陳代謝為葡萄糖。輸注的右旋糖酐 MW 70,000 約有 50% 會在 24 小時內無變更地從尿液中排出 20。
離心/細胞和細胞器分離
含有葡聚糖(MW 250,000)的膠體溶液已被用來分離聚集的血小板21 20。sup>21 白細胞22 和淋巴細胞23 。
Dextran (MW 40,000) 已被用於分離完整的細胞核。24
蛋白沉澱
在免疫擴散應用中,已將二聚乙二醇用於增強抗體-抗原複合物的沉澱和敏感性。
Dextran (MW 80,000)被注入免疫電泳凝膠中,最大劑量為 80 mg/mL。25
Dextrans (MW 250,000 和 2,000,000) 也被用於類似應用。26
抑制血小板聚集
在較低的濃度下,Dextrans(MW 10,000-40,000)已被用來抑制血小板聚集。
參考資料
若要繼續閱讀,請登入或建立帳戶。
還沒有帳戶?為便利客戶閱讀,此頁面中文以機器翻譯完成。雖然我們已盡力確保機器翻譯的準確性,但機器翻譯並非完美。如果您對機器翻譯的內容不滿意,請參考英文版本。