Rozdzielanie antybiotyków tetracyklinowych metodą HPLC z odwróconymi fazami przy użyciu kolumn Discovery
Reporter EU Volume 14
Carmen T. Santasania, David S. Bell
Reporter EU Volume 16
Na rynku znajduje się obecnie ponad 100 antybiotyków, a wiele innych jest w fazie opracowywania. Oporność na antybiotyki stanowi poważny problem (1,2): antybiotyk, którego wprowadzenie na rynek zajmuje dekadę, może wywołać oporność w ciągu kilku miesięcy od jego wprowadzenia do praktyki klinicznej (3). Częstotliwość występowania oporności u bakterii i liczba leków, na które są one oporne, rośnie. Dlatego tak ważne jest monitorowanie poziomu antybiotyków podawanych ludziom i zwierzętom.
HPLC jest potężnym narzędziem do izolacji i ilościowego oznaczania antybiotyków. W tym zastosowaniu pięć antybiotyków tetracyklinowych (rysunek A) analizowano metodą HPLC przy użyciu kolumn Discovery C18, Discovery C8 i Discovery RP-AmideC16. Antybiotyki tetracyklinowe mają szerokie spektrum działania, są stosunkowo bezpieczne i skuteczne w zwalczaniu wielu infekcji wywołanych przez bakterie Gram-ujemne i Gram-dodatnie (4,5).

Rysunek A.Struktury antybiotyków tetracyklinowych
Rozdzielenia chromatograficzne przeprowadzono w systemie Waters Alliance HPLC. Wszystkie iniekcje zostały wykonane przez autosampler. Do monitorowania absorbancji UV próbek przy 260 nm wykorzystano detektor UV Waters 2487 o podwójnej długości fali. Kolumny HPLC z fazą odwróconą Discovery C18, Discovery C8 i Discovery RP-AmideC16 o średnicy 15 cm x 4,6 mm ID były używane bez kolumn ochronnych i filtrów. Cząstki wypełnienia we wszystkich kolumnach miały średnicę 5 μm.
Doksycyklina, minocyklina, tetracyklina, chlortetracyklina i oksytetracyklina zostały rozpuszczone w 25 mM KH2PO4 buforze, pH 3.
Pięć antybiotyków tetracyklinowych rozdzielono za pomocą elucji gradientowej. Temperatura kolumny była kontrolowana na poziomie 35°C. Ciśnienie w kolumnie wynosiło poniżej 1050 psi we wszystkich przypadkach. Szczegółowe warunki dla każdej analizy przedstawiono wraz z odpowiednim chromatogramem.
Rozdzielanie pięciu tetracyklin zilustrowano na rysunkach B, C i D. Minocyklina i oksytetracyklina będą koeluować z kolumny C18, ale są bardzo dobrze rozdzielane przez kolumny RP-AmideC16 i C8 (rysunki C i D). Kolumna Discovery RP-AmideC16 zapewnia najlepszą rozdzielczość minocykliny i oksytetracykliny. Tło wokół pików chlortetracykliny i doksycykliny jest spowodowane zanieczyszczeniami w próbkach. Należy zauważyć, że ilości analitów na kolumnie różniły się między rysunkami B, C i D.

Rysunek B.Antybiotyki tetracyklinowe na odkrywczej kolumnie C18 HPLC (504955)
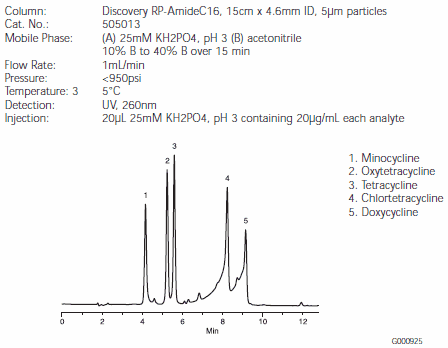
Rysunek C.Antybiotyki tetracyklinowe na kolumnie HPLC Discovery RP-AmideC16 (505013)
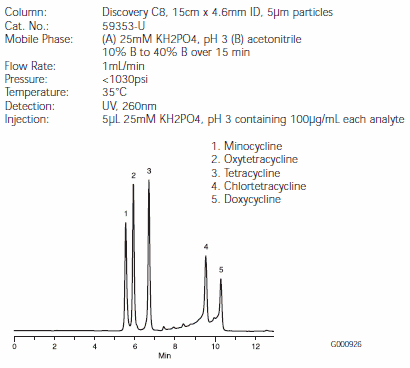
Rysunek D.Antybiotyki tetracyklinowe na kolumnie HPLC Discovery C8 (59353-U)
Zdolność fazy RP-AmideC16 do rozdzielania minocykliny i oksytetracykliny można wytłumaczyć wiązaniem wodorowym między funkcyjnością amidową fazy i funkcyjnością hydroksylową oksytetracykliny. Takie różnice w selektywności pokazują zalety stosowania kolumny amidowej do trudnego rozdzielania.
Badanie to wykazało, że mieszaniny antybiotyków tetracyklinowych można rozdzielić za pomocą HPLC z odwróconymi fazami, przy użyciu kolumn Discovery C18, Discovery C8 i Discovery RP-AmideC16. Z wyjątkiem koelucji tetracyklin minocykliny i oksytetracykliny na kolumnie Discovery C18, uzyskano doskonałą rozdzielczość w każdym rozdziale.
Referencje
Zaloguj się lub utwórz konto, aby kontynuować.
Nie masz konta użytkownika?