Az AAV-folyamat intenzifikálása magas sótartalmú lízis és sótűrő endonukleáz használatával
Ez az oldal leírja a sejtlízis legfontosabb szempontjait, valamint azt, hogy a magas sókoncentráció és a sótűrő endonukleáz kombinációja hogyan használható a vektor titerének és fertőzőképességének növelésére.

Bővebben
- A sejtlízisre vonatkozó megfontolások
- A sejtlízisre vonatkozó megfontolások
- A DNS-emésztéssel kapcsolatos megfontolások
- Sótűrő endonukleáz kifejlesztése AAV-vektorok előállításához
- A megfelelő benzonáz® kiválasztása az Ön alkalmazásához /a>
- A magas sótartalmú kihívás megoldása
- Benzonáz® GYIK
- Deviron® GYIK
- Kapcsolódó termékek
- Referenciák
Az adeno-asszociált vírus (AAV) vektorok előállítása egy olyan középső lépést tartalmaz, amely a sejtlízist és a nukleáz kezelést kombinálja. Itt detergenseket használnak a sejtek lipid kettősrétegének felbontására, felszabadítva a vektorokat, míg a gazdasejt DNS-ét és a megmaradt plazmidokat endonukleázzal a betegbiztonság biztosítása és a downstream folyamat hatékonyságának javítása érdekében. A maradék DNS-t 10 ng/dózis alá kell csökkenteni, és a fragmentum méretének körülbelül 200 bázispárnál kisebbnek kell lennie, ahogyan azt a 2020-as FDA Guidance for Gene Therapy Investigational New Drug Applications (Génterápiás új gyógyszerek vizsgálati kérelmére vonatkozó FDA útmutató) ajánlja.
A sejtlízisre vonatkozó megfontolások
A sejtlízis lépés látszólag egyszerű, mégis számos kihívást jelent. A sejtlízishez általánosan használt detergensek, mint például a TRITON™ X-100 (4-tert-oktil-fenol-polietoxilát), problémásak lehetnek. A TRITON™ X-100 nem engedélyezett használatát 2021 januárjától az Európai Bizottság az Európai Unióban betiltotta a REACH (vegyi anyagok regisztrálása, értékelése, engedélyezése és korlátozása) listán való feltüntetése miatt. Ez a jegyzékbe vétel, valamint az EU-ban történő felhasználásával kapcsolatos szigorú irányelvek a TRITON™ X-100 bomlástermékének endokrin és mutagén hatásai miatt történtek, amelyekről megállapították, hogy veszélyt jelentenek a betegekre és a környezetre.
A sejtlízishez használt detergens kiválasztásakor további szempont, hogy az ne károsítsa a vírusvektorokat és a vírusrészecskék fertőzőképességét, és ne zavarja a downstream folyamatot, ami a poliszorbátok használata esetén előfordulhat. A kiválasztott detergensnek továbbá módosíthatónak kell lennie a későbbi munkafolyamat lépésekben történő eltávolítás és kimutatás szempontjából.
Végezetül fontos megérteni a sókoncentráció hatását a sejtlízisre és a vektorhozamra. Az AAV-kapszidok felszabadítására használt lízispufferek korábban fiziológiás sókoncentrációt (150 mM NaCl) tartalmaztak. A legújabb publikációk azonban arról számoltak be, hogy a sókoncentráció 500 mM-ra történő emelése növeli a vektor részecskék számát és a fertőző titereket, valamint csökkenti az AAV aggregációt. Az alábbiakban leírtak szerint azonban a magas só negatívan befolyásolhatja a DNS-emésztés az AAV-vektor gyártási folyamatában.
A magas sókoncentráció hatása a középső lépések során az AAV-termelésre
Vizsgálatot végeztünk a sejtlízis során alkalmazott magasabb sókoncentráció hatásának meghatározására. AAV5 vektorokat állítottunk elő HEK293 sejtekben, amelyeket TRITON™ X-100, poliszorbát 20, Deviron® C16 vagy Deviron® 13-S9 segítségével lizáltunk. A folyamat során keletkezett kapszidok alapszámát 150 mM NaCl felhasználásával határoztuk meg poliszorbát 20 lízispufferben. A lízispufferben 500mM só használata az AAV5 kapszidtiterek átlagosan 29%-os növekedéséhez vezetett (1. ábra).

1. ábra.A nagy sótartalmú lízis hatása az AAV5-titerek előállítására.
A magas sókoncentráció hatása a középső lépések során az AAV-fertőzőképességre
Az 500 mM NaCl körülmények AAV-fertőzőképességre gyakorolt hatásának mérésére hasonló vizsgálatot végeztünk, amelyben AAV2 vektorokat állítottunk elő HEK293 sejtekben. Az alapszintű lízispuffer körülmények 150mM NaCl és poliszorbát 20 voltak. Amikor a sókoncentrációt 500mM-re növelték és különböző detergenseket alkalmaztak, a fertőzőképesség legalább 10-szeres növekedését figyelték meg (2. ábra). Amint fentebb említettük, a magas sókoncentráció lízis során történő alkalmazásának további előnye az AAV-aggregáció csökkenése.
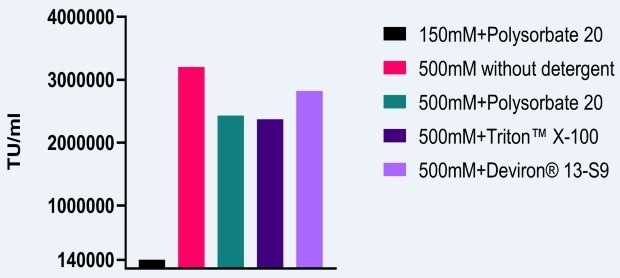
2. ábra.A nagy sótartalmú lízis hatása az AAV5 fertőzőképességre.
A DNS-emésztés megfontolásai
A sejtlízis lépéshez hasonlóan a DNS-emésztés is számos kihívást jelent. A legfontosabbak közé tartozik a megfelelő minőségű anyagok beszerzésének szükségessége a szabályozási követelmények teljesítése és az ellátási lánc stabilitásának biztosítása érdekében. A GMP mellett a tisztaság, a glikozilációs állapot és a biológiai terheltség is a figyelembe veendő tényezők közé tartozik. Az enzim magas sótartalommal szembeni toleranciája szintén kritikus tényező, amely megakadályozza a magas sókoncentrációk használatát az AAV-gyártás során.
Az AAV-gyártáshoz szükséges enzim kiválasztásának legfontosabb kritériumai
- IPEC PQG GMP vagy azzal egyenértékű elérhető, FDA DMF/BBMF
- >99%-os tisztaságú termék /li>
- Poszt-transzlációs módosításoktól mentes
- Mycoplasma teszt
- Kísérleti vírusok tesztje
- Endotoxin teszt
- Tailgate minták elérhetősége
- Logisztikailag erős &; Ellátási robusztusság
- Technikai támogatás az alkalmazással kapcsolatos kérdésekben
- Pontos kimutatási módszer
A DNS emésztéshez használt enzimet is hatékonyan el kell távolítani a feldolgozás során, és figyelembe kell venni az aktivitását a folyamatban használt sókoncentráció mellett. Míg a magasabb sókoncentráció javíthatja a vektor hozamát, addig a hagyományos endonukleáz enzimek és a DNS közötti kölcsönhatás nem jön létre nagy ionerősségnél, így megakadályozza a nukleinsav hasítását. Ez történelmileg azt jelentette, hogy a kívánt nukleáz aktivitást és a sókoncentrációt megfelelően egyensúlyba kellett hozni.

Sótűrő endonukleáz kifejlesztése AAV-vektorok előállításához
A sejtlízishez előnyben részesített magas sókoncentrációk mellett is hatékony aktivitású endonukleáz iránti igény kielégítésére fejlett fehérjemérnöki képességeket használtunk a Benzonase® Salt Tolerant endonukleáz kifejlesztésére. Ez a nem állati eredetű endonukleáz akár 1000 mM sókoncentrációban is képes a DNS és az RNS emésztésére, és IPEC, PQG, GMP és Emprove® Expert termékként kerül forgalomba.
A baktérium-expressziós rendszert használjuk a Benzonase® Salt Tolerant endonukleáz előállításához, mivel ez biztosítja a pontosan meghatározott molekulaméretet, a poszttranszlációs módosítások hiányát és a magas tételenkénti reprodukálhatóságot. Az alábbi adatok a Benzonase® Salt Tolerant endonukleáz aktivitását és előnyeit mutatják.
Fehérje profil
A baktérium expressziós rendszert használjuk a Benzonáz® Salt Tolerant endonukleáz előállításához, mivel ez biztosítja a pontosan meghatározott molekulaméretet, a poszt-transzlációs módosítások hiányát és a magas tételenkénti reprodukálhatóságot. A fehérje homogén profilja lehetővé teszi a pontos kimutatását immunvizsgálatokkal (pl. ELISA), ellentétben az élesztőben kifejezett enzimekkel, amelyek erősen glikoziláltak és nagy a tételenkénti poszt-transzlációs variabilitási profiljuk.

3. ábra.A benzonáz® sótűrő endonukleáz és a versenytárs A azonossága és tisztasága redukáló SDS-PAGE segítségével.

4. ábra.A benzonáz® sótűrő endonukleáz és a versenytárs A azonossága és tisztasága, amint azt a nem redukáló SDS-PAGE kimutatta.
Az E.coli benzonáz® sótűrő endonukleázból Emprove® Expert mutatja:
- Tiszta és tiszta fehérje
- Poszttranszlációs módosításoktól mentes
- Nagyfokú tételenkénti reprodukálhatóság
A 3. és 4. ábrán látható következtetés azt mutatja, hogy a Benzonase® Salt Tolerant endonukleáz Emprove® Expert pontosan meghatározott molekulamérettel rendelkezik. A magas sóban aktív referencia endonukleáz (Comp A) nem.
Endonukleáz aktivitás
Az endonukleázok aktivitásukhoz magnéziumra vannak utalva. Az 5. ábra a Benzonáz® sótűrő endonukleázok és a nem sótűrő nukleázok aktivitásának összehasonlítását mutatja be különböző magnéziumkoncentrációk mellett. A Benzonáz® Sótűrő endonukleáz aktivitását a magas sókoncentráció fokozta, és az aktivitás stabil volt 1-10 mM Mg2+ és 500 mM só tartományban. 150mM és 500mM só mellett a Benzonáz® sótűrő endonukleáz aktivitása hasonló volt a standard nukleázéhoz 10mM Mg2+ mellett (6. ábra).
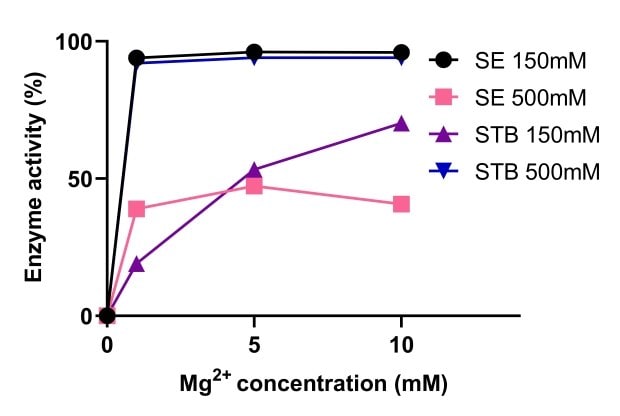
5. ábra.A benzonáz® sótűrő endonukleáz és egy nem sótűrő endonukleáz aktivitásának összehasonlítása.
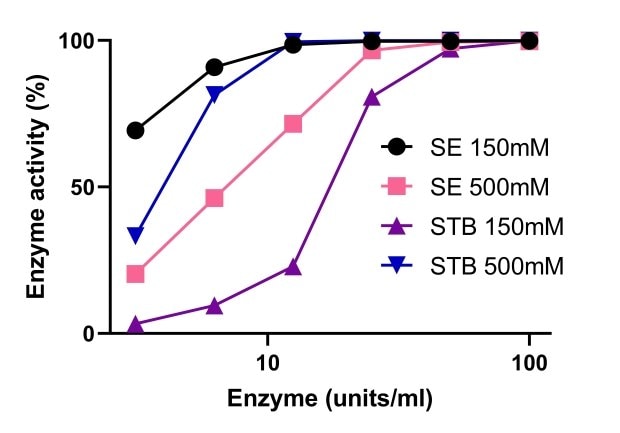
6. ábra.A benzonáz® sótűrő endonukleáz és egy nem sótűrő endonukleáz aktivitásának összehasonlítása.
A 7. ábra annak a vizsgálatnak az eredményeit mutatja, amelyben a DNS-t a Benzonase® Salt Tolerant endonukleázzal és más, kereskedelmi forgalomban kapható sóaktív és nem sóaktív endonukleázokkal emésztették 500 mM és 1 M NaCl mellett egy órán keresztül 37 °C-on. A benzonáz® Salt Tolerant endonukleáz teljesen megemésztette a DNS-t 500mM és 1M só mellett, és hasonló vagy jobb teljesítményt mutatott a többi endonukleázhoz képest.

7. ábra.A DNS-emésztés összehasonlítása benzonáz® sótűrő endonukleázzal és egy kereskedelmi forgalomban kapható sóaktív és egy nem sóaktív endonukleázzal 37°C-on egy órán keresztül.
Legend
M - GeneRuler Ultra Low Range DNS Ladder Cat# SM1213
Comp A ** - Sóaktív endonukleáz-kompetitor
b>SE - Standard endonukleáz mint Cat# 103773
STB - Benzonáz® sótűrő endonukleáz Emprove® Expert
Nukleinsav-fragmentum mérete
A benzonáz® sótűrő endonukleáz 10 bázispár méret alatt nem kimutatható mértékben emészti a DNS-t. A 8. ábra 4%-os agaróz gélen futtatott DNS-fragmentumokat mutat, alacsony molekulatömegű DNS-markerrel. A 150 mM só mellett a DNS nem emésztődött fel teljesen; 500 mM só mellett az emésztést követően nem maradtak DNS-fragmentumok.

8. ábra.25U/ml méretű DNS-fragmentum a benzonáz® sótűrő endonukleázzal 37°C-on 30 percig végzett emésztést követően.
A benzonáz® sótűrő endonukleáz és a detergensek kompatibilitása az AAV-vektorok előállításában
A benzonáz® sótűrő endonukleáz aktivitását négy különböző, sejtlízisre használt detergenssel együtt alkalmazva vizsgáltuk: TRITON™ X-100, poliszorbát 20, valamint a TRITON™ X-100 betiltására válaszul kifejlesztett két detergens-alternatívával - Deviron® C16 és 13-S9. Amint a 9. ábra mutatja, a Benzonase® Salt Tolerant endonukleáz aktivitását a négy detergens egyike sem befolyásolta. A DNS teljes mértékben emésztődött az 500 mM NaCl lízispufferben TRITON™ X-100, poliszorbát 20 és Deviron® 13-S9 jelenlétében (7B).
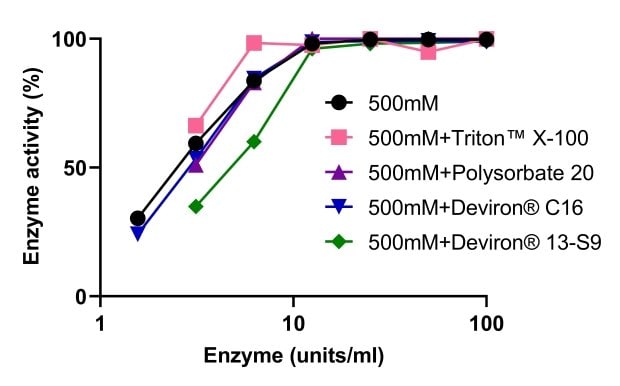
9. ábra.Benzonáz® Sótűrő endonukleáz aktivitás különböző detergensekkel kombinálva.

10. ábra.Benzonáz® A DNS sótűrő emésztése különböző detergensekkel kombinálva.
A megfelelő benzonáz® kiválasztása az Ön alkalmazásához
A benzonáz® Saltoleráns endonukleázt olyan alkalmazásokhoz kell használni, amelyekben a sókoncentráció 200 mM vagy magasabb. 500mM sókoncentrációnál a DNS teljesen emésztődik, és ahogy fentebb látható, 29%-os AAV titernövekedés és közel 2000%-os fertőzőképesség érhető el. A betegek biztonságát növeli a magas sótartalmú körülmények alkalmazása ebben a középső lépésben, mivel az AAV aggregációját akadályozza, és biztosítja a DNS hatékony eltávolítását a víruskapszidokról. A Benzonase® Salt Tolerant endonukleáz poszttranszlációs profilja biztosítja a gyógyszergyártásban a nem glikozilált és könnyen detektálható fehérje használatát is.
Azokhoz az alkalmazásokhoz, amelyekben a sókoncentráció 200 mM-nál kisebb, a Benzonáz® Safety Plus standard endonukleázt kell használni.
A 3. táblázat összefoglalja a három GMP Benzonáz® endonukleáz referenciánk specifikációit. A Benzonase® Salt Tolerant endonukleáz az Emprove® program része, amely segít a gyártóknak minimalizálni a fennakadásokat és alapos kockázatértékelést végezni a fejlesztésről a gyártásra való áttéréskor. A program olyan nyers- és kiindulási anyagokat biztosít, amelyek szigorúan minősítettek az iparág vezető szabványai szerint. A programban szereplő anyagokat átfogó dokumentációs csomagok támogatják, amelyek megfelelnek a gyógyszergyártók információs igényeinek a nyersanyagok minősítése, a kockázatértékelés elvégzése és a gyártási folyamat optimalizálása során.
A magas sókoncentráció kihívásának megoldása
A magas sókoncentráció alkalmazása az AAV-előállítás során a sejtlízis során magasabb titert és jobb fertőzőképességet biztosít. Történelmileg azonban ennek a megközelítésnek az alkalmazása nem volt praktikus, mivel a magas sókoncentráció gátolja a DNS-emésztéshez használt hagyományos endonukleázok aktivitását.
A Benzonáz® sótűrő endonukleáz elérhetősége lehetővé teszi 500 mM nagyságrendű sókoncentrációk beépítését a középső lízis és a DNS-emésztés lépése során, és kompatibilis az összes vizsgált detergenssel, beleértve a Deviron® detergenseket is, amelyek a TRITON™ X-100 alternatívájaként szolgálhatnak.
Az Benzonáz® sótűrő endonukleáz vagy a Deviron® portfólió termék mintájának kéréséhez kérjük, kattintson az alábbi linkre és töltse ki nagyon rövid webes űrlapunkat.
Benzonáz® GYIK
Meghatározás
Mi a benzonáz® endonukleáz?
A Benzonáz® endonukleáz a {hcég} tulajdonában lévő kereskedelmi név a kutatásban és biotechnológiai alkalmazásokban használt endonukleázok számára.
Milyen enzimek találhatók ezen a kereskedelmi néven?
A Benzonáz® endonukleáz család jelenleg két különböző enzimet tartalmaz.
- A hagyományos Benzonáz® endonukleáz termékcsalád, mint például a Benzonáz® Safety Plus endonukleáz, amelyet Serratia marcescensből izoláltak, és rekombinánsan állítottak elő E. coli K12 W3110 törzsben. A fehérje molekulatömege 30 kDa, izoelektromos pontja (PI) 6,85.
- Az új Benzonáz® sótűrő endonukleáz (1.4445). A legmodernebb fehérjemérnöki képességekkel tervezték, hogy a legmagasabb aktivitást biztosítsák magas sókoncentráció mellett.
A fehérje monomer, molekulatömege körülbelül 27 kDa, pI-je pH 9,68-nál. A ez a GYIK kifejezetten ezzel az enzimmel foglalkozik.
Hatásmód
Milyen típusú nukleinsavakra hat a benzonáz® nukleáz? Használhatom-e RNS izolálásakor?
A benzonáz® nukleáz egy promiszkusz endonukleáz, amely a DNS és az RNS minden formáját (egyszálú, kettős szálú, lineáris és cirkuláris) megtámadja és lebontja.
Mi a végeredménye a benzonáz® nukleáz általi teljes nukleinsavlebontásnak?
A benzonáz® nukleáz a nukleinsavakat teljesen lebontja 2-5 bázis hosszúságú, 5'-monofoszfát végződésű oligonukleotidokká.
Gátlás és eltávolítás
Hogyan lehet a benzonáz® nukleázt inaktiválni? Hogyan lehet eltávolítani?
A visszafordítható gátlás az EDTA segítségével érhető el az esszenciális fémionok kelátképzésével. Irreverzibilis inaktiválás csak extrém körülmények között (100 mM NaOH 70 °C-on 30 percig 70 °C-on) érhető el. A benzonáz kromatográfiával elválasztható a célterméktől. Ennek az endonukleáznak a robosztus jellege miatt azonban azt javasoljuk, hogy a benzonáz ne kerüljön felhasználásra, ha nukleázmentes végtermékre van szükség.
Miért nem működik a benzonáz® endonukleáz? Mi gátolja az aktivitását?
A Benzonáz® endonukleáz a működési feltételek széles skáláján aktív (lásd az enzim jellemzői bekezdést); azonban a Benzonáz® endonukleáz aktivitásához elengedhetetlen 1-2 mM Mg2+ koncentráció.
A Mn2+ helyettesítheti az Mg2+-t; az enzim azonban csak Mg2+ jelenlétében éri el optimális aktivitását. Egyértékű kationkoncentráció > 300 mM, foszfátkoncentráció > 100 mM és ammónium-szulfátkoncentráció > 100 mM gátolja (kb. 50%-os aktivitás). Ezenkívül > 1 mM EDTA koncentráció is gátolja a benzonáz® endonukleáz aktivitását.
Az aktivitás csökkenését tapasztalom: miért?
A benzonáz® endonukleáz általában nagyon stabil; ritka esetekben azonban megfigyelhető az aktivitás csökkenése. Ennek több oka is lehet: az irreverzibilis inaktiválódás oka lehet a mintában lévő denaturáló anyagok, pl. proteázok jelenléte; vagy pedig a helytelen tárolás. A reverzibilis inaktiváció általában kelátképző szerek, például EDTA jelenlétének köszönhető, amelyek eltávolítják az alapvető magnéziumionokat.
Hogyan távolíthatom el a benzonáz® endonukleázt egy bioprocesszáló sablonból?
A benzonáz® endonukleáz eltávolítása több downstream műveleti egységgel is elvégezhető, mint például mélységi szűrés a tisztításhoz, érintőleges áramlású szűrés (TFF) a koncentráláshoz és diafilterezés és kromatográfia (IEX, SEC, HIC). További információkért lásd a Függelék 2. fejezetének "A benzonáz® endonukleáz eltávolítása" című részét (36. oldal).
STÁBILITÁS ÉS MŰKÖDÉSI FELTÉTELEK
A Benzonáz®-endonukleázom kint maradt a padon. Még mindig jó?
A Benzonáz® endonukleázon kiterjedt stabilitási vizsgálatokat végeztünk, és megállapítottuk, hogy rendkívül stabil. A Benzonáz® endonukleáz még 37 °C-on történő hosszabb inkubáció esetén is több hónapig megőrizte > 90%-os aktivitását.
Más puffert szeretnék használni. Milyen feltételek feltétlenül szükségesek a Benzonáz® endonukleáz teljes aktivitásához? Mi csökkenti az aktivitását?
A benzonáz® endonukleáznak 1-2 mM Mg2+ szükséges az aktivitáshoz. A benzonázt gátolja (kb. 50%-os aktivitással) a monovalens kationok koncentrációja >50%, a foszfát koncentrációja >20 mM, és az ammónium-szulfát koncentrációja >25 mM.
Mennyivel több benzonáz® endonukleázt kell hozzáadnom, ha alacsony hőmérsékleten dolgozom?
A benzonáz® endonukleáznak 1-2 mM Mg2+ szükséges az aktivitáshoz. A benzonázt gátolja (kb. 50%-os aktivitás) az egyértékű kationok koncentrációja >50%, a foszfát koncentrációja >20 mM, valamint az ammónium-szulfát koncentrációja >25 mM.
Proteinkivonási alkalmazások
A Benzonáz® endnukleáz kompatibilis a proteáz inhibitor koktélokkal?
Igen. Azonban óvatosságra int, mivel sok proteáz inhibitor koktél tartalmaz EDTA-t. Az 1 mM EDTA-nál nagyobb koncentráció gátolja a Benzonáz® endonukleáz aktivitását.
A fehérjém oldhatatlan, és denaturáló körülmények között kell elvégeznem a tisztítást. A benzonáz® endonukleáz karbamidban is működni fog?
A benzonáz® endonukleáz aktivitása ténylegesen növekszik karbamid jelenlétében 6 M koncentrációig. 6 M karbamidnál az enzim aktivitása először növekszik, majd idővel csökken. 7 M karbamidnál a benzonáz® endonukleáz 15 perc után denaturálódik, és az aktivitás megszűnik. A nukleinsavak jelentős lebontása azonban még az inaktiválódás előtt bekövetkezik. A Benzonáz® endonukleáz magasabb kezdeti koncentrációja részben kompenzálhatja a 7 M karbamid hatását.
Miért van ennyi fajta Benzonáz® endonukleáz? Mit jelent a HC? Milyen hatása van a 90%-os és a 99%-os tisztaságnak?
A feldolgozási és költségigények lehető legszélesebb körének kielégítése érdekében a Benzonáz® endonukleáz két különböző tisztasági fokozatban kapható: I. tisztasági fokozat (99%-os tisztaságú) és II. tisztasági fokozat (90%-os tisztaságú). Mindkét minőség 25 U/μL vagy magas koncentrációban (HC), amely 250 U/μL-ben van meghatározva. Tömeges vásárlás esetén forduljon az Egyedi szolgáltatásokhoz.
A benzonáz® termékek teljes listájáért és a köztük lévő különbségekért látogasson el endonukleáz oldalunkra itt.
Mi a végeredménye a benzonáz® endonukleáz általi teljes nukleinsavlebontásnak?
A benzonáz® endonukleáz a nukleinsavakat teljesen lebontja 2-5 bázis hosszúságú, 5'-monofoszfát végződésű oligonukleotidokká.
BIOMEGYÁRTÁSI ALKALMAZÁSOK
Melyik minőségű/mennyiségű benzonáz® endonukleáz lesz megfelelő egy adott alkalmazáshoz?
A Benzonáz® endonukleáz aktivitását számos paraméter befolyásolja. Ezért az optimális feltételek folyamatonként eltérőek, és azokat kísérletileg kell meghatározni. A viszkozitás csökkentéséhez gyakran elegendő a II. tisztasági fokozatú (≥ 90%) benzonáz® endonukleáz. Standard vizsgálati körülmények között egy egység benzonáz® endonukleáz körülbelül annak az enzimmennyiségnek felel meg, amely 37 µg DNS 30 percen belüli teljes feltárásához szükséges.
Melyik lépésnél kell a Benzonáz® endonukleázt bevezetnem a folyamatomba?
A válasz erre a kérdésre attól függően változik, hogy miért használ Benzonáz® endonukleázt. A megadott alkalmazási példák remélhetőleg segítenek a kérdés megválaszolásában. Általános szabályként azonban a Benzonáz® endonukleázt általában a tenyésztés után és a befogási lépés előtt a legjobb hozzáadni.
A Benzonáz® endonukleáz biztonságos?
Igen, a Benzonáz® endonukleázzal toxikológiai vizsgálatokat végeztek (belső jelentések állnak rendelkezésre). A szisztémás toxicitást egyszeri alkalmazást követően egereken és patkányokon vizsgálták: még nagyon magas dózisok esetén sem észleltek toxikus hatásokat. Ezenkívül nem figyeltek meg mutagén potenciált egereknél, amelyeket intravénásan kezeltek, még a Benzonáz® endonukleáz nagyon nagy dózisával sem.
Miért nincs megadva az 5 millió egységnyi csövek töltési tartományának térfogata?
Mivel a Benzonáz® endonukleáz aktivitása (U/ml) gyártási tételenként változhat, úgy döntöttünk, hogy a tubusonkénti egységeket adjuk meg, de a térfogatot nem. A tubusonkénti térfogat könnyen kiszámítható az analitikai tanúsítványon (CoA) szereplő aktivitási információból.
BENZONÁZ® SÓTOLERÁNS ENDONUKLEÁZIS
A szekvencia hasonló a korábbi Benzonáz® termékekhez, mint például a Benzonáz® Safety Plus?
A Benzonáz® sótűrő endonukleáz egy vadonatúj enzim, amelyet a legmodernebb fehérjemérnöki módszerekkel úgy terveztek, hogy magas sókoncentráció mellett is a legmagasabb aktivitást biztosítsa. Más aminosav szekvenciával rendelkezik, mint a többi Benzonáz® örökölt termék.
Mi a különbség a működési feltételek tekintetében a korábbi Benzonáz® termékekhez képest?
A Benzonáz® sótűrő endonukleáz endonukleázként ugyanolyan feltételek mellett működik, mint a hagyományos Benzonáz® termékek. Kivételt képez a monovalens kationkoncentráció, ahol legalább 300 mM NaCl-t ajánlunk.
Hogyan lehet gátolni ezt az enzimet?
Az enzim gátolható EDTA hozzáadásával vagy hőhatásnak való kitettséggel.
Hogyan távolíthatom el ezt az enzimet?
Fentebb a "Hogyan távolíthatom el a benzonáz® endonukleázt egy biofeldolgozási sablonban?" című pontra hivatkozom.
Hogyan tudom kimutatni ennek az enzimnek a nyomait?
A Benzonáz® enzimünk esetében egy dedikált Elisa kit egészíti ki kínálatunkat, amely biztosítja a Benzonáz® sótűrő endonukleáz robusztus kimutatását.
Miért használjam ezt az enzimet más standard nukleázok helyett?
A piacon lévő összes bioprocesszáláshoz használt standard nukleáz nagyon hasonló aminosav-szekvencián alapul. Ez azt jelenti, hogy a nukleinsavak magas sókon történő emésztésére való képességük hasonló, és nem tekinthető optimálisnak.
Az egyértékű kationkoncentrációra vonatkozó hatékony működési feltételeik 0 és 200 mM között mozognak. Hasonlóan a biológiai folyamatokban előforduló fiziológiás sókoncentrációkhoz.
Párhuzamosan kimutatták, hogy a HEK sejtek lízise során a fiziológiás koncentráció feletti magasabb sókoncentrációk alkalmazása valódi hatással van a folyamat teljes hozamára. 500 mM NaCl-koncentráció esetén a fertőzőképesség és az AAV teljes visszanyerési aránya jelentősen magasabb, mint 150 mM sókoncentráció esetén.
Ezután sótűrő nukleáz használata szükséges a nukleinsav eltávolításához ilyen magas sókoncentráció mellett.
Még >200mM sókoncentrációnál is használhatok hagyományos nukleázokat?
A fiziológiásnál magasabb sókoncentrációnál a hagyományos nukleázok aktivitása drasztikusan csökken, ami további enzimek hozzáadásához és a hatóanyag-tisztítási folyamat bonyolításához vezet. Ez szintén rossz költséghatékonyságú, magasabb üzemeltetési költségekkel járó folyamathoz vezet. Ezért javasoljuk a sótűrő nukleázok használatát.
Megoldható-e más szállítók detektáló készleteivel a Benzonáz® sótűrő endonukleáz kimutatása? Mint más, más "sóaktív" nukleázokra specializálódott kitek?
A Benzonáz®Salt Tolerant Endonukleáz egy vadonatúj enzim, a saját detektáló kitjeinken kívül nincs olyan detektáló kit, amely képes lenne a piacon lévő detektáló kitek kimutatására.
Figyelem: Minden olyan termék, amelyet nem hivatalos Merck csatornán keresztül értékesítenek, és amelyen a "Benzonase®" kereskedelmi név szerepel, hamisított terméknek tekintendő.
Miért olyan fontos az expressziós gazdatest az enzimgyártásnál?
A fehérje expressziója többféle gyártási platformmal is megvalósítható. Az élesztő alapú és a baktérium alapú expresszió a legelterjedtebb. Mégis, a keletkező termékek nem hasonlóak, és a transzláció utáni módosítási profilok a használt platformtól függően eltérőek.
Az élesztőből kifejezett fehérjék erősen glikoziláltak és módosítottak, ami a termék felhasználása során különböző problémákhoz vezethet, mint például a gyenge kimutatási pontosság az antitestvizsgálatokkal.
A piacon lévő legfontosabb Salt Active Endonuclease-t élesztőben fejezik ki.
Miért befolyásolhatja a nukleázok transzláció utáni módosítása a kimutatási pontosságot és hatékonyságot?
A glikozilált fehérjék nem homogén profilt mutatnak (ahogy a 2. ábrán látható), amely nem reprodukálható tételről tételre. Mivel a standard kimutatási módszerek immunpróbákat használnak, az érdeklődésre számot tartó fehérje kimutatására létrehozott antitestek nem képesek lefedni az élesztő-expresszió során megfigyelt módosítások teljes spektrumát. Ez az antitest alapú kimutatási módszerek, például az Elisa Kitek gyenge kimutatási pontosságához vezet.
Milyen toxikológiai profilja van ennek az enzimnek?
A Benzonase® Salt Tolerant endonukleáz ugyanolyan toxikológiai profillal rendelkezik, mint a Benzonase® portfólió többi tagja.
Segíthet meghatározni, hogy melyik nukleáz lenne a legköltséghatékonyabb a folyamatomhoz? Szem előtt tartva a folyamat általános hatékonyságát és hozamát.
Nukleázok teljes portfóliójával rendelkezünk, amelyek megfelelnek az Ön szabályozási és folyamatfeltételekkel kapcsolatos igényeinek. Ne habozzon, kérje MSAT (Manufacturing Science And Technology) támogatásunkat a folyamatfejlesztéshez. Szakértőink lefedik a teljes gyártási sablonokat, az Upstream-től a Final Fill-ig.
Deviron® GYIK
Megtarthatom-e a TRITON™ X-100 használatát, ha nem az Európai Unióban tartózkodom?
A TRITON™ X-100 betiltásáról az ECHA1 a REACH2 rendelet alapján döntött. A fő mozgatórugó a termék emberi egészségre és környezetre gyakorolt magas toxicitása volt. Ezért ennek a terméknek a biotermelésből való kivonása az egyik legforróbb trend az iparágban. Az EU-n kívüli szabályozó ügynökségek is értékelni fogják a termék használatát, ami további betiltásokhoz vezet majd.
Miért nem használhatok kutatási minőségű mosószert a biogyártáshoz?
A mosószereket általában hatalmas mennyiségben, szerves kémiai láncreakciókkal állítják elő. Gyakran a nyersanyag minősége rossz, hogy az előállítási költségeket lecsökkentsék. Ez nagyon veszélyes szennyeződéseket eredményez a végtermékben, mint például dioxin vagy nitrozamin. Ezeket a kutatási minőségű mosószereket kizárólag tisztítási célokra használják, és nem kerülhetnek gyógyszerformulák közelébe.
Melyek a Deviron®-ra való áttérés legfontosabb lépései?
A Deviron® portfólió 3 tételben áll rendelkezésre GMP EXCiPACT gyártású termék. Ezekből a tételekből már most is kérhetők minták minősítési céllal. A termékeinkkel együtt érkező Emprove® dossziék tartalmaznak minden olyan információt, amely a szabályozó hatóságokhoz történő benyújtáshoz szükséges. A toxikológiai információk is könnyen elérhetők."
A Deviron®-t szeretném kipróbálni, de nincs hozzá szakértelmem, hogyan tudnak támogatni?
Az alkalmazással kapcsolatos támogatás tekintetében számíthat biogyártási szakértői csapatunkra, akik végigvezetik Önt ezen a változáson. Vegye fel a kapcsolatot Merck kapcsolattartójával, hogy ingyenes támogatást kapjon.
Mi a különbség az MQ400/Emprove® Evolve és az MQ500/Emprove® Expert (GMP) között?
Azért, hogy segítsük a hatósági kitöltést, különböző dokumentációs és minőségi programokat hoztunk létre, hogy segítsünk Önnek a megfelelő terméket a megfelelő alkalmazáshoz beszerezni. Kattintson az alábbi linkekre, ha többet szeretne megtudni a Emprove® és M-Clarity® programok. A Deviron® C16 Emprove® Evolve és a Deviron® 13-S9 Emprove® Expert az általunk kínált legmagasabb minőségi szintek közé tartozik.
Melyek a célalkalmazásokhoz ajánlott koncentrációk?
Vírus inaktiváláshoz a TRITON™ X-100-hoz használt ASTM3 E3042-16 a mai napig a monoklonális antitestek gyártásához használt dokumentum. Az iparban használt koncentrációk az alkalmazástól függően 0,5 és 1% között változnak.
A sejtlízis alkalmazásokhoz a koncentrációk széles skáláját használják, amelyek mind folyamat-specifikusak. Javasoljuk, hogy a folyamatfejlesztés során több koncentrációt próbáljanak ki párhuzamosan. Deviron® mosószereink legalább olyan hatékonyak, mint a TRITON™ X-100 vagy a poliszorbátok.
Kifejleszthetünk GMP kimutatási módszert a Deviron® számára?
K+F szakértőink a Deviron® portfóliónkhoz olyan kimutatási módszereket fejlesztettek ki, amelyeket átadhatunk ügyfeleinknek. A GMP-kimutatási módszerekhez azonban a Bioreliance® laboratóriumunk a megfelelő partner. Bármilyen kérdéssel forduljon hozzánk.
A Deviron® portfólió kompatibilis a sejtlízis alkalmazásokhoz használt Benzonázzal®?
A benzonáz® az AAV4 eljárásokban a DNS-emésztés arany standardja. A Deviron® portfólióját úgy fejlesztettük ki, hogy teljes mértékben kompatibilis legyen a Benzonase® Endonukleázokkal. A két portfólió együttes használata nem jár az enzimatikus aktivitás vagy a detergens tulajdonságok elvesztésével. Az alkalmazási adatok a Deviron® portfólió brosúrájában találhatók.
Milyen gyártási kapacitással rendelkezik a Deviron® portfólió?
A Deviron® portfólió a németországi darmstadti telephelyünkön jelenik meg, már több mint 100 tonna terméket tudunk kínálni évente. Ne habozzon, ha előrejelzést szeretne kapni tőlünk, hogy megbeszélhessük az esetspecifikus átfutási időket.
1Európai Vegyianyag-ügynökség
2Kémiai anyagok regisztrálása, értékelése, engedélyezése és korlátozása*
.3Amerikai szabvány vizsgálati módszerre
4Adeno Associated Virus
A TRITON a The Dow Chemical Company ("Dow") vagy a Dow valamely kapcsolt vállalatának védjegye, amelyet licenc alapján használnak.
Az AAV-folyamat intenzifikálása magas sótartalmú lízis és sótűrő endonukleáz alkalmazásával:
- Olvassa el az adatlapot "Benzonáz® sótűrő endonukleáz Emprove® Expert"
- Lásd a technikai posztert "AAV-folyamatok intenzifikálása magas sótűrő lízis és benzonáz® sótűrő endonukleáz használatával"
- Tekintse meg a család portfólió szórólapját "Explore the Benzonase® endonukleáz portfólió"
- Tekintse meg a Deviron® mosószerportfólió brosúra "Explore Greener Alternatives to Triton™ X-100 for Biopharmaceutical Applications"
Hivatkozások
Tájékoztatást és tanácsadást nyújtunk ügyfeleinknek legjobb tudásunk és képességeink szerint, de kötelezettség és felelősség nélkül. A hatályos törvényeket és rendeleteket ügyfeleinknek minden esetben be kell tartaniuk. Ez vonatkozik a harmadik felek jogaira is. Információink és tanácsaink nem mentesítik ügyfeleinket saját felelősségük alól, hogy ellenőrizzék termékeink alkalmasságát a tervezett célra.
Az olvasás folytatásához jelentkezzen be vagy hozzon létre egy felhasználói fiókot.
Még nem rendelkezik fiókkal?