Intelligens nanoszálas hálók, mint helyi gyógyszeradagoló platformok
Mitsuhiro Ebara1, 2, 3
1International Center for Materials Nanoarchitectonics (WPIMANA), National Institute for Materials Science (NIMS), 1-1 Namiki, Tsukuba, Ibaraki 305-0044, Japan, 2Graduate School of Pure and Applied Sciences, University of Tsukuba, 1-1-1 Tennodai, Tsukuba, Ibaraki 305-8577, Japan, 3Graduate School of Industrial Science and Technology, Tokyo University of Science, 6-3-1 Niijuku, Katsushika-Ku, Tokyo 125-8585, Japan
Material Matters™, 2020, 15.3
Bevezetés
A szálas anyagok egyre jelentősebb szerepet játszanak számos alkalmazásban, többek között a textíliákban, a nem szőtt anyagokban és a kompozit anyagokban. Különösen a polimer nanoszálak jelentenek izgalmas új anyagosztályt, amelyek figyelemre méltó tulajdonságaik, például a nagy fajlagos felület, a nagy porozitás, a nagy molekuláris igazodás és a nanoméretű hatások miatt jelentős figyelmet vonzanak ( 1A ábra).1 Ezen túlmenően a nanoszálak lehetővé teszik a különböző terápiás molekulák egyszerű beépítését, miközben bővítik a nanoszálak hatóanyag-terhelhetőségét és támogatják a beágyazott gyógyszermolekulák tartós felszabadulását (1B ábra). Emellett a polimer szálak makroszkopikus ömlesztett anyagként való könnyű manipulálhatósága potenciális felhasználási lehetőségeket biztosíthat beültethető helyi gyógyszeradagoló platformként.

1. ábra.A) A fólia és a nem szőtt nanoszálas hálók sematikus képei. B) Példák a nanoszálakba könnyen beépíthető különböző típusú molekulákra.
A nanoszálakat számos technikával lehet szintetizálni. Ezek közé tartozik a fázisszétválasztás, az önösszeszerelés, az elektrospinning, a húzás és a mikrofluidikai módszerek.2 Az egyik legszélesebb körben vizsgált technika az elektrospinning. Az elektrospinning egy viszonylag olcsó, egyszerű módszert kínál a mikro- és nanométeres skálán egységes átmérőjű, különböző folytonos szálak létrehozására.3 Sokoldalú is, mivel szinte bármilyen oldható vagy olvasztható polimer feldolgozható nanoszálakká.
A közelmúltban a tudományos közösség megújította érdeklődését a rendelkezésre álló funkcionális nanoszálak könyvtárának bővítése iránt különböző alkalmazások. Többféle összetételű nanoszálak például nanorészecskékkel, szén nanocsövekkel, kerámiákkal, biomolekulákkal és más anyagokkal kevert polimerek elektrospinningelésével állíthatók elő.4 Ezek a funkcionális nanoszálak ígéretesnek tűnnek a legkülönbözőbb alkalmazások, például a szövettechnológia, az érzékelők és a sebgyógyítás területén. Továbbá az "intelligens" tulajdonságokkal rendelkező nanoszálak felkeltették az érdeklődést olyan alkalmazások iránt, mint az áteresztőképesség, a nedvesíthetőség és a duzzadó/duzzadó viselkedés "on-off" kapcsolható szabályozása.5 Az intelligens nanoszálak előállításához speciális polimereket használnak; ezeket a polimereket fizikai vagy kémiai tulajdonságaik alapján különböző elnevezésekkel illetik, mint például "ingerekre reagáló", "környezetérzékeny", "intelligens" vagy "intelligens" polimerek. A következetesség és az egyértelműség érdekében a cikk további részében az "intelligens polimerek" kifejezést használjuk.
A nanoszálaknak van egy olyan tulajdonsága, amely lényegében meghatározza az okosságukat: az a képességük, hogy reagálnak a környezetükben bekövetkező nagyon csekély változásokra. A szerkezetükben bekövetkező gyors makroszkopikus változások és ezen átmenetek reverzibilitása bizonyítja ezen anyagok egyediségét. Az intelligens polimerekből készült nanoszálak gyors reakciósebességgel rendelkezhetnek a velük született tervezési tulajdonságaiknak köszönhetően.6 Ez az áttekintés az intelligens nanoszálas hálók, mint beültethető helyi gyógyszeradagoló platformok alkalmazására összpontosít, négyféle nanoszál bemutatásával, amint azt a 2. ábra mutatja. Ezek a nanoszálak tartós (A típus), on-off (B típus) gyógyszerfelszabadítási tulajdonságokkal rendelkeznek, valamint olyan nanoszálak, amelyek e típusok egyikének kombinációjaként léteznek a hőterápiával (C és D típus néven ismertek), amit hőforrás bevezetése tesz lehetővé.

2. ábra.Ebben a tanulmányban négyféle beültethető nanoszálas rendszer javasolt a helyi gyógyszeradagoló rendszerhez. Nanoszálak tartós (A típus) és on-off (B típus) hatóanyag-felszabadítási tulajdonságokkal, hőterápiával kombinálva (C és D típus).
A gyógyszerfelszabadulás szabályozása
Megőrzött hatóanyag-felszabadulás (A típus)
A tartós hatóanyag-felszabadulás technológiáját alkalmazó intelligens anyag egyik példája egy perifériás idegsérülések kezelésére tervezett nanoszálas háló. Ha egy seb perifériás idegkárosodást okoz, a beteg motoros bénulást, érzékszervi bénulást és vegetatív idegkárosodást szenvedhet. A perifériás idegsérülések szokásos kezelési módszerei közé tartozik a vágás közvetlen összevarrása vagy az idegek kinyerése és átültetése a test más részeiből. A közelmúltban előrelépés történt az idegek regenerációjának támogatására használt mesterséges idegek kifejlesztésében.
Kutatócsoportunk kifejlesztett egy nanoszálas hálót, amelyet közvetlenül a sérült perifériás idegek köré tekernek, hogy elősegítsék a regenerációt és helyreállítsák a működőképességet. A nanoszálas háló poli(e-kaprolaktonból) (PCL), egy biológiailag lebomló alifás poliészterből áll, amelyet az amerikai Élelmiszer- és Gyógyszerügyi Hivatal (FDA) jóváhagyott olyan biomedicinális alkalmazásokhoz, mint a gyógyszeradagolás, a szövetszerkezet-építési állványok és az implantátumanyagok.7 A tudósok a PCL-t gyűrűnyílásos polimerizációval szintetizálták egy iniciátor terminális hidroxilcsoportjaiból, ónoktoát (S3252) katalizátorral.8 ;PCL nanoszálakat állítottunk elő elektrospinning módszerrel 1,1,1,1,3,3,3,3-hexafluorizopropanol (HFIP, 105228) oldószerként.
A háló metilkobalamint (MeCbl) tartalmaz, egy aktív B12-vitamin-homológot, amely kedvezően szállítja az idegszövetekbe, és hatékonynak bizonyul az idegek regenerációjának és az idegsejtek túlélésének elősegítésében. A PCL nanoszálas hálók fokozatosan szabadították fel a MeCbl -t legalább 8 héten keresztül, amikor in vitro tesztelték ( 3A ábra). A MeCbl-t tartalmazó nanoszálas lapok helyi beültetése sikeresen hozzájárult a motoros és érzékszervi funkciók helyreállításához, az idegvezetési sebesség helyreállításához és a myelinizáció elősegítéséhez az isiászideg sérülését követően, anélkül, hogy befolyásolta volna a MeCbl plazmakoncentrációját.9
A PCL nanoszálas rendszereket egy immunmoduláló szerrel is teszteltük (3B ábra),10 inaktivált vírust (3C. ábra),11 és mikroRNS-t (3D. ábra) bazálsejtes karcinóma, prosztatarákos sejtek, illetve májrákos sejtek kezelésére. Ezek a példák a nanoszálas rendszerek előnyeire utalnak, amelyekbe a különböző típusú molekulák könnyen beépíthetők, függetlenül a molekula méretétől, alakjától, felületi töltésétől és hidrofilitásától.

3. ábra. A) A metilkobalamin (MeCbl) PCL nanoszálas hálókból történő gyógyszerfelszabadulási viselkedése. B) Immunmoduláló hatóanyaggal bevont nanoszálas háló sematikus képe a bazálsejtes karcinóma terápiájához. C) Pásztázó elektronmikroszkópos kép inaktivált vírusrészecskékkel módosított PCL nanoszálas hálóról prosztatarák terápiájához. D) Mikro-RNS 145 hatóanyag-leadásának viselkedése PCL nanoszálas hálóból.
Kikapcsolható hatóanyag-felszabadítás (B-típus)
A tartós hatóanyag-felszabadítás mellett a hatékony kemoterápia szempontjából kritikus fontosságú a hatóanyag beadásának időbeli szabályozása. A közelmúltban nagy figyelmet kapott egy új gyógyszerelési koncepció, az úgynevezett "dózissűrű kemoterápia", mivel a maximális tumorpusztítást a kemoterápia adagolásának növelésével, nem pedig az adagolás növelésével éri el. A kemoterápia heti adagjának beadása a 3 hetenkénti adagolás helyett lehetővé teszi, hogy a kezelés megszakítsa a daganatsejtek gyors növekedési fázisát.13 Tekintettel erre a helyzetre, az intelligens nanoszálas hálók alkalmasak lehetnek a külső ingerek által kiváltott időbeli gyógyszerfelszabadításra. Az intelligens nanoszálas hálók fejlesztésének egyik jelentős kihívása azonban a dinamikusan és reverzibilisen hangolható szálszerkezettel rendelkező nanoszálak tervezése mind nano-, mind makroszkopikus léptékben. Ezt N-izopropilakrilamid (NIPAAm, 731129) és egy UV-reaktív benzofenon (BP) konjugált komonomer elektroszálas kopolimerjével sikerült elérni.14 Ezek a foto-kereszthálózással, hőmérsékletre reagáló, polimer alapú nanoszálas hálók dinamikusan és reverzibilisen hangolható tulajdonságokat mutattak, beleértve a duzzadást/zsugorodást, a mechanikai szilárdságot és a porozitást. A módszer egyik hiányossága azonban az, hogy a BP hidrofób jellege miatt a konjugáció után csökken a kopolimer fázisátalakulási hőmérséklete. Ezért NIPAAm és N-hidroxi-metil-akrilamid (HMAAm) kopolimerek elektrospinningjével is előállítottunk intelligens nanoszálakat, mivel a HMAAm hidroxilcsoportjai ezt követően termikus kikeményítéssel térhálósodnak. A kopolimerek sikeres előállítása jól definiált, kb. 600-700 nm átmérőjű nanoszálas struktúrává, ahol a szálak a termikus keményítés után is megőrizték morfológiájukat.
A kapott térhálósított nanoszálak gyors és reverzibilis térfogatváltozást mutattak vizes közegben a testhőmérséklet körüli hőmérséklet-változási ciklusok hatására.15 A térhálósított nanoszálakból a dextrán ki-be kapcsolható felszabadulását figyelték meg. Hat melegítési ciklus után szinte az összes dextrán felszabadult a nanoszálakból, míg a hűtés során csak elhanyagolható mennyiségű dextrán szabadult fel. Ezek a hatóanyag-felszabadulási profilok azt mutatják, hogy a javasolt rendszer képes a betegség cirkadián ritmusára reagálva bizonyos mennyiségű hatóanyagot felszabadítani. Ez lehetővé teszi egy ilyen rendszer alkalmazását a cirkadián variációt mutató krónikus betegségek, mint például az asztma, a magas vérnyomás, a szívinfarktus és az ízületi gyulladás optimális kezelésére.
Kombináció hipertermiával
Fenntartott felszabadulás hővel (C típus)
Noha a kemoterápia történelmileg az elsődleges és áttétes rákbetegségek standard kezelése, klinikai előnyei még mindig korlátozottak, ha egyetlen rákellenes gyógyszert adunk. Ezért az elmúlt évtizedekben a klinikai gyakorlatban a különböző rákos megbetegedések kezelésére két vagy több klasszikus rákellenes gyógyszert tartalmazó kombinált kemoterápiás kezeléseket alkalmaztak. Például számos klinikai vizsgálat kimutatta a tumor méretének jelentős csökkenését, amikor a kemoterápiát más kezelésekkel, például sugárterápiával és hőterápiával kombinálták.16 A hőterápia, más néven hipertermia a rákkezelés egy olyan típusa, amelynek során a testszöveteket magas hőmérsékletnek (43-45 °C) teszik ki.
A hipertermia fokozhatja bizonyos rákellenes gyógyszerek, például a paclitaxel (PTX) hatását is, így egyes rákos sejtek érzékenyebbé válnak a kezelésre. Ezekből a szempontokból egy olyan intelligens nanoszálas rendszert terveztünk, amely a kemoterápia és a hipertermia kombinációját használja a hatékonyabb rákterápia érdekében (4A ábra).17 A hálót biológiailag lebomló PCL-ből állítottuk össze PTX-szel és mágneses nanorészecskékkel (MNP-k) (4B ábra). A PCL-háló in vitro vizsgálat során legalább 6 héten keresztül lassan szabadította fel a PTX-et. Az in vivo megfigyelt elhúzódó terápiás hatás a gyógyszer folyamatos felszabadulása a hálóból hosszabb időn keresztül, összehasonlítva a PTX közvetlen injekciózásával a tumor helyére. Emellett a szinergista rákellenes hatás a háló váltakozó mágneses térrel (AMF) történő gerjesztésekor is megvalósult, mivel a nanoszálban lévő MNP-k lokalizált hőt generáltak, ami hőindukált sejtpusztulást, valamint a PTX fokozott kemoterápiás hatását okozta.
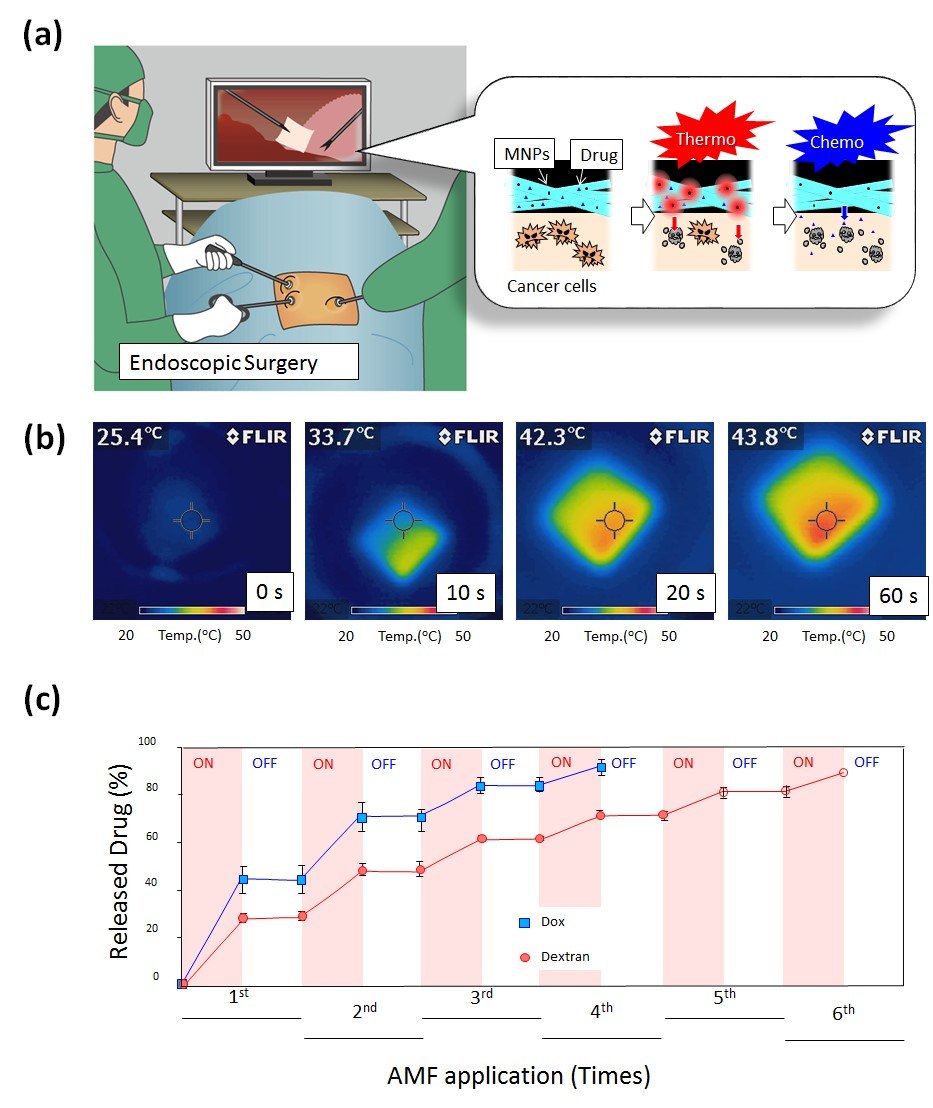
4. ábra. A) Sematikus ábrázolás a rákos termokemoterápiában alkalmazott on-off kapcsolható hőmérsékletre reagáló szálhálóról. B) Az MNP-kkel töltött nanoszálas háló infravörös hőképei AMF-ben. C) A DOX és a dextrán on-off kapcsolható gyógyszerfelszabadulási profilja a hőmérsékletre reagáló nanoszálas hálóból az AMF alkalmazására reagálva.
Az eredmények alapján az intelligens nanoszálas rendszer ígéretesnek tűnik a jövőben a rákterápiában, és új ismeretekkel szolgálhat a lokalizált termo-/kémoterápia jövőbeli fejlesztéséhez.
Kapcsolható, kikapcsolható hatóanyag-leadás hővel (D-típus)
A kikapcsolható, kapcsolható hatóanyag-leadó rendszerek a cirkadián óra szempontjából is figyelmet kaptak.18 A programozható, időzített hatóanyag-leadó rendszereket például kronoterapeutikumként használják. Ennek a rendszernek a hipertermikus kezelésekkel való kombinálása elősegíti a PTX által kiváltott apoptózist a kaszpáz-7 aktiválásán keresztül, növelve a G2/M-ben leállított sejtek arányát, ezáltal csökkentve a PTX IC50 értékét.
Ezeket a háttereket figyelembe véve egy intelligens hipertermia nanoszálas rendszert fejlesztettünk ki, amely az AMF be- és kikapcsolására reagálva egyidejű hőtermeléssel és gyógyszerfelszabadítással rendelkezik a rákos apoptózis indukciójára.19 A nanoszál egy kémiailag térhálósítható, hőmérsékletre reagáló polimerből, poli(NIPAAm-co-HMAAm)-ból, egy rákellenes hatóanyaggal (doxorubicin; DOX) és MNP-kből áll. A háló előállításához elektrospinning módszert alkalmaztunk.
A kémiai térhálósítás révén a nanoszálas háló az AMF váltakozó be- és kikapcsolására válaszul kapcsolható változásokat mutat a duzzadási arányban, mivel a beépített MNP-k öngenerált hője a nanoszálban lévő polimerhálózatok duzzadásának megszüntetését idézi elő, ami lehetővé teszi a DOX megfelelő be- és kikapcsolódó felszabadulásának megfigyelését a nanoszálakból az AMF hatására (4C ábra). A humán melanomasejtek 70%-a elpusztult az AMF 5 perces alkalmazása során az MNP-k és a DOX-ba épített nanoszálak jelenlétében a hő és a gyógyszer kettős hatása révén.
Ezt az intelligens hipertermiát tüdő adenokarcinómára is alkalmazták. A hőmérsékletre reagáló háló fázisátalakulási hőmérsékletét a 43 °C körüli enyhe hipertermia hőmérsékleti tartományba állították be. In vitro daganatellenes vizsgálatok kimutatták, hogy mind az MNP-vel, mind a PTX-szel töltött háló a sejtek mintegy 66%-át elpusztította, míg a csak PTX-szel töltött háló a sejtek mintegy 43%-át.20 Egy egér tüdőrákmodellben a termokemoterápiás kombináció fokozott daganatellenes aktivitást mutatott, kiküszöbölve a kemoterápiás szerek helyi felszabadulása miatt az egerekre gyakorolt szisztémás toxikus hatásokat. Úgy véljük, hogy az ilyen típusú javasolt szálrendszerek mintát nyújthatnak a biztonságos és hatékony rákkezeléshez szükséges helyi hatóanyag-leadó rendszerek következő generációjának tervezéséhez.
Következtetések
A különböző típusú, különböző gyártási fázisokban lévő szálakat már számos területen, többek között a nanotechnológia, a textilipar, az ipar, az üzemanyagcellák, a szövettechnológia, a regeneratív orvoslás és a bioanyagok területén számos alkalmazásban vizsgálták. Ezek a szálak, különösen a jól definiált nanoszálak, más anyagtípusokhoz képest elképesztő tulajdonságokkal rendelkeznek. Például a nagy fajlagos felület, a nagy porozitás és a biomimetikus tulajdonságok ígéretes alkalmazási lehetőségeket kínálnak.
Ezek közül a szálak közül azokat, amelyek stimuláló hatású közeggel kombinálhatók, intelligens szálaknak nevezik. Az intelligens szálak külső ingerek alkalmazásával távolról vezérelhetők, anélkül, hogy a szál egyéb jellemzői megváltoznának. Ezen intelligens szálak dinamikus jellege arra is felhasználható, hogy olyan mechanikai erőket idézzenek elő, amelyek a sejtek viselkedésének megváltozásához vezetnek.21 Az intelligens szálak összes előnyét figyelembe véve ezek az anyagok számos alkalmazásban eszközként hasznosíthatók.
Hivatkozások
Az olvasás folytatásához jelentkezzen be vagy hozzon létre egy felhasználói fiókot.
Még nem rendelkezik fiókkal?