Peptidkapcsoló reagensek útmutató
A szakasz áttekintése
- Related Materials
- In-situ Aktiváló-reagensek
- Foszfónium kontra urónium reagensek
- Az urónium és foszfónium kapcsolóreagensek összefoglalása /a>
- Referenciák
A Novabiochem® márka a piacon az in situ aktiváláshoz használt, kiváló minőségű kapcsolási reagensek egyik legkiterjedtebb választékát kínálja. A rendelkezésre álló reagensek ilyen sokasága mellett azonban nem mindig egyszerű kiválasztani az optimális csatolóreagenseket egy adott alkalmazáshoz. A kondenzációs reagensek a kapcsolási hatékonyság, a stabilitás, az oldhatóság vagy az aktív speciesek reaktivitása szempontjából különböznek.
In-situ aktiváló-reagensek
Az in situ aktiváló reagensek széles körben elterjedtek, mert könnyen kezelhetők, gyors reakciókat eredményeznek, még a sztérikusan akadályozott aminosavak között is, és alkalmazásuk általában mellékhatásoktól mentes. A legtöbbjük foszfónium- vagy aminium (korábbi nevén urónium) sókon alapul, amelyek egy tercier bázis jelenlétében a védett aminosavakat zökkenőmentesen képesek különböző aktivált fajokká alakítani (1. ábra). A Novabiochem® kapcsolóreagensek tulajdonságait az 1. táblázat foglalja össze.

1. ábra.A leggyakrabban használt kapcsolási reagensekkel előállított aktív észterek.
P1A1 = TOTU, P1A2 = HBTU/TBTU, P1A3 = HCTU, P1A4 = HATU, P1A5 = TSTU
P2A1 = COMU
P3A1 = PyOxim, P3A2 = PyBOP, P3A3 = PyClock, P3A4 = PyAOP.
A leggyakrabban használt reagensek, a BOP, a PyBOP és a HBTU OBt-észtereket hoznak létre, és ezek széles körben alkalmazásra kerültek a rutin SPPS és az oldatszintézisben a nehéz kapcsolásokhoz. Olyan kapcsolási reagensek is rendelkezésre állnak, amelyek az OBt-nél reaktívabb észtereket hoznak létre. A legfontosabbak a HATU2, PyAOP1,3 és a HCTU4, PyClocK, amelyek bázis jelenlétében a karbonsavakat a megfelelő OAt, illetve O-6-ClBt észterekké alakítják. Ezek az észterek a HOAt és HO-6-ClBt HOBt-hoz képest alacsonyabb pKa értéke miatt reaktívabbak, mint OBt társaik. Továbbá a HOAt további előnye a piridin-nitrogén, amely anchiomerikus segítséget nyújt a kapcsolási reakcióhoz, így a HATU és a PyAOP az OBt-sorozat leghatékonyabb kapcsolási reagensévé válik.
A közelmúltban vezették be az Oxyma Pure távozócsoporton alapuló kapcsolási reagenseket, amelyek közül a leghasznosabbak a COMU5,6 és a PyOxim7. Az e reagensek által létrehozott Oxyma-észterek relatív reaktivitására vonatkozó bizonyítékok nem egyértelműek. Az eredeti jelentések szerint ezek az Oxyma-alapú reagensek hatékonyabbak, mint a HOAt-alapúak, míg a mi házon belüli vizsgálataink8 szerint a HOAt-reagensek jobbak. Mindazonáltal az Oxyma-alapú reagensek mindig jobban teljesítenek, mint a HOBt (PyBOP, HBTU) és az O-6-ClBt (PyClocK és HCTU) alapúak. Az oxima alapú kapcsolási reagensek egyik különleges előnye, hogy nem a potenciálisan robbanásveszélyes triazolreagenseken alapulnak.
Kísérleteinkben úgy tűnik, hogy egy kapcsolási reagens hatékonysága szinte teljes mértékben az általa létrehozott aktív észter jellegével függ össze, a reakcióképesség sorrendje OAt> Oxyma Pure > 2-ClOBt > OBt. Úgy tűnt, hogy az urónium- vagy foszfóniumkomponens szerkezete kevéssé befolyásolja.
Foszfónium versus urónium-reagensek
A COMU kivételével az urónium-alapú reagensek DMF-ben lévő oldatai rendkívül stabilak, így ideálisak a kapcsolóreagensek előre elkészített oldatait használó szintetizátorokon való használatra. Ezzel szemben a foszfónium-reagensek DMF-ben lévő oldatai mérsékelten stabilak, ezért azokat zárt üvegekben kell tartani, és csak legfeljebb 2 napig szabad használni. A foszfóniumreagensek azonban lényegesen jobban oldódnak DMF-ben, mint az uróniumreagensek. Ennek fontos gyakorlati következményei vannak, mivel lehetővé teszi, hogy a reakciókat nagyobb koncentrációban végezzük el, és ezzel párhuzamosan javul a hatékonyság.
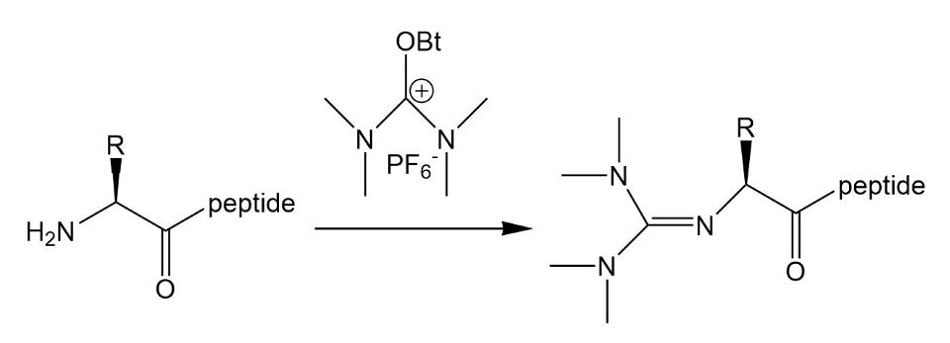
A foszfónium-kapcsolási reagensek általában tisztább reakciókat eredményeznek, mint az urónium-reagensek. Az utóbbiak a Nvégső aminocsoport9 guanidinyilálásával láncvégződéseket okozhatnak. Ez a mellékreakció különösen problematikus, ha a karboxilaktiválás lassú, például a fragmentálási és ciklizációs reakciók esetében, vagy ha felesleges uróniumreagens kerül alkalmazásra. Az ilyen melléktermékek képződése hosszú peptidek összeállításánál is nehézségeket okoz, mivel ezek a rövid pozitív töltésű peptidek elfedhetik a célion jelenlétét az ESI tömegspektrumban. Az uróniumreagensekkel ellentétben a foszfóniumreagensek feleslegben is használhatók, és akár egy lassú ciklizációs vagy fragmentum-kapcsolási reakció "táplálására" is felhasználhatók, hogy segítsék azok befejezéséhez.
Hivatkozások
Az olvasás folytatásához jelentkezzen be vagy hozzon létre egy felhasználói fiókot.
Még nem rendelkezik fiókkal?