以下頁面包含 HILIC 分離技術的介紹,以及開發極性和親水性化合物穩健分離方法的策略概述。
閱讀更多
什麼是 HILIC?
親水互動液相層析
HILIC 或親水互動液相層析是一種高效液相層析 (HPLC) 技術,用於分離極性和親水性化合物。最初,這種分離技術被稱為 "親水互動色譜法",偶爾也會使用 "Aqueous Normal Phase" 的表述。
簡單來說:HILIC 是一種正相分離類型,但使用的是反相型洗提液。
因此,HILIC 提供:
- 具有親水固定相的色譜柱
- 含有水、緩衝液和高濃度水混溶有機溶劑的洗滌液。
典型的 HILIC 應用使用濃度介於 50-95% 的乙腈,並加入水性緩衝液,例如甲酸銨、醋酸銨或其酸類,這些酸類在有機溶劑中具有高溶解度。HILIC 可與多種檢測技術搭配使用,例如結合電噴霧離子質譜法 (ESI-MS),HILIC 還可達到更高的靈敏度。

圖 1.比較 HILIC 和 RPLC 中的多肽分離。
HILIC的洗脫順序與RPLC(反相液相色譜)大致相反。在 RPLC 色譜柱的空隙容積中洗脫的化合物通常在 HILIC 中具有高保留率,反之亦然。

圖 2.HILIC 填補了色譜工具箱中的空白,但也與 RPLC、NPLC 和 IC 分離技術有部分重疊。

圖 3.使用 HILIC 成功分離化合物的範例。圖例:膽鹼(左上)、抗壞血酸(右上)、對甲苯磺酸(左下)和利塞膦酸(右下)。
HILIC 分離技術解決了許多以往難以解決的分離問題,包括分離小分子有機酸、基本藥物、陽離子、陰離子以及許多其他中性和帶電物質,因此受到廣泛關注。
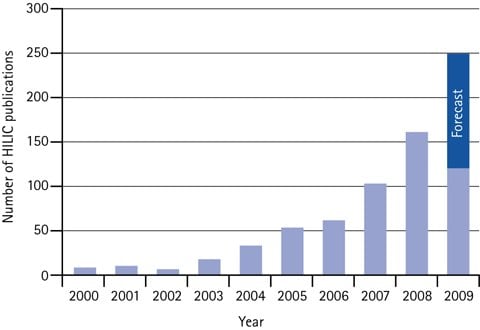
圖 4.2000 年至 2009 年中期的 HILIC 科學論文年數量,以及 2009 年的預測。
HILIC 的採用使得科學論文的引用次數呈指數級成長。
不具吸引力的替代方案>
由於目前的結合型 RPLC 固定相具有穩定性和可重複性,因此常用的策略是對 RPLC 進行調整,使其也能分離極性和親水性化合物。為了達到此目的,所採用的技術包括離子配對或膠束色譜、極性嵌入相和衍生化。RPLC 的這些轉變有時能完成工作,但也有許多限制,例如:MS 相容性低、固定相穩定性低、色譜柱出血、因多種干擾而耗費時間。
親水性化合物的穩健分離
相較於上述選項,HILIC 是針對極性和親水性化合物最直接、最多樣且最穩健的分離技術。近幾年來,具有高穩定性和可重複性的專用接合固定相開始用於 HILIC 分離,克服了以往 HILIC 相對於其他分離技術的局限性。此外,極性和親水化合物在含水的 HILIC 洗出液中具有良好的溶解性,這也是 HILIC 的優勢所在。
LC-UV和LC/MS的靈敏檢測
HILIC分離技術非常容易與多種檢測技術結合,例如紫外光吸收(UV)、螢光(FL)、折射率(RI)、蒸發光散射(ELSD)、帶電氣霧(CAD)和質譜(MS)。
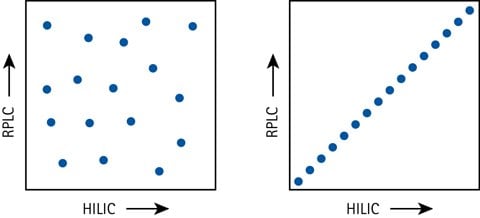
圖 5.HILIC 和 RPLC 在二維分離空間中的分離正交性示意圖 - 優異正交性 (左) vs 無正交性 (右)。
HILIC的一個吸引人的特點是與RPLC一起實現了2D分離能力。如果將正交性定義為二維分離空間的覆蓋率,HILIC-RPLC(或反之亦然)是液體分離技術中最正交的組合。與 HILIC 相比,IC 和 SEC(尺寸排阻色譜)等其他技術會導致更多的峰群或更差的解析度。
從同一樣品中獲得更多資訊
在 HILIC 和 RPLC 模式下運行同一樣品並合併數據,也可利用 HILIC-RPLC 正交性的優點。這可提供總樣品的更多資訊(圖 7),例如,可透過資料庫搜尋用於增強蛋白質識別,或用於樣品指紋分析方法。

圖 6.結合 HILIC 和 RPLC 的資料,從同一樣品中獲得更多資訊,這裡以 BSA 的胰蛋白酶消化法為例。

圖 7.造成色譜保留的 HILIC 分離過程。
目前的 HILIC 理論認為,HILIC 的保留是由於注入的分析物質溶質分子在流動相洗出液和親水性 HILIC 固定相中的富水層之間的分離造成的。
機理仍有爭議
儘管親水表面在接觸到有機溶劑和水的混合物時會保持水份這一點已被證實,但 HILIC 分離理論僅基於環境證據。有些研究指出了更多模式的分離機制,其中氫鍵以及偶極-偶極互作為重要的貢獻。不同 HILIC 固定相的選擇性差異也表明,造成色譜保留的作用不只一種。
幸運的是,這種缺乏詳細機理理解的情況並沒有限制 HILIC 在極性和親水性化合物分離方面的有效性。
調整保留
HILIC 中的保留和選擇性受到調整洗劑的影響,方法是改變有機溶劑的比例(和類型)、緩衝液的濃度(和類型)以及 pH 值。保留率會隨著有機溶劑比例的增加而增加,這是調整保留率最有效的方法。

圖 8.在 HILIC 中,不同洗脫液因素對於調整保留的相對近似重要性。
緩衝液和 pH 對離子化和可離子化分子的保留影響比中性分子更大,因為離子化分子更親水,因此在 HILIC 中保留更強。
有關 HILIC 機理以及不同溶劑和緩衝類型對分離的影響的更多資訊,請參閱小冊子 "A Practical Guide to HILIC"。
HILIC固定相由於 HILIC 只需要親水性表面來吸附和固定水層以進行分離過程,因此很容易讓人假設所有親水性固定相表面都適用於 HILIC,而且具有相同的性能。事實當然並非如此!不同類型的 HILIC 固定相之間的整體電荷、pH 依賴性、次要互動程度以及相穩定性都會有很大差異。
HILIC固定相的分類
原則上,HILIC固定相可分為中性、帶電和滋陽離子三類:
HILIC固定相可分為中性、帶電和滋陽離子三類。

圖 9.用於 HILIC 的不同類型固定相。中性 (上圖)、帶電 (中圖) 及齊聚物 (下圖)。
中性
- 無靜電互動
- 二元醇相、酰胺相
充電
- 白炭黑相、氨基丙基相
Zwitterionic
- 弱靜電互動
- SeQuant® ZIC®-HILIC ZIC®-HILIC和ZIC®-pHILIC相
好的和壞的二次交互作用
對於會隨 pH 值改變其特性的固定相(例如普通矽膠),保留與 pH 值之間會產生複雜的關係,使得預測和最佳化分離變得更加困難。

圖 10.在不同的 HILIC 固定相(普通矽膠和齊聚物)上保留帶有強正電荷的基本肽 Bradykinin (pI=12),說明太強的離子相互作用的影響。條件;40% 乙腈於乙酸銨緩衝液 (50 mM, pH 6.5)。
不同分析物之間的分離選擇性可能會受到靜電(離子)互動的影響,而靜電(離子)互動有助於帶電荷的 HILIC 固定相的保留。由於靜電相互作用太強,洗脫液中需要高濃度的鹽離子來破壞這些相互作用,以達到有效的洗脫。這是不利的,因為高濃度的鹽或緩衝劑會降低多種檢測技術 (包括 MS) 的靈敏度。使用鍵合的齊聚物來平衡固定相的電荷,是Merck的 SeQuant® ZIC®-HILIC 色譜柱所採用的設計策略,可達到兩全其美的效果。
用於 HILIC 流出液的溶劑
乙腈和其他極性有機溶劑
乙腈通常是 HILIC 的首選有機溶劑成分,因為它與水有良好的混溶性、良好的 HILIC 保留性和低粘度。然而,許多其他極性有機溶劑,如甲醇、乙醇、丙醇、異丙醇、二噁烷、丙酮和 DMF 等,也可用作 HILIC 洗提液中的非洗脱溶劑。HILIC 中的相對溶劑強度約為:丙酮 <;異丙醇 ~ 丙醇 <;乙腈 <;乙醇 <;二噁烷 <;DMF ~ 甲醇 <;水
利用溶劑控制保留
。
圖 11.保留因子 k 與洗提液中作為有機修飾劑的乙腈(閉合符號)或甲醇(開放符號)的濃度的關係。圖例;(三角形)胞嘧啶(正方形)腺嘌呤。
在 HILIC 中,改變保留率的最有效方法是調整有機溶劑成分的濃度。在 HILIC 中,保留率會隨著有機溶劑成分的增加而增加。
不過,我們已經意識到,保留因子 (k) 與流動相中有機溶劑成分之間的關係並非對數關係(RPLC 中通常是這種關係)。相反,通常觀察到的是對數關係。這造成的實際結果是,HILIC 梯度應該跑得更淺,因為有機溶劑濃度稍微調整,保留的變化就會更大。
若要繼續閱讀,請登入或建立帳戶。
還沒有帳戶?為便利客戶閱讀,此頁面中文以機器翻譯完成。雖然我們已盡力確保機器翻譯的準確性,但機器翻譯並非完美。如果您對機器翻譯的內容不滿意,請參考英文版本。