S1153
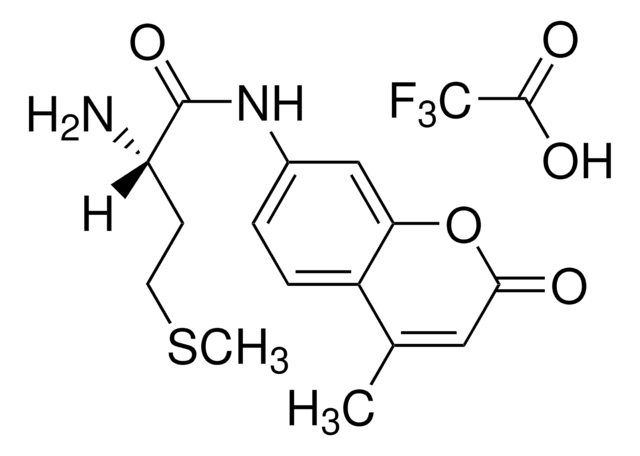
N-Succinyl-Leu-Tyr-7-amido-4-methylcoumarin
calpain substrate, solid
About This Item
Polecane produkty
product name
N-Succinyl-Leu-Tyr-7-amido-4-methylcoumarin, calpain substrate
Postać
solid
temp. przechowywania
−20°C
ciąg SMILES
CC(C)CC(NC(=O)CCC(O)=O)C(=O)NC(Cc1ccc(O)cc1)C(=O)Nc2ccc3C(C)=CC(=O)Oc3c2
InChI
1S/C29H33N3O8/c1-16(2)12-22(31-25(34)10-11-26(35)36)29(39)32-23(14-18-4-7-20(33)8-5-18)28(38)30-19-6-9-21-17(3)13-27(37)40-24(21)15-19/h4-9,13,15-16,22-23,33H,10-12,14H2,1-3H3,(H,30,38)(H,31,34)(H,32,39)(H,35,36)
Klucz InChI
RIYLNECMTVNMSO-UHFFFAOYSA-N
Szukasz podobnych produktów? Odwiedź Przewodnik dotyczący porównywania produktów
Substraty
Kod klasy składowania
11 - Combustible Solids
Klasa zagrożenia wodnego (WGK)
WGK 3
Temperatura zapłonu (°F)
Not applicable
Temperatura zapłonu (°C)
Not applicable
Środki ochrony indywidualnej
Eyeshields, Gloves, type N95 (US)
Certyfikaty analizy (CoA)
Poszukaj Certyfikaty analizy (CoA), wpisując numer partii/serii produktów. Numery serii i partii można znaleźć na etykiecie produktu po słowach „seria” lub „partia”.
Masz już ten produkt?
Dokumenty związane z niedawno zakupionymi produktami zostały zamieszczone w Bibliotece dokumentów.
Nasz zespół naukowców ma doświadczenie we wszystkich obszarach badań, w tym w naukach przyrodniczych, materiałoznawstwie, syntezie chemicznej, chromatografii, analityce i wielu innych dziedzinach.
Skontaktuj się z zespołem ds. pomocy technicznej