Wichtige Dokumente
SML3043
XL188
≥98% (HPLC)
Synonym(e):
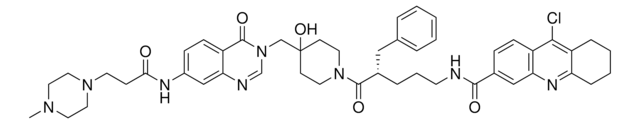
((R)-N-(3-((4-hydroxy-1-(3-phenylbutanoyl)piperidin-4-yl)methyl)-4-oxo-3,4-dihydroquinazolin-7-yl)-3-(4-methylpiperazin-1-yl)propanamide, N-[3,4-Dihydro-3-[[4-hydroxy-1-[(3R)-1-oxo-3-phenylbutyl]-4-piperidinyl]methyl]-4-oxo-7-quinazolinyl]-4-methyl-1-piperazinepropanamide, XL-188
About This Item
Empfohlene Produkte
Qualitätsniveau
Assay
≥98% (HPLC)
Form
powder
Farbe
white to beige
Löslichkeit
DMSO: 2 mg/mL, clear
Lagertemp.
2-8°C
SMILES String
O=C1N(CC2(O)CCN(C(C[C@@H](C)C3=CC=CC=C3)=O)CC2)C=NC4=CC(NC(CCN5CCN(C)CC5)=O)=CC=C41
InChI
1S/C32H42N6O4/c1-24(25-6-4-3-5-7-25)20-30(40)37-14-11-32(42,12-15-37)22-38-23-33-28-21-26(8-9-27(28)31(38)41)34-29(39)10-13-36-18-16-35(2)17-19-36/h3-9,21,23-24,42H,10-20,22H2,1-2H3,(H,34,39)/t24-/m1/s1
InChIKey
QLBYDWATOPNXBG-XMMPIXPASA-N
Biochem./physiol. Wirkung
Lagerklassenschlüssel
11 - Combustible Solids
WGK
WGK 3
Flammpunkt (°F)
Not applicable
Flammpunkt (°C)
Not applicable
Hier finden Sie alle aktuellen Versionen:
Analysenzertifikate (COA)
Die passende Version wird nicht angezeigt?
Wenn Sie eine bestimmte Version benötigen, können Sie anhand der Lot- oder Chargennummer nach einem spezifischen Zertifikat suchen.
Besitzen Sie dieses Produkt bereits?
In der Dokumentenbibliothek finden Sie die Dokumentation zu den Produkten, die Sie kürzlich erworben haben.
Unser Team von Wissenschaftlern verfügt über Erfahrung in allen Forschungsbereichen einschließlich Life Science, Materialwissenschaften, chemischer Synthese, Chromatographie, Analytik und vielen mehr..
Setzen Sie sich mit dem technischen Dienst in Verbindung.