ペロブスカイト型金属酸化物ナノ構造体
Yuanbing Mao1, Hongjun Zhou1, Stanislaus S. Wong1, 2
1Department of Chemistry, State University of New York at Stony Brook, Stony Brook, NY 11794-3400, 2Condensed Matter Physics and Materials Sciences Department, Brookhaven National Laboratory, Upton, NY 11973
Material Matters 2010, 5.2, 50.
Material Matters PDF版
ペロブスカイト型化合物の特性
ペロブスカイト型金属酸化物は、強誘電性、誘電性、焦電性、圧電性など、さまざまな興味深い物理的性質を示します1-4。具体的には、線形誘電体材料は、印加電場に比例して分極します。また、強誘電性セラミックスは永久電気双極子を持つ誘電体であり、電場を印加して双極子を配向させることができます。焦電性材料は自発分極を持ちますが、電場の印加によって分極方向を反転させることはできません。圧電体では、機械的応力によって電荷が発生するか、もしくは電場の印加によって機械的変形が生じます。一般に、このようなさまざまな特性は、材料が持つ結晶の対称性から生じます5,6。
このような各種材料のうち、強誘電性材料は焦電性と圧電性を有するだけでなく、電場を印加することによって電気双極子の向きを変えることができるため、現在大きな関心を集めています。ただし、強誘電性材料はすべて、キュリー温度(Tc)を超えると本来の極性を失い、常誘電体として知られる無極性状態に変化します。たとえば、チタン酸バリウム(BaTiO3、467634)は、キュリー温度である120℃で強誘電性正方晶相から常誘電性立方晶相に変化します。強誘電性材料の特性は温度がTCに近づくにつれて大きく変化し、Tcにおいて誘電率は最大となります。具体的には、BaTiO3の場合7、Tcより10 K低い温度からTcの間で誘電率の値が1,000から約10,000まで増加しますが、TCを超えると誘電率は徐々に低下します。このことから、BaTiO3の主な用途はこの相転移をはじめとする特性、特に誘電体としての可能性に基づいています。この相転移温度は、固溶体が生成するように他の金属酸化物で部分的にBaTiO3を置換することで調整することもできます。たとえば、結晶格子の大きさはドーパントによる置換で変化することから、相変化の起こる温度を変えることができます。ドープしたBaTiO3は、PTC(positive temperature coeffi cient、正の温度係数)サーミスタ、半導体、および圧電素子に幅広く利用されています8。
ペロブスカイト型材料のさまざまな物理的性質はその相転移と関連しているため、化学組成、純度、表面欠陥およびバルク欠陥の数、粒子径、焼結条件などの要素の影響を受けます。したがって、これらの材料から製造されるデバイスの品質を効果的に管理するには、これらのパラメーターの制御が不可欠です。たとえば、BaTiO3が持つ結晶構造に対する結晶子サイズの影響が研究されています。一例として、多くの場合、BaTiO3結晶の表面は立方晶ですがバルク内は正方晶であり、この2つの相は遷移領域(正方晶から立方晶へ連続的に構造が変わる層)によって分けられています。結晶子サイズが数マイクロメートル未満になると、表面からの影響を受ける結晶の割合が増加し、歪みのない正方晶相はすべて消滅します。このように、結晶が十分小さい場合(ナノサイズ)、強誘電性状態は完全に消滅して疑立方晶の超常誘電性状態(superparaelectric state)に置き換わります9。
一般に極めて高い融点を持つペロブスカイト型酸化物は、不均一触媒活性など、多くの興味深い化学的性質も示します。たとえば、これらの酸化物は、CO酸化、炭化水素および塩素化された揮発性有機化合物の酸化、メタンから合成ガスへの部分酸化、N2O分解、NOx還元、アルケンの水素化反応、SO2還元のほか、さまざまな電極触媒および光触媒反応に多く用いられます10,11。
緻密なペロブスカイト型複合金属酸化物には、高温(T > 600℃)で高い酸素透過性を示すものが多数存在します。これらの材料の中には、高温での酸素透過性が多孔質膜より優れているものがあります。たとえば、LiNbO3(254290)、SrCeO3、およびSrTiO3(517011)は、酸素輸送に適したペロブスカイト型酸化物の例です。これらの材料で作製した膜は密度が高いため、酸素に対して非常に優れた分離選択性を持っています。詳しく言えば、これらの材料の酸素輸送メカニズムは膜表面でのO2の酸化・還元と、緻密なセラミックスマトリックスを通過する酸化物イオンと電子の拡散から成っています。なお、この拡散は酸素ポテンシャル勾配を駆動力としています。これらの材料は高温で安定しており、しかも酸素透過性が高いため、酸化反応など多くの高温メンブレン反応器用途での検討が行われています12,13。
上述したように、BaTiO3やSrTiO3などの強誘電性ペロブスカイト酸化物は、高い非線形光学係数と高誘電率および低い損失特性を示します。これら新規物理的性質は、多くの場合、強い電子間相互作用によるものです。これらの効果は構造と有限サイズに依存する(たとえば、孤立した粒子の強誘電転移温度は平均粒径が約200 nmになると低下する可能性があります。)14,15ため、これらの強誘電体酸化物の純粋な結晶や薄膜についての(大きさ、形状、および形態の点で)適切な合成方法に関する研究が盛んに行われてきました16-18。バルクの強誘電体と比較した場合、低次元のナノスケール強誘電性構造体には、不揮発性強誘電体ランダムアクセスメモリー(NvFeRAM)の記憶密度を最大5倍に高める可能性があります19。
ペロブスカイト型金属酸化物材料の応用
多くの主要なペロブスカイト型複合金属酸化物について、その特性と応用20を表1に示します。これら材料の用途には、電気機械素子、トランスデューサー(変換器)、コンデンサ、アクチュエータ、High-k誘電体、DRAM、電場効果トランジスタ(FET)、論理回路などがあり、これらのエレクトロニクス用途に関連した材料固有の誘電性、強誘電性、圧電性、および焦電性といった特性を利用しています1,21,22。すべての強誘電性材料は焦電性と圧電性を共に有しており、この特性を用いた新たな用途に利用される可能性があります。
たとえば、強誘電性材料は、TCまたはその付近で分極を反転させる(切り換える)ことができるため、メモリへの応用が考えられます。特に、電子部品の小型化に伴い、セラミックコンデンサ、とりわけ最大の誘電率を持つセラミックス誘電体材料を使用した積層セラミックコンデンサ(MLCC:multilayer ceramic capacitor)が開発されています。より小さな空間により大きな静電容量を持ったコンデンサを開発するために、さらに複雑な多層構造も考案されています23。近年、内部Ni電極によって1~100 μFの静電容量を持つMLCCが作製されましたが、これは、厚さ約2 μmの薄膜誘電体を500層以上積層したものです8。
多くの関心を集めているもう1つの領域に、強誘電体薄膜の不揮発性コンピュータメモリへの応用があります20。現在のスタティックおよびダイナミックメモリチップ(SRAM、DRAM)では、メモリコンポーネントへの電源供給が停止すると、多くの場合、記憶情報は失われ回復することはできません。磁気記憶装置はこの問題に対する1つの解決策ですが、用途によっては、シリコンチップ内に集積化された低消費電力の軽量かつ高速なメモリの利用が必要になります。また、強誘電性材料は理論的には放射線場や磁場の影響を受けないと考えられていますが、一般的なメモリチップに記憶されたデータは放射線場や磁場によって破壊されてしまいます。強誘電性材料を使用した不揮発性メモリの主要な設計方法には、水平MIM構造と垂直MIM構造の2つがあります。これらの構造の主な特徴の1つは非破壊読み出し法ですが、これは、この種のメモリ素子が持つ一般的な問題です。つまり、メモリーセルを読み出すには分極させる必要がありますが、その際にセル内の情報は必ず消えてしまいます。この欠点はシステム設計で解決されており、一度セルの内容が最初に読み出された後、その情報によって再度、メモリへの書き換えが行われます。
現在研究されているもう1つの用途は、強誘電性材料を光コンピューター用の電気光学スイッチングデバイスとして使用することです13,20。このアイデアは、電場が印加されると屈折率が変わる強誘電性材料の性質を利用したものです。この材料を電気光学用途に使用できるかどうかは、膜厚、光の波長、電極の特性など多くの要素の影響を受けます。薄膜のもう1つの用途には、読み出し/書き込み用光記憶装置が考えられます。この用途での材料にはチタン酸ジルコン酸鉛ランタン(PLZT)などがあり、膜が印加電場の影響を受けている間、光ビームを照射した材料の状態は強誘電性と反強誘電性の間で切り替わります。薄膜の信号対雑音比(SN比)は一般に低いのですが、特定の薄膜PLZT系(約0.5 μm)では干渉効果を最適化すれば大幅に改善することができます。この種の光記憶装置は磁場の影響を比較的受けにくいため、コンピュータ磁気ハードディスクの光学的装置と考えることができます。
ペロブスカイト型材料の物理的性質の制御
これらの材料の物理的性質は、多くの場合、非化学量論相(nonintegral stoichiometric phase)または固溶体のいずれかを形成することによって調整されます。ペロブスカイト化合物の金属導電性は強いカチオン-アニオン-カチオン相互作用によるものであるため、化学的置換によりこれらの材料の構造を変えると、得られる材料の局所的秩序および特性に大きな影響を与えることが可能です。たとえば、CaTiO3-SrTiO3系はそのモデルとなる例です24,25。チタン酸ストロンチウムは立方晶のペロブスカイトであり、チタン酸カルシウム(633801)は歪んだ斜方晶のペロブスカイトです。Sr+2サイトをCa+2で置き換えたCaxSr1-xTiO3において、「x」の値は誘電率だけでなく材料の結晶相にも大きな影響を与え、斜方晶から正方晶、立方晶まで変化させることができます26-28。この材料が強誘電性または反強誘電性の相転移を起こすかどうかは、その正確な化学組成によって決まります29。その重要性を表す例としては、ナノサイズのCa0.7Sr0.3TiO3粒子の合成が可能な場合、高効率誘電体バリア放電によるプラズマを利用したCO2の無触媒分解での利用がより進む可能性があります28。
ペロブスカイト型材料の溶融塩合成
溶融塩合成(MSS:molten salt synthesis)法は、バルク材料の合成には以前から使われていましたが、この手法を用いた均一なナノ構造体は21世紀に入って初めて合成されました。Antoniettiら30は、高濃度の塩溶液とブロック共重合体界面活性剤を使用した「塩、金属、および金属酸化物ナノ粒子の簡便な合成法」を初めて報告しました。その後、アジアの研究グループ31-33が、界面活性剤(TWEEN®や、Triton® X-100など)の存在下でNaClを使用したMSS法により、平滑な単結晶のMn3O4、SnO2、およびCuOの1次元ナノ構造体を高い収率で調製し、観察されたナノワイヤー成長では、「オストワルド熟成」現象(微粒子が選択的に溶解し、より大きな粒子が成長する)が主に寄与していることを見いだしました。

図1BaTiO3ナノロッドとSrTiO3ナノキューブのSEM画像
我々の研究室では、MSS反応を使用することで直径50~80 nm、縦横比1 : 1~25 : 1を超える範囲の純粋なBaTiO3ナノ構造(ナノワイヤーを含む)と、一辺の平均長さが80 nmの単結晶SrTiO3ナノキューブを調製しました(図1)。MSS法は、化学的に純度の高い単一相の結晶質粉末を得るための、最も簡便で汎用性と費用効率の高い合成方法の1つです。この方法は従来の固相反応と比較して収率が高く、多くの場合、より低温かつ短い反応時間で残留不純物をほとんど含まない粉末を得ることができます34。この方法の長所は、その本質的な拡張性の高さ、一般化可能性(generalizability)、および簡便さのほか、反応媒質として基本的に塩を使用する点です34。実際、表2にまとめたように、(i)塩のアニオンの種類と大きさ、(ii)溶融塩自体の構成成分の溶解度/溶出速度、(iii)使用する塩または錯塩混合物の正確な融点、(iv)加熱温度と加熱時間、および、(v)関係する前駆物質固有の形態的(たとえば形状)および化学的組成、はすべて、成長速度だけでなく調整されたままの状態の粒子で得られる構造特性(サイズ、形状、および結晶性)にも影響を与える、重要かつ容易に制御できる要素です34-36。

表2ペロブスカイト型材料の合成に用いられるMSS法のフローチャートおよび得られる粒子に影響を与える要素
MSSは、たとえばNaClと非イオン界面活性剤(NP-9(ノニルフェニルエーテル))などを用いる、単純で容易にスケールアップが可能な固相反応です。以下の反応(反応式1および反応式2)は、ナノ材料の合成に関する推定されるメカニズムをまとめたものです。ここでは関連する例として、「M」(金属種)はBaまたはSrのいずれかを表します。
MC2O4 → MO + CO + CO2(反応式1)
MO + TiO2 → MTiO3(反応式2)
これらナノ構造の形成には用いる実験条件が極めて重要です。注目すべきは、特にBaTiO3とSrTiO3の場合、シュウ酸塩ではなく酸化物や塩化物などの別の前駆体物質を使用すると、単一相のチタン酸塩は得られず、かつナノ構造さえも得られない点です。さらに、反応温度を810℃(NaClの融点未満)に下げるなどのわずかな条件変更でさえ、得られるチタン酸塩は単一相ではなくなります。この熱的影響は、成長媒質の粘性の変化、つまり温度が上昇すると粘性が低下することによって説明できます。
更なる実験の結果37から、同じ実験条件(イオン強度、温度、もしくは界面活性剤の種類)を維持しても、使用する金属前駆体物質を変えることによって、さまざまな形状のペロブスカイトナノ構造を合成できることが明らかになっています。これは、得られる最終生成物の形態を決定する上で、金属前駆体物質と媒質である塩自体の間の界面エネルギーが重要であることを示唆しています。実際、ナノ結晶の形状は、結晶面に関連した相対的な比表面エネルギーによって決まります。すなわち、バリウムではナノワイヤーを作製できますが、ストロンチウムでは通常ナノキューブが合成されます。単結晶ナノ構造の最終的な形状は、対応する結晶格子の持つ固有の対称性を反映しています。
MSS法は、一連の単結晶Ca1–xSrxTiO3(0 ≤ x ≤ 1)ナノ粒子の調製にも使用されています38,39。得られるCa1–xSrxTiO3ナノ粒子の形状は、x値が小さくなると立方体から疑似球体に変化します。代表的なナノ粒子(図2)の大きさは、SrまたはCaの含有量に関係なく70~110 nmの範囲です。得られるナノ粒子の正確な化学的性質は、反応物質の比率を変えることによって容易に調整できます。ドーピングレベルの制御された材料の合成によって、今後は、材料の組成に依存する特性の研究が可能になると考えられます。たとえば、大きさが80±10 nmのSrTiO3ナノキューブは、バルクとは異なり強い1次ラマン散乱を示します。さらに、材料中のナノスケール強誘電性領域内で分極が高速に揺動して極性フォノンが妨げられ、これらSrTiO3ナノキューブやCa0.3Sr0.7TiO3のラマンスペクトルに、ファノ効果のような非対称の形状が生じることがあります39。
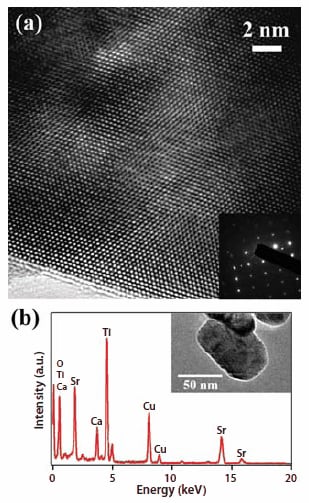
図2(a)Ca0.3Sr0.7TiO3ナノ粒子のHRTEM画像。挿入写真はそのSAED パターン。(b)合成したままのCa0.3Sr0.7TiO3ナノ粒子のEDSデータ。挿入写真は、典型的なTEM 画像。
最近、NaOH/KOH塩混合物を用いたMSS法による単結晶BaZrO3粒子40の合成において、ペロブスカイト金属酸化物の形状の効果的な制御が実現しています(図3)。適切なアニール温度にてアニール時間/反応時間を増やし、その他のパラメーターはすべて同じ条件に保つことによって、大部分が立方体である粒子の形態が、立方体と球体の混合物、さらに最終的にすべてが球体へと変化します。ペロブスカイト酸化物の物理的性質は構造に強く依存するため、その形状を制御することは非常に重要です41,42。たとえば、調整したままのサブミクロンスケールの試料は、バルクと比較して著しく高いフォトルミネセンス(PL)効率を持ち、特に球体の試料は立方体より強いPL信号を示しました。
![BaZrO<sub>3</sub>立方体:(<b>a</b>)典型的なTEM画像。(<b>b</b>)(a)の立方体の一部分のHRTEM画像([001]晶帯軸)、(<b>c</b>)立方体試料のSAEDパターン、(<b>d</b>)EDS。CuとCのピークはTEMのメッシュ(グリッド)に由来するものです。BaZrO<sub>3</sub>球体:(<b>e</b>)代表的なTEM顕微鏡写真、(<b>f</b>)(e)の球体の一部分のHRTEM画像([011]晶帯軸)。挿入写真はSAEDパターンです。 BaZrO3の各種分析画像](/deepweb/assets/sigmaaldrich/marketing/global/images/technical-documents/articles/materials-science-and-engineering/photovoltaics-and-solar-cells/fig3.gif)
図3BaZrO3立方体:(a)典型的なTEM画像。(b)(a)の立方体の一部分のHRTEM画像([001]晶帯軸)、(c)立方体試料のSAEDパターン、(d)EDS。CuとCのピークはTEMのメッシュ(グリッド)に由来するものです。BaZrO3球体:(e)代表的なTEM顕微鏡写真、(f)(e)の球体の一部分のHRTEM画像([011]晶帯軸)。挿入写真はSAEDパターンです。
我々の行った更なる実験43によって、比較的高品質のジルコン酸バリウムの合成にはアニール温度が高いこと、冷却速度が低いこと、および全体の反応時間が長いことが一般的に有利であることが明らかになりました。全体としての最適な反応条件という観点から、最も均一で高い結晶性と優れた分散度、かつ化学的に均質なサブミクロンサイズのBaZrO3粒子は、前駆体物質にBaC2O4とZrO2、溶融反応の媒質としてNaOH/KOHをそれぞれ用い、BaC2O4 : ZrO2 : 塩のモル比を1 : 1 : 20、加熱速度を5℃/分、反応温度を720℃とすることで得られます。アニール時間を短くする(たとえば30分)と同時に冷却速度を高くする(たとえば100℃/分)と、サイズの小さい立方体粒子が生成します。反対に、アニール時間を長くする(たとえば60~210分)と同時に冷却速度を低くする(たとえば5℃/分)か、そのいずれかだけでも粒子は立方体から球体に変化し、通常は立方体と球体の混合物が得られました。さらに、アニール時間を長くするか、または冷却速度を低くすると、サイズの大きな球体の粒子が生成されました。
この分野における今後の研究では、ナノスケールでの強誘電性、圧電性、および常誘電性の詳細な確認のほか、合成を最適化するためのナノ構造の形成と成長に関するメカニズムの研究が必要です。また、ペロブスカイトナノ構造の構造と物性との相関関係をより詳細に解明する研究が精力的に行われるでしょう。
参考文献
続きを確認するには、ログインするか、新規登録が必要です。
アカウントをお持ちではありませんか?