Co jsou to biomateriály?
Biokompatibilní polymery
Biodegradabilní polymery
Crosslinkers
Biokompatibilní anorganické materiály
Biokompatibilní anorganické materiály
.Supramolekulární chemie
Úvod
Během posledních dvou desetiletí bylo dosaženo významného pokroku ve vývoji .biokompatibilních a biodegradabilních materiálů pro biomedicínské aplikace a v případě druhé kategorie také pro průmyslové aplikace. V biomedicínské oblasti je cílem vyvinout a charakterizovat umělé materiály nebo, jinými slovy, "náhradní díly"1 pro použití v lidském těle za účelem měření, obnovy a zlepšení fyziologických funkcí a zvýšení přežití a kvality života. Obvykle se anorganické (kovy, keramika a skla) a polymerní (syntetické a přírodní) materiály používají pro takové položky, jako jsou umělé srdeční chlopně, (na bázi polymeru nebo uhlíku), syntetické krevní cévy, umělé kyčle (kovové nebo keramické), lékařská lepidla, stehy, zubní kompozity a polymery pro řízené pomalé podávání léků. Vývoj nových biokompatibilních materiálů zahrnuje úvahy, které jdou nad rámec netoxičnosti k bioaktivitě, pokud jde o interakci s biologickým prostředím a jeho časovou integraci do něj, jakož i další vlastnosti přizpůsobené v závislosti na konkrétní aplikaci.2
Souběžný obor "biomimetika" lze popsat jako "abstrakci dobrého designu z přírody" nebo jednoduše řečeno jako "kradení nápadů z přírody". Cílem je vyrábět materiály pro nebiologické použití na základě inspirace přírodou jejich kombinací s umělými, nebiologickými zařízeními nebo procesy. To se rychle stává novou hranicí výzkumu.
Biokompatibilní polymery
Jednou z oblastí intenzivní výzkumné činnosti je využití biokompatibilních polymerů pro řízené podávání léčiv. Vyvinula se z potřeby prodlouženého a lepšího řízení podávání léčiv. Cílem zařízení s řízeným uvolňováním je udržet léčivo v požadovaném terapeutickém rozmezí pouze jednou dávkou. Lokalizované podávání léčiva do určitého tělesného kompartmentu snižuje systémovou hladinu léčiva, snižuje potřebu následné péče, zachovává léčiva, která se v těle rychle ničí, a zvyšuje komfort pacienta a/nebo zlepšuje compliance. Rychlost uvolňování je obecně dána konstrukcí systému a je téměř nezávislá na podmínkách prostředí.3
Vhodná klasifikace systémů s řízeným uvolňováním je založena na mechanismu, který řídí uvolňování dané látky. Nejběžnějším mechanismem je difúze. Byly vyvinuty dva typy systémů s řízenou difuzí; prvním je zásobníkové zařízení, ve kterém bioaktivní látka (léčivo) tvoří jádro obklopené inertní difuzní bariérou (obrázek 1). Mezi tyto systémy patří membrány, kapsle, mikrokapsle, liposomy a dutá vlákna. Druhým typem je monolitické zařízení, ve kterém je účinná látka dispergována nebo rozpuštěna v inertním polymeru (obrázek 2). Stejně jako u zásobníkových systémů je rychlost limitujícím krokem difuze léčiva polymerní matricí a rychlost uvolňování je určena volbou polymeru a jeho následným vlivem na difuzní a rozdělovací koeficient uvolňovaného léčiva.3,4
V chemicky řízených systémech lze dosáhnout chemické kontroly pomocí bioerodovatelných nebo přívěsných řetězců. Důvodem pro použití bioerodibilních (nebo biologicky odbouratelných) systémů je skutečnost, že bioerodibilní zařízení jsou nakonec vstřebána organismem, a proto nemusí být chirurgicky odstraněna. Bioerozi polymerů lze definovat jako přeměnu materiálu, který je nerozpustný ve vodě, na materiál rozpustný ve vodě. V bioerodibilním systému je léčivo v ideálním případě rovnoměrně rozloženo v polymeru stejným způsobem jako v monolitických systémech. Jak se polymer obklopující léčivo eroduje, léčivo uniká (obrázek 3). V systému s visícím řetězcem je léčivo kovalentně vázáno na polymer a uvolňuje se štěpením vazby vlivem vody nebo enzymů.5,6 V systémech řízených rozpouštědlem je účinná látka rozpuštěna nebo rozptýlena v polymerní matrici a není schopna touto matricí difundovat. V jednom typu rozpouštědlem řízeného systému při pronikání okolní tekutiny (např. vody) do matrice polymer nabobtná a jeho teplota skelného přechodu se sníží pod teplotu prostředí (hostitele).7 Nabobtnalý polymer je tedy v gumovitém stavu a umožňuje léčivé látce v něm obsažené difundovat zapouzdřením.
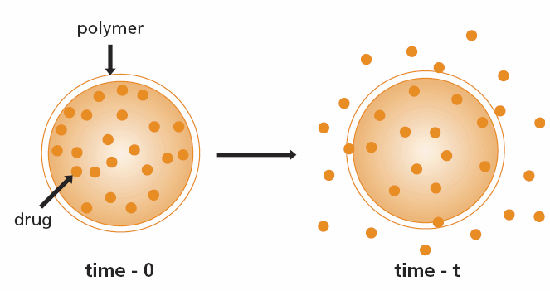
Obrázek 1.Schematické znázornění zásobníkového zařízení s řízenou difuzí léčiv.
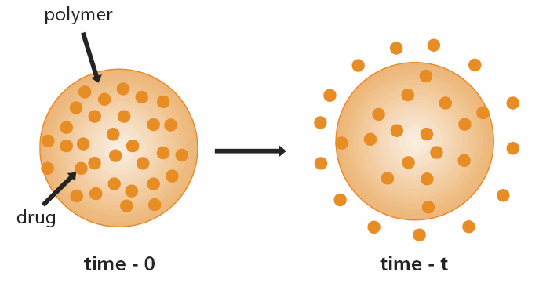
Obrázek 2.Schematické znázornění monolitického (matricového) zařízení s řízenou difuzí léčiv.
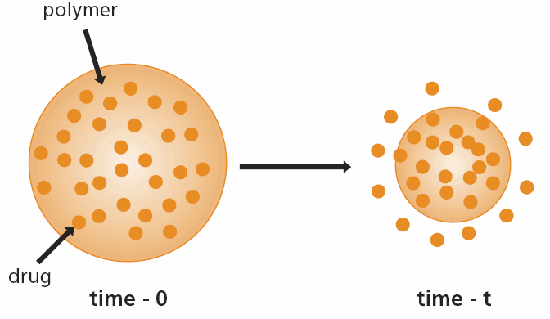
Obrázek 3.Schematické znázornění biodegradabilního (bioerodibilního) zařízení pro podávání léčiv.
Biodegradabilní polymery
Rozmanité přírodní, syntetické a biosyntetické polymery jsou biologicky a ekologicky rozložitelné. Polymer založený na C-C páteři bývá biologicky nerozložitelný, zatímco polymerní páteře obsahující heteroatomy biologickou rozložitelnost propůjčují. Biologickou rozložitelnost lze proto do polymerů upravit uvážlivým přidáním chemických vazeb, jako jsou mimo jiné anhydridové, esterové nebo amidové vazby. Obrázek 4 uvádí schematické znázornění typů rozkladu polymerů. Mechanismus degradace spočívá v hydrolýze nebo enzymatickém štěpení, které vede ke štěpení páteře polymeru. Makroorganismy mohou polymery požírat a někdy i trávit a také iniciovat mechanické, chemické nebo enzymatické stárnutí.8
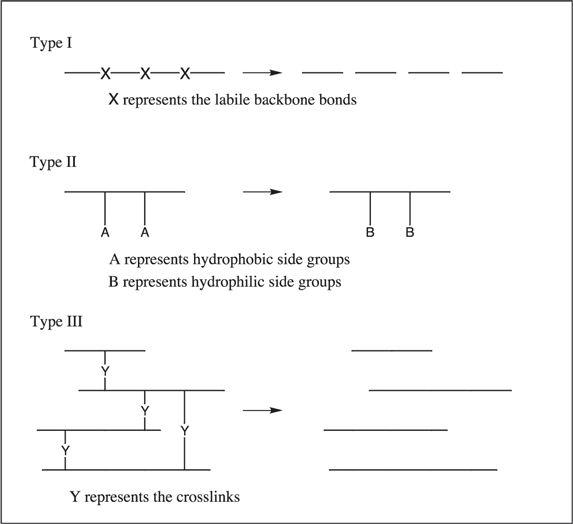
Obrázek 4.Schematické znázornění typů degradace polymerů.9
Biodegradabilní polymery s hydrolyzovatelnými chemickými vazbami jsou předmětem intenzivního výzkumu pro biomedicínské, farmaceutické, zemědělské a obalové aplikace.10 Aby mohl být použit ve zdravotnických prostředcích a aplikacích s řízeným uvolňováním léčiv, musí být biodegradabilní polymer biokompatibilní a splňovat další kritéria, aby mohl být kvalifikován jako biomateriál - zpracovatelný, sterilizovatelný a schopný řízené stability nebo degradace v závislosti na biologických podmínkách.11 Degradační produkty často definují biokompatibilitu polymeru, nikoli nutně polymer samotný. Poly(estery) na bázi polylaktidu (PLA), polyglykolidu (PGA), polykaprolaktonu (PCL) a jejich kopolymerů se hojně používají jako biomateriály.12,13 Degradací těchto materiálů vznikají odpovídající hydroxykyseliny, takže jsou bezpečné pro použití in vivo.
Mezi další bio/environmentálně degradovatelné polymery patří poly(hydroxyalkanoáty)třídy PHB-PHV, další poly(estery)a přírodní polymery, zejména modifikované poly(sacharidy), např, škrob, celulóza a chitosan.
Chitosan je technologicky významný biomateriál. Chitin je po celulóze druhým nejrozšířenějším přírodním polymerem na světě. Po deacetylaci z něj vzniká nový biomateriál chitosan, který po další hydrolýze poskytuje oligosacharid s extrémně nízkou molekulovou hmotností (schéma 1). Chitosan má širokou škálu užitečných vlastností. Konkrétně se jedná o biokompatibilní, antibakteriální a ekologicky šetrný polyelektrolyt, který se tak hodí pro celou řadu aplikací14 včetně úpravy vody, chromatografie, přísad do kosmetiky, úpravy textilií pro antimikrobiální aktivitu,které se dají použít v praxi.sup>15 nová vlákna pro textilie, fotografické papíry, biologicky rozložitelné filmy,16 biomedicínská zařízení a mikrokapslové implantáty pro řízené uvolňování při podávání léčiv.17-19
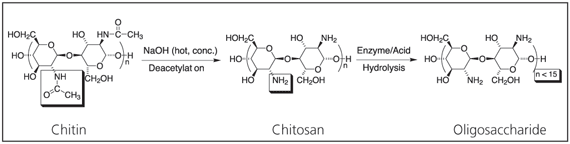
Schéma 1.Deacetylace chitinu za vzniku chitosanu a hydrolýza za vzniku oligosacharidu.
Poly(ethylenglykoly)s se poprvé objevily v americkém lékopise v roce 1950. Od té doby se stále častěji používají pro různé farmaceutické aplikace.
Víceblokové kopolymery poly(ethylenoxidu) (PEO) a poly(butylentereftalátu) (PBT) se také vyvíjejí jako protetické pomůcky a umělá kůže a jako scaffoldy pro tkáňové inženýrství.20 Tyto materiály podléhají hydrolýze (přes esterové vazby) i oxidaci (přes éterové vazby). Rychlost degradace je ovlivněna molekulovou hmotností a obsahem PEO. Navíc kopolymer s nejvyšší absorpcí vody degraduje nejrychleji.
Široce používaným nedegradovatelným polymerem je kopolymer ethylen-vinylacetátu. Tento kopolymer vykazuje vynikající biokompatibilitu, fyzikální stabilitu, biologickou inertnost a zpracovatelnost. Při aplikaci pro podávání léčiv tyto kopolymery obvykle obsahují 30-50 hmotnostních procent vinylacetátu. Membrána kopolymeru ethylenu a vinylacetátu působí jako bariéra omezující rychlost difúze léčiva. Ve třídě degradovatelných polymerů typu II je prvním krokem v procesu degradace přeměna hydrofobních substituentů na hydrofilní postranní skupiny. Tým výzkumníků se zabýval problémem výroby biodegradabilních polymerních scaffoldů s otevřenými póry pro výsev buněk nebo jiné aplikace tkáňového inženýrství.21 Zvoleným materiálem byl polykarbonát odvozený od tyrosinu poly(DTE-co-DT karbonát), ve kterém je pendantní skupinou prostřednictvím tyrosinu, aminokyseliny, buď ethylester (DTE), nebo volný karboxylát (DT). Změnou poměru DTE a DT lze manipulovat s hydrofobní/hydrofilní rovnováhou materiálu a rychlostí rozkladu in vivo. Ukázalo se, že se zvyšujícím se obsahem DT se zmenšuje velikost pórů, polymery se stávají hydrofilnějšími a aniontovějšími a buňky se na ně snadněji připojují.
Vodou nasákavé polymerní sítě mohou fungovat jako hydrogely na jednom konci nebo jako superabsorbéry na druhém konci. Hydrogely se vyznačují výraznou afinitou svých chemických struktur k vodným roztokům, ve kterých spíše bobtnají, než aby se rozpouštěly. Takové polymerní sítě mohou být v rozmezí od mírně absorpčních, kdy obvykle zadržují 30 % hmot. vody ve své struktuře, až po superabsorpční, kdy zadržují mnohonásobek své hmotnosti vodných kapalin. Pro přípravu absorpčních polymerů bylo navrženo několik syntetických strategií22 včetně:
- Polyelektrolyt(y) podrobený(é) kovalentnímu zesíťování23
- Sociativní polymery sestávající z hydrofilních a hydrofobních složek (&sup>23 ), které se skládají z hydrofilních a hydrofobních složek (&sup>23).quot;účinných" příčných vazeb prostřednictvím vodíkové vazby)24-26
- Fyzikálně se prolínající polymerní sítě poskytující absorpční polymery s vysokou mechanickou pevností.27
Je zřejmé, že tyto strategie se vzájemně nevylučují, a úsilí se zaměřilo na přizpůsobení kompozitních gelů, které jsou kriticky závislé na rovnováze mezi interakcemi polymer-polymer a polymer-rozpouštědlo při různých podnětech, včetně změn teploty, pH, iontové síly, rozpouštědla, koncentrace, tlaku, napětí, intenzity světla a elektrických nebo magnetických polí.28,29 Takové polymery reagující na podněty, tzv. chytré gely, jsou nadále předmětem rozsáhlého výzkumu pro aplikace v různých oblastech. Tyto aplikace sahají od biomedicínských (řízené uvolňování léčiv, oční zařízení a biomimetika),30-32 zemědělských (půdní přísada pro zachování vody, obalení kořenů rostlin pro zvýšení dostupnosti vody a obalení semen pro zvýšení klíčivosti) a osobní hygieny (plenky a hygienické výrobky pro dospělé),31 32 sup>23,33 až po průmyslové (zahušťovadlo, želírovací prostředek, obal na kabely, speciální obaly, snížení lepivosti přírodního kaučuku a odvodnění jemného uhlí).34-37
Absorpční polymery mohou být syntetického (petrochemického) původu, kde vliv morfologie a pórovitosti ovlivňuje absorpční vlastnosti.38 Sigma-Aldrich nabízí také rozsáhlý výběr polymerů přírodního (škroby atd.) a polosyntetického (ethery celulózy atd.) původu pro použití při syntéze vícesložkových hydrogelů.39 Na pomoc při navrhování hydrogelu pro konkrétní aplikaci nabízí společnost Sigma-Aldrich více než 1 500 monomerů a široký výběr síťovacích činidel.
Síťovací činidla
Síťování je tvorba chemických vazeb mezi molekulárními řetězci za vzniku trojrozměrné sítě propojených molekul. Příkladem síťování je vulkanizace kaučuku pomocí elementární síry, která přeměňuje surový kaučuk ze slabého plastu na vysoce pružný elastomer. Strategie kovalentního síťování se používá v několika dalších komerčně i vědecky zajímavých technologiích pro kontrolu a zlepšení vlastností výsledného polymerního systému nebo rozhraní, jako jsou termosety a nátěrové hmoty.40-42
Síťování bylo použito při syntéze iontově výměnných pryskyřic43 a stimulačně reagujících hydrogelů44 vyrobených z polymerních molekul obsahujících polární skupiny. Jako polyelektrolyty jsou hydrogely ze své podstaty rozpustné ve vodě. Aby se staly nerozpustnými, jsou chemicky zesíťovány během výroby nebo druhou reakcí následující po polymeraci výchozích monomerů. Stupeň zesíťování, kvantifikovaný z hlediska hustoty zesíťování, má spolu s detaily molekulární struktury zásadní vliv na bobtnací vlastnosti zesíťovaného systému. Na obrázku 4, ztráta zesíťování v reakci na specifické biologické podmínky vede k degradaci polymeru typu III.
Biokompatibilní anorganické materiály
Keramika může vyvolat představu takových předmětů, jako jsou čajové konvice a dlaždice. Existuje však mnoho dalších aplikací, které jsou zajímavé z technického hlediska a stále častěji i v biomedicínské oblasti. Biokeramika může mít strukturální funkci jako náhrada kloubů nebo tkání, může být použita jako povlak pro zlepšení biokompatibility kovových implantátů a může fungovat jako resorbovatelná mřížka, která poskytuje dočasné struktury a kostru, která se rozpouští, nahrazuje, když tělo obnovuje tkáň. Tepelná a chemická stabilita keramiky, její vysoká pevnost, odolnost proti opotřebení a trvanlivost přispívají k tomu, že keramika je vhodným materiálem pro chirurgické implantáty. Některé keramiky mají dokonce schopnost dodávat léčiva.
Materiály pro chirurgické implantáty a zdravotnické prostředky musí být především netoxické. Biokeramika tento test splňuje a navíc může být bioinertní, tj. neinteragující s biologickými systémy; bioaktivní, tj. trvanlivé materiály, které mohou podléhat mezifázovým interakcím s okolními tkáněmi; biodegradabilní, rozpustné nebo resorbovatelné (případně nahraditelné nebo zabudované do tkáně). Na některé keramické materiály se mohou vázat cukry a bílkoviny. Do některých keramických protéz mohou například pronikat krevní cévy a kostní materiál je může časem začít nahrazovat.45-47
Pro svou pevnost, pružnost a biokompatibilitu se pro kloubní a kostní implantáty často používají slitiny titanu. Z podobných důvodů se pro kostní implantáty používají také slitiny chromu a kobaltu a nerezová ocel, i když poněkud méně často.
Tvarově paměťové slitiny mají biomedicínské využití při zákrocích, jako je angioplastika, kdy mohou zabránit opětovnému ucpání cév.48
Nejnovější práce se zaměřují na nanokrystalické titanové prášky pro kostní implantáty. Tyto ultrajemnozrnné materiály využívají biokompatibility titanu, ale jsou přibližně 10krát pevnější než běžné titanové implantáty. Proto je nyní možné používat duté kyčelní implantáty, které se více blíží přirozené kosti.49
Dokonalý materiál pro lékařské aplikace by byl nejen biokompatibilní, ale měl by také podobné fyzikální vlastnosti jako nahrazovaná nebo opravovaná tkáň nebo jiný biologický systém. Například keramické povlaky, které napodobují strukturu a vzhled přírodních zubů potažených kovovými podpěrami, představují primární nástroj pro protetickou náhradu zubů.50
Keramika, ačkoli zahrnuje dobré chemické a korozivzdorné vlastnosti, je notoricky známá svou křehkostí. Výzkumníci proto hledali způsoby, jak kombinovat žádoucí keramiku s jinými materiály a přizpůsobit tak vlastnosti, jako je pevnost a pružnost, požadavkům systému. K optimalizaci výběru materiálů byly zkoumány kompozity, funkčně gradientní materiály a povlaky. Zdá se, že biokompatibilní kovy s keramickým povlakem nabízejí vynikající kompromis mezi pevností a pružností kovů a schopností keramiky začlenit se do biologických systémů.
Mnoho práce bylo věnováno mezifázovým reakcím biologických systémů s hydroxyapatitem, keramikou s chemickou strukturou velmi podobnou tvrdé struktuře kosti. Hydroxyapatit se používá jako povlak na kovové chirurgické implantáty (nejčastěji z titanu a jeho slitin nebo nerezových ocelí) a nedávné studie zkoumaly možnost jeho použití v kompozitní formě, v materiálech, které kombinují polymery s keramikou nebo kombinací kovu a keramiky. Byl proveden rozsáhlý výzkum metod nanášení povlaků a syntézy apatitů in-situ a důsledků pro vlastnosti a mikrostrukturu keramiky.
Keramika v řadě forem a složení se v současné době používá nebo se o ní uvažuje a další jsou ve vývoji. Od objevu stabilních keramických složek SiO2-Na2O-CaO před několika tisíci lety má většina křemičitanové keramiky používané člověkem obsah SiO2 65 % hmot. nebo více. Tato keramika SiO2-Na2O-CaO se častěji nazývá sklo. Přestože jsou tato skla s obsahem 65 % hmotn. oxidu křemičitého mimořádně bioinertní, obsahují jen málo dalších žádoucích vlastností. Jsou slabá a snadno se tříští. První bioaktivní sklo obsahovalo 20-25 % hmot. Na2O a 20-25 % hmot. CaO a pouze 45-55 % hmot. SiO2. Bohužel byl tento nový typ skla stále velmi slabý a křehký. Přidáním P2O5 do matrice SiO2-Na2O-CaO se sklo stalo mimořádně bioaktivním.
Bioaktivní skla a opracovatelná sklokeramika jsou k dispozici pod řadou obchodních názvů. Některé z patentovaných keramik, jako například "Ceravital" a "Bioglass 45S5", jsou natolik bioaktivní, že se během jedné hodiny po implantaci vytvoří HCA vrstva (prekurzor [v]růstu kosti) hluboká téměř 500 nm. Rovněž se tvrdí, že byl pozorován růst měkké tkáně na povrchu "Bioglass 45S5". Hliník a zirkon patří mezi bioinertní keramiku používanou pro protetické pomůcky. Porézní keramika, jako jsou materiály na bázi fosforečnanu vápenatého, se používá k vyplňování kostních defektů. Schopnost řídit pórovitost a rozpustnost některých keramických materiálů nabízí možnost použití jako systémů pro podávání léčiv. Skleněné mikrosféry byly například použity jako systémy pro doručování radioaktivních terapeutických látek.
Výběr materiálu musí také zohledňovat požadavky na tvarování složitých tvarů s přísnými rozměrovými tolerancemi. Zařízení pro použití v těle musí být schopna odolávat korozi v biologickém prostředí a vydržet používání po mnoho let bez nadměrného opotřebení (a bez poškození okolních tkání). Před vložením by se neměly měnit během skladování a musí být sterilizovatelné bez poškození. Materiáloví vědci musí mít na paměti množství vlastností a schopností, když se snaží vyvinout materiály, které budou sloužit ke zlepšení života pacientů.
Závěrem lze říci, že objevování nových anorganických a polymerních biomateriálů a zdokonalování těch tradičních vyvolává v této oblasti nebývalé vzrušení, protože konstruktéři materiálů stále častěji čelí mnoha základním výzvám lékařské vědy. Jak se vyvíjí samotný obor biomateriálů, překvapivé pokroky posledních několika let v genomice a proteomice, v různých vysoce výkonných technikách zpracování buněk, v supramolekulární a permutační chemii a v informačních technologiích a bioinformatice slibují podpořit hledání nových materiálů výkonnými analytickými nástroji a poznatky s bezmeznou energií a propracovaností.
Supramolekulární chemie
Dalším zajímavým novým slibným oborem je supramolekulární chemie, která se zabývá vývojem molekulárních sestav pro biologické aplikace založených na makromolekulárních architekturách, které napodobují systémy nebo mechanismy v nanorozměrech v přírodě (biomimetika). Nové metody syntézy založené na supramolekulární chemii byly použity k vytvoření rozvětvených nebo roubovaných, cyklických, zesíťovaných, hvězdicových a dendritických polymerních struktur. Úplný seznam dendrimerů od společnosti Sigma-Aldrich je uveden v části o nanomateriálech.
Odkazy
Abyste mohli pokračovat ve čtení, přihlaste se nebo vytvořte účet.
Nemáte účet?