8.52373
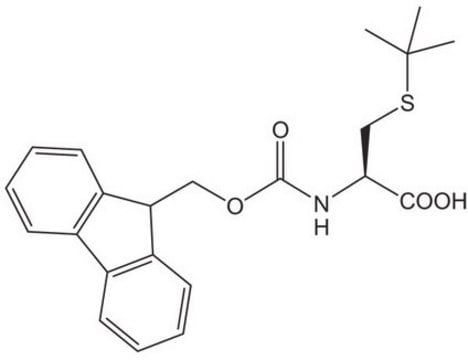
Fmoc-Cys(STmp)-OH
for peptide synthesis, Novabiochem®
Synonym(e):
Fmoc-Cys(STmp)-OH, N-α-Fmoc-S-2,4,6-trimethoxyphenylthio-L-cysteine
About This Item
Empfohlene Produkte
product name
Fmoc-Cys(STmp)-OH, Novabiochem®
Qualitätsniveau
Produktlinie
Novabiochem®
Form
powder
Eignung der Reaktion
reaction type: Fmoc solid-phase peptide synthesis
Hersteller/Markenname
Novabiochem®
Anwendung(en)
peptide synthesis
Funktionelle Gruppe
thiol
Lagertemp.
15-25°C
Verwandte Kategorien
Allgemeine Beschreibung
Zugehörige Protokolle und technische Artikel
Protokolle zur Spaltung und Entschützung bei der Festphasen-Peptidsynthese (SPPS) mit Fmoc-Schutzgruppen
Fmoc-SPPS von Cystein-haltigen Peptiden
Literaturverweise:
[1] T. M. Postma, et al. (2012) Org. Lett., 14, 5468.
[2] T. M. Postma & F. Albericio (2013) Org. Lett., 15, 616.
Anwendung
- Synthese von Insulinanalogen durch Bildung regiospezifischer Disulfidbindungen.
- Ein Review der schrittweisen Einführung von Disulfidbindungen.
- Synthese des humanen insulinähnlichen Peptids 6.
Hinweis zur Analyse
Aussehen der Substanz (visuell): Pulver
Identität (IR): entspricht
Enantiomere Reinheit: ≥ 99,5 % (a/a)
Gehalt (HPLC, Fl. %): ≥ 94,0 % (a/a)
Reinheit (TLC(011A)): ≥ 98 %
Löslichkeit (1 mmol in 2 ml DMF): klar löslich
Ethylacetat (HS-GC): ≤ 0,5 %
Acetat (IC): ≤ 0,05 %
Informationen über die Lösungsmittelsysteme für TLC von Novabiochem® Produkten finden Sie hier.
Rechtliche Hinweise
Lagerklassenschlüssel
11 - Combustible Solids
WGK
WGK 1
Flammpunkt (°F)
Not applicable
Flammpunkt (°C)
Not applicable
Analysenzertifikate (COA)
Suchen Sie nach Analysenzertifikate (COA), indem Sie die Lot-/Chargennummer des Produkts eingeben. Lot- und Chargennummern sind auf dem Produktetikett hinter den Wörtern ‘Lot’ oder ‘Batch’ (Lot oder Charge) zu finden.
Besitzen Sie dieses Produkt bereits?
In der Dokumentenbibliothek finden Sie die Dokumentation zu den Produkten, die Sie kürzlich erworben haben.
Kunden haben sich ebenfalls angesehen
Artikel
Novabiochem® offers orthogonally protected amino acids for peptide synthesis, including cyclic and branched peptides.
Protokolle
Overcome challenges in synthesis and disulfide bond formation with protocols for Fmoc solid-phase peptide synthesis of peptides with cysteine and methionine.
Unser Team von Wissenschaftlern verfügt über Erfahrung in allen Forschungsbereichen einschließlich Life Science, Materialwissenschaften, chemischer Synthese, Chromatographie, Analytik und vielen mehr..
Setzen Sie sich mit dem technischen Dienst in Verbindung.