Wybierz wielkość
393,00 zł
707,00 zł
1310,00 zł
3970,00 zł
6980,00 zł
393,00 zł
Informacje o tej pozycji
Przejdź do
Nazwa produktu
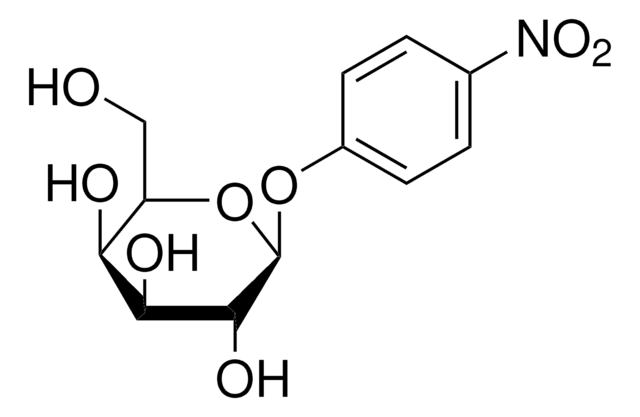
4-Nitrophenyl β-D-galactopyranoside, ≥98% (enzymatic)
InChI key
IFBHRQDFSNCLOZ-YBXAARCKSA-N
InChI
1S/C12H15NO8/c14-5-8-9(15)10(16)11(17)12(21-8)20-7-3-1-6(2-4-7)13(18)19/h1-4,8-12,14-17H,5H2/t8-,9+,10+,11-,12-/m1/s1
SMILES string
OC[C@H]1O[C@@H](Oc2ccc(cc2)[N+]([O-])=O)[C@H](O)[C@@H](O)[C@H]1O
assay
≥98% (TLC), ≥98% (enzymatic)
form
powder
solubility
water: 10 mg/mL, clear, colorless to very faintly green
storage temp.
−20°C
Quality Level
1 of 4
Ta pozycja | |||
|---|---|---|---|
| assay ≥98% (TLC), ≥98% (enzymatic) | assay ≥99% (TLC) | assay ≥98% (TLC) | assay ≥98% (TLC) |
| solubility water: 10 mg/mL, clear, colorless to very faintly green | solubility methanol: 100 mg/mL, clear to very slightly hazy | solubility water: 50 mg/mL, clear to very slightly hazy | solubility DMF: 25 mg/mL, clear, colorless to faintly yellow |
| Quality Level 300 | Quality Level 200 | Quality Level 300 | Quality Level 200 |
| form powder | form powder | form powder | form powder |
| storage temp. −20°C | storage temp. −20°C | storage temp. −20°C | storage temp. −20°C |
Application
- as a substrate to assess the activity of glycosaminoglycan (GAG)-degrading enzymes[1]
- as a substrate to study the kinetic properties of recombinant Leuconostoc mesenteroides glycosidase (BgLm1) and determine β-glucosidase activity
- to prepare substrate solution in a modified universal buffer
Klasa składowania
11 - Combustible Solids
wgk
WGK 3
flash_point_f
Not applicable
flash_point_c
Not applicable
ppe
Eyeshields, Gloves, type N95 (US)
Wybierz jedną z najnowszych wersji:
Masz już ten produkt?
Dokumenty związane z niedawno zakupionymi produktami zostały zamieszczone w Bibliotece dokumentów.
Active Filters
Nasz zespół naukowców ma doświadczenie we wszystkich obszarach badań, w tym w naukach przyrodniczych, materiałoznawstwie, syntezie chemicznej, chromatografii, analityce i wielu innych dziedzinach.
Skontaktuj się z zespołem ds. pomocy technicznej