A6185
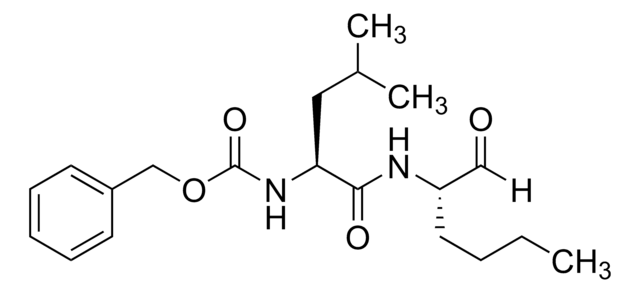
Calpain Inhibitor I
≥97% (TLC), powder
Sinónimos:
ALLN, Ac-LLnL-CHO, MG-101, N-Acetyl-L-leucyl-L-leucyl-L-norleucinal, N-Acetyl-Leu-Leu-Norleu-al
Seleccione un Tamaño
127,00 €
Seleccione un Tamaño
About This Item
127,00 €
Productos recomendados
origen biológico
synthetic (organic)
Nivel de calidad
Ensayo
≥97% (TLC)
Formulario
powder
color
white
solubilidad
DMSO: soluble
ethanol: soluble
temp. de almacenamiento
−20°C
cadena SMILES
[H]C(=O)[C@H](CCCC)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(C)C)NC(C)=O
InChI
1S/C20H37N3O4/c1-7-8-9-16(12-24)22-19(26)18(11-14(4)5)23-20(27)17(10-13(2)3)21-15(6)25/h12-14,16-18H,7-11H2,1-6H3,(H,21,25)(H,22,26)(H,23,27)/t16-,17-,18-/m0/s1
Clave InChI
FMYKJLXRRQTBOR-BZSNNMDCSA-N
Información sobre el gen
human ... CAPN1(823) , CTSB(1508) , PSMA1(5682)
¿Está buscando productos similares? Visita Guía de comparación de productos
Aplicación
Acciones bioquímicas o fisiológicas
Código de clase de almacenamiento
11 - Combustible Solids
Clase de riesgo para el agua (WGK)
WGK 3
Punto de inflamabilidad (°F)
Not applicable
Punto de inflamabilidad (°C)
Not applicable
Equipo de protección personal
Eyeshields, Gloves, type N95 (US)
Elija entre una de las versiones más recientes:
¿Ya tiene este producto?
Encuentre la documentación para los productos que ha comprado recientemente en la Biblioteca de documentos.
Los clientes también vieron
Artículos
DISCOVER Bioactive Small Molecules for Nitric Oxide & Cell Stress Research
Filtros activos
Nuestro equipo de científicos tiene experiencia en todas las áreas de investigación: Ciencias de la vida, Ciencia de los materiales, Síntesis química, Cromatografía, Analítica y muchas otras.
Póngase en contacto con el Servicio técnico