Wdrożenie i skalowanie jednoprzebiegowej filtracji z przepływem stycznym

Rysunek 1.Porównanie tradycyjnego TFF (1A) z jednoprzebiegowym TFF (1B). Konwersja wzrasta wraz z czasem przebywania w konfiguracji szeregowego kanału zasilającego (1C) w porównaniu z konfiguracją równoległą (1D) ze względu na wyższe prędkości przepływu i transfer masy. Permeat nie jest pokazany w 1D.
Filtracja z przepływem stycznym (TFF) jest stosowana w dalszym przetwarzaniu w celu zagęszczenia produktu i wymiany buforów. Zwykle działa w trybie wsadowym i wymaga kilku przejść przez zespół filtra TFF (Rysunek 1A).
Alternatywą jest jednoprzebiegowa filtracja z przepływem stycznym (SPTFF). W SPTFF wsad jest zagęszczany już po jednym przejściu przez filtr, eliminując potrzebę recyklingu retentatu (Rysunek 1B). Podstawową zasadą leżącą u podstaw SPTFF jest to, że wydłużony czas przebywania w kanale zasilającym skutkuje zwiększoną konwersją. Zwiększony czas przebywania można osiągnąć poprzez zmniejszenie natężenia przepływu lub zwiększenie długości ścieżki w konfiguracji szeregowej (Rysunek 1C). Konfiguracja kaset lub kapsułek TFF w szeregu może poprawić konwersję. Szeregowe filtry TFF mają wyższy transfer masy w porównaniu do konfiguracji równoległych przy równoważnych czasach przebywania (Rysunek 1D). Dowiedz się więcej o różnych typach TFF w naszym artykule technicznym.
Przegląd sekcji:
Wdrożenie jednoprzebiegowej filtracji z przepływem stycznym
Wdrożenie SPTFF przy użyciu kapsuł Pellicon® w procesie wymaga trzech podstawowych kroków:
- Ustawienie zespołu filtrującego poprzez szeregową instalację kapsuł Pellicon®
- Ustalenie warunków pracy poprzez (a) określenie optymalnego ciśnienia retentatu przy wyjściowym testowym natężeniu przepływu oraz (b) przeprowadzenie skoków strumienia zasilającego w celu uzyskania docelowej konwersji
- Potwierdzenie stabilności poprzez przeprowadzenie pojedynczego testu z użyciem kapsuł Pellicon®.Potwierdzenie stabilności poprzez przeprowadzenie jednoprzebiegowej symulacji procesu przy docelowej konwersji
Instalacja kapsułek Pellicon®
Kapsułki Pellicon® są najpierw konfigurowane z docelową liczbą sekcji (kapsułki instalowane szeregowo), zazwyczaj trzy sekcje, gdzie każda sekcja musi mieć taką samą powierzchnię dla pełnej eksploracji okna procesu. Zaleca się, aby system był skonfigurowany w trybie całkowitego recyklingu (retentat i permeaty powracają do zbiornika zasilającego), aby zminimalizować objętość zasilania wymaganą podczas wydłużonego czasu pracy podczas ustawiania warunków pracy. Retentat z pierwszej kapsuły w szeregu zostanie podłączony bezpośrednio do zasilania drugiej kapsuły, a następnie naprzemiennie dla każdej kolejnej kapsuły w szeregu. Ta konfiguracja utworzy wydłużony kanał zasilający.
Ustalanie warunków pracy
Aby znaleźć optymalne ciśnienie retentatu, strumień zasilający jest zwykle ustawiony na 1 LMM (litry/min na m2), a konwersja jest monitorowana począwszy od najniższego ciśnienia retentatu (np. zawór retentatu jest całkowicie otwarty).zawór retentatu jest całkowicie otwarty), które jest następnie stopniowo zwiększane, aż do osiągnięcia maksymalnej pożądanej konwersji, system staje się trudny do kontrolowania lub niestabilny, lub strumień przestaje rosnąć. Punkt końcowy zależy od zastosowania. Przed ustawieniem ostatecznych warunków ciśnienia roboczego ważne jest, aby zapewnić wystarczającą ilość czasu na pełne rozwinięcie polaryzacji i ustabilizowanie strumienia - zakres czasu stabilizacji wynosi zwykle 1-30 minut, w zależności od stężenia białka i innych warunków procesu i jest wskazywany przez stabilne odczyty ciśnienia.
Ciśnienie retentatu jest zwiększane w małych krokach (np. 1-2 psi), aż do zaobserwowania przegięcia krzywej (Rysunek 2). Jeśli zawór retentatu jest całkowicie zamknięty lub TMP rozciąga się zbyt daleko do obszaru plateau, membrana ulegnie zanieczyszczeniu. W przykładzie pokazanym na Rysunku 2, idealna wartość zadana ciśnienia wynosi około 2 psi dla 0.1 m2 Pellicon® Capsule i 5 psi dla kasety 0,11 m2 Pellicon® 3. Przy tej kombinacji wartości zadanych istnieje równoważna konwersja między formatami urządzeń i tolerancja dla niewielkich zmian ciśnienia retentatu.

Rysunek 2.Przykład optymalnych krzywych ciśnienia dla wsadu 1 g/L przy 1 LMM.
Po znalezieniu optymalnego ciśnienia retentatu, musi ono być utrzymywane na stałym poziomie przez cały czas trwania eksperymentów, ale może zostać potwierdzone po ustaleniu pożądanego natężenia przepływu paszy, aby zapewnić solidny proces. Należy pamiętać, że bardziej rozcieńczone pasze zazwyczaj wymagają niższego ciśnienia retentatu dla danej konwersji.
Przepływy strumienia paszy są następnie przeprowadzane przy użyciu ustalonego optymalnego ciśnienia retentatu i rozpoczynając od 1 LMM (w zależności od pożądanej konwersji, operator może zdecydować się na pracę przy wyższych prędkościach przepływu paszy, jeśli konwersja jest zbyt wysoka przy 1 LMM). W przypadku serii 3-sekcyjnej uruchamiany jest cały zespół, a poszczególne przepływy permeatu są rejestrowane w celu obliczenia konwersji dla każdej sekcji: 1 sekcja, 2 sekcje (sekcje 1 i 2) i 3 sekcje (sekcje od 1 do 3), przy różnych natężeniach przepływu zasilania. Natężenie przepływu zasilania dla procesu jest określane na podstawie wymaganej konwersji i liczby sekcji. Będzie się ono różnić w zależności od procesu, w zależności od pożądanego rezultatu. Dane te są wykreślane w celu ujawnienia optymalnego natężenia przepływu zasilania dla pracy przy pożądanej konwersji.
Potwierdzenie stabilności
Używając wybranych warunków pracy i liczby sekcji, stabilność jest potwierdzana poprzez przeprowadzenie symulacji procesu jednoprzebiegowego. W tym momencie zaleca się rozpoczęcie od świeżego materiału wsadowego.
Po wyrównaniu, wsad jest pompowany przez zespół SPTFF kapsułki w określonych optymalnych warunkach, aż profil konwersji i ciśnienia stanie się stały. Można to zrobić w trybie jednoprzebiegowym lub w trybie całkowitego recyklingu, jeśli objętość wsadu jest niewystarczająca. Czas stabilizacji zależy od warunków zasilania i wybranego natężenia przepływu. Należy pamiętać, że początkowe rozcieńczenie może być konieczne, jeśli praca w stanie ustalonym zostanie osiągnięta w trybie jednoprzebiegowym. Proces ten powinien trwać od 1 do 30 minut, ale może wykraczać poza ten zakres. Po ustabilizowaniu retentat jest zbierany w trybie jednoprzebiegowym, a konwersja jest monitorowana przez docelowy czas pracy.
Studium przypadku 1: Pellicon® Capsule vs Pellicon® 3 Cassette na bydlęcej gamma globulinie (BgG)
Przeprowadzono badania w skali laboratoryjnej w celu oceny skuteczności Pellicon® Capsules 0.1 m2 do stosowania w SPTFF w porównaniu z Pellicon® 3 kasetami 0,11 m2. Roztwór bydlęcej gamma globuliny (BgG) został użyty jako modelowy wsad przeciwciał. Kapsułki i kasety zostały uruchomione obok siebie w trybie SPTFF. W każdym przypadku określono optymalne ciśnienie retentatu przed uruchomieniem skoków strumienia paszy i przeprowadzono końcowe badanie stabilności konwersji.
Określenia optymalnego ciśnienia retentatu przeprowadzono zarówno na urządzeniu Pellicon® Capsule, jak i na urządzeniu Pellicon® 3 kasetowym SPTFF dla wsadów 1 g/L i 25 g/L BgG przy użyciu metodologii opisanej powyżej. Idealne ustawienie ciśnienia retentatu jest niższe dla niższego stężenia wsadu. Jest to ważna uwaga, ponieważ warunki zasilania mają bezpośredni wpływ na wydajność pracy SPTFF i powinny być sprawdzane w przypadku zmiany składu zasilania. Oprócz zmiany związanej z paszą, z danych przedstawionych na Rysunku 3 wynika, że między kapsułką a kasetą występuje inne ciśnienie retentatu. Jednak, jak opisano w Skalowalność kapsułek i kaset SPTFF (poniżej), utrzymanie spadku ciśnienia i strumienia zasilania pozwoli na zachowanie spójności konwersji między oboma formatami filtrów.
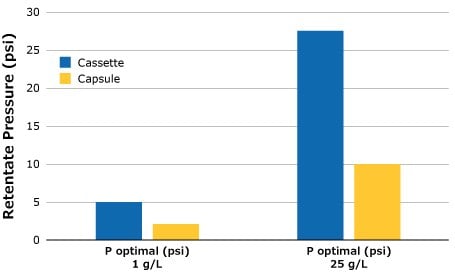
Rysunek 3.Optymalne ciśnienie retentatu dla konfiguracji SPTFF, 3 w szeregu.
Przepływy strumienia zasilającego wykonano dla roztworu zasilającego 25 g/L przy ustalonych optymalnych ciśnieniach retentatu, zaczynając od strumienia zasilającego 1 LMM i zmniejszając go w pożądanych odstępach czasu do 0,14 LMM. Krzywe strumienia zasilającego dla roztworu zasilającego 25 g/L porównano na Rysunku 4. Chociaż najwyższa konwersja została osiągnięta przy 0,14 LMM przez trzecią kapsułkę dla kapsułek 0,1 m2, wykreślone punkty danych dla obu formatów kaset i kapsułek przedstawiają porównywalną wydajność w trakcie skoków strumienia zasilającego.
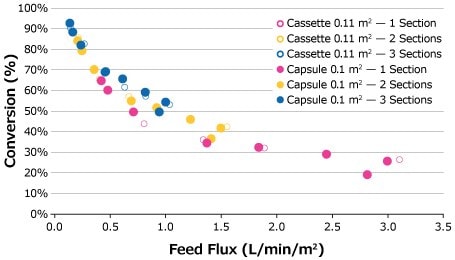
Rysunek 4.Wzrost strumienia zasilającego dla roztworu zasilającego 25 g/L BgG.
Po ocenie strumienia zasilającego przeprowadzono badanie stabilności w celu wykazania stabilności procesu i ogólnej konwersji dla każdego systemu. Dla tego przebiegu wybrano natężenie przepływu, które dało najwyższą konwersję (0,14 LMM), aby zademonstrować solidność przy najtrudniejszej wartości zadanej. Jak widać na krzywych strumienia zasilającego na Rysunku 5, przewidywano, że kapsułka wytworzy nieco wyższą ogólną konwersję niż kaseta. Zostało to potwierdzone w badaniu stabilności (Rysunek 5).
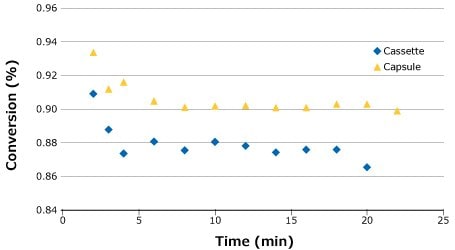
Rysunek 5.Stabilność procesu dla SPTFF z 25 g/L BgG przy 0,14 LMM.
Na podstawie wyników eksperymentów i ustaleń można oczekiwać podobnej wydajności przy przełączaniu między kapsułką Pellicon® a kasetą Pellicon® 3 do operacji SPTFF. Warunki zasilania odgrywają znaczącą rolę, zwłaszcza przy niskich stężeniach zasilania; dlatego ważne jest, aby sprawdzić optymalne ciśnienie retentatu, szczególnie w przypadku przełączania między formatami kaset i kapsułek.
Skalowalność kapsułek i kaset SPTFF
Skalowanie do lub z 0.1 m2 Pellicon® Capsule do innego rozmiaru kapsułki lub kasety Pellicon® Cassette można łatwo osiągnąć, utrzymując strumień podawania (ustawiany przez pompę) i spadek ciśnienia w kanale podawania (ustawiany przez zawór retentatu przy danym strumieniu podawania) na tym samym poziomie pomiędzy skalowaniami. Spowoduje to uzyskanie nowej optymalnej wartości zadanej ciśnienia retentatu. Alternatywnie, optymalne ciśnienie retentatu może zostać ponownie ustalone od zera w nowej wadze.
Dla łatwości użycia zalecana jest pierwsza metoda, w której ten sam spadek ciśnienia w kanale zasilającym jest utrzymywany w różnych wagach. Utrzymując spadek ciśnienia i strumień zasilania, konwersja pozostanie spójna. Kapsuła będzie skalowana w ramach własnej rodziny lub do kaset bez konieczności ponownego ustalania optymalnego ciśnienia retentatu.
Studium przypadku 2: Badanie skalowania kapsułek Pellicon® na m Ab od 0.1 m2 do 0,5 m2 Badanie skalowania w dół
Badanie zmniejszania skali
Celem eksperymentu było określenie optymalnych warunków pracy dla operacji w skali pilotażowej. Badania skalowania od 0,1 m2 do 0,5 m2 kapsułki Pellicon® przeprowadzono przy użyciu oczyszczonego płynu zbiorczego z własnej hodowli komórek CHO wyrażających mAb przy początkowym stężeniu mAb około 1,3 g/L. W dniu zbioru, 2 litry klarowanej paszy zostały uruchomione w skali 0,1 m2 w 3-sekcyjnym (3 × 0,1 m2) systemie kapsułkowym SPTFF.
Zastosowując metodologię opisaną w Studium przypadku 1, ustalono optymalne ciśnienie retentatu dla roztworu paszy mAb przy strumieniu paszy 1 LMM. Wartość zadana ciśnienia retentatu została ustalona na 4 psi i była utrzymywana na stałym poziomie podczas kolejnych skoków strumienia podawania.
Począwszy od około 1 LMM i kontynuując w malejących odstępach czasu, przeprowadzono serię skoków strumienia podawania. Celem było określenie warunków dla 90% konwersji (współczynnik stężenia 10x). Dane dotyczące mętności i zmierzonego stężenia zostały wykreślone wraz z przewidywanymi krzywymi stężenia. Wykres na Rysunku 6 przedstawia wyniki serii eksperymentów w funkcji stężenia, przewidywane matematycznie przez uzyskaną konwersję i potwierdzone pomiarami PrA HPLC.
Zmierzone wartości oznaczone jako "×" pokazują zgodność między przewidywanymi i rzeczywistymi danymi pomiarowymi. Dla docelowej konwersji 90% (stężenie końcowe ~13 g/L), wymagany strumień zasilający z 3 kapsułkami w szeregu został określony poprzez prostą identyfikację wynikowej wartości osi x przy stężeniu docelowym. W związku z tym do przetworzenia pełnej objętości około 70 l wybrano strumień podawania 0,84 LMM.

Rysunek 6.Wyniki 3-sekcyjnego badania skalowania SPTFF w kapsułce 0,1 m2.
Badanie skalowania
W przypadku pilotażu trzy kapsułki Pellicon® o średnicy 0,5 m2 zostały ułożone szeregowo, przepłukane i zrównoważone buforem przed przetwarzaniem. Pompa zasilająca została ustawiona na 0,84 LMM, aby dopasować optymalny strumień zasilający określony na podstawie systemu zmniejszania skali. W tym eksperymencie retentat nie został zawrócony do zbiornika zasilającego na okres stabilizacji: zarówno retentat, jak i permeat były gromadzone w zbiornikach na wadze i mierzone w regularnych odstępach czasu podczas całego cyklu w celu monitorowania stabilności procesu.
Ciśnienie retentatu zostało początkowo ustawione na 4 psi i ręcznie zwiększone do 13 psi, aby dopasować spadek ciśnienia w kanale zasilającym z badania scale-down i osiągnąć pożądaną konwersję. Podobnie jak w przypadku różnic ciśnienia zaobserwowanych między kasetą Pellicon® Capsule 0,1 m2 a kasetą Pellicon® 3 0.11 m2, widoczne są różnice ciśnień między kapsułkami 0,1 m2 i 0,5 m2 (Rysunek 7). Tylko w przypadku kapsułki 0,1 m2 do osiągnięcia pożądanej konwersji potrzebne jest niższe ciśnienie. Jednak porównując spadek ciśnienia między różnymi rozmiarami kapsułek, wartości są takie same.

Rysunek 7.Spadek ciśnienia w kanale zasilającym dla kapsułek 0,1 i 0,5 m2 przy 0,84 LMM.
Po osiągnięciu stabilności proces przebiegał nieprzerwanie przez około 1 godzinę przy stałym stężeniu i konwersji. Początkowe niskie odczyty wskazują na okres potrzebny do wyparcia buforu i utworzenia warstwy żelu na powierzchni membrany. Zmierzone stężenie połączonej próbki, pokazane na Rysunku 8 (otwarty okrąg), potwierdziło przewidywaną wydajność partii. Zarówno konwersja, jak i przewidywane stężenie były monitorowane i śledzone przez cały czas trwania badania i są wykreślone na Rysunku 8 wraz ze zmierzoną próbką puli.

Rysunek 8.Stabilność procesu w skali pilotażowej.
Odkryj naszą szeroką gamę filtrów Pellicon®, dostosowanych do Twoich unikalnych wymagań procesowych. Odwiedź naszą stronę produktu, aby dowiedzieć się więcej.
Zaloguj się lub utwórz konto, aby kontynuować.
Nie masz konta użytkownika?