Wodorki metali do zastosowań w akumulatorach NiMH
Dhanesh Chandra*, Wen-Ming Chien, Anjali Talekar
University of Nevada, Reno, College of Engineering Reno, NV 89557
Material Matters Volume 6 Article 2
Wprowadzenie
Ładowalne baterie półprzewodnikowe stają się coraz ważniejsze ze względu na ich szerokie zastosowanie w komputerach, przenośnej elektronice i pojazdach. Partnerstwo dla Nowej Generacji Pojazdów (PNGV), współpraca między rządem USA a przemysłem motoryzacyjnym, została zainicjowana w 1996 roku w celu promowania rozwoju hybrydowych pojazdów elektrycznych (HEV) o znacznie zwiększonej oszczędności paliwa. Jak pokazano na Rysunku 1, akumulatory wodorkowo-metalowe i litowo-jonowe mają wysoką gęstość energii i są najbardziej obiecującymi klasami nowoczesnych akumulatorów.1 Akumulatory litowo-jonowe są bardzo atrakcyjne dla nowoczesnych przenośnych urządzeń elektronicznych, a akumulatory niklowo-wodorkowe (NiMH) są istotnym elementem nowoczesnych samochodów hybrydowych. W oparciu o ceny z 1996 r. szacowany koszt tych materiałów wynosił 1 USD/gH wyprodukowanego (Tabela 2).2-4 Chociaż zarówno akumulatory NiMH, jak i litowo-jonowe są równie ważne dla różnych zastosowań, żywotność od kołyski do bramy (ctg) Ectg/kg jest nieco wyższa niż w przypadku innych akumulatorów (Rysunek 2).5 Niniejszy artykuł stanowi podsumowanie związków międzymetalicznych ziem rzadkich oraz ich struktur, właściwości, technologii i zastosowań, w szczególności w odniesieniu do baterii wielokrotnego ładowania.

Rysunek 1.Porównanie objętościowej i grawimetrycznej gęstości energii ważnych akumulatorów NiMH, kwasowo-ołowiowych (PbA), Ni-Cd, Na/S i litowo-jonowych.

Rysunek 2.Średnia żywotność od kołyski do bramki (Ectg) na watogodzinę z jednym odchyleniem standardowym dla akumulatorów NiMH, kwasowo-ołowiowych (PbA), Ni-Cd, Na/S i litowo-jonowych.
Wodorki metali były szeroko badane na przestrzeni lat, a znaczące zainteresowanie nimi rozwinęło się w latach 60-tych XX wieku. Większość badań prowadzonych przed 1960 rokiem została opisana w książce Mueller, Blackledge i Libowitz zatytułowanej Metal Hydrides6. Nowsze prace zostały omówione w kilku dobrych recenzjach autorstwa Schlapbacha,7 Sandrocka,8 Yvon,9 Fukai,10 Walker,11 i inni. Ogólnie rzecz biorąc, metastabilne stopy binarne lub stopy wyższego rzędu, które odwracalnie absorbują/desorbują wodór, są preferowane w zastosowaniach ze względu na ich metastabilny charakter: czyste pierwiastki mają tendencję do tworzenia porównywalnie stabilnych wodorków. Stopy prekursorowe stosowane do produkcji wodorków są ogólnie podzielone na sześć kategorii w oparciu o układy składników A-B. Przykładami prostych układów binarnych, bez podstawień, są:
- AB (HfNi, FeTi)
- AB2 (Mn2Zn, TiFe2)
- A2B (Hf2Fe, Mg2Ni)
- A2B7 (Pr2Ni7, Ce2Co7)
- AB3 (NdCo3, GdFe3)
- AB5 (LaNi5, CeNi5)
Typ AB5, LaNi5H6.7 wodorki mają wysoką wydajność objętościową (~130 kgH2/m3), niską wydajność grawimetryczną (~2% wag. H2) i działają w pobliżu temperatury pokojowej. Aby pomóc zrozumieć rozwój tych wodorków, niepodstawione wodorki A-B zostaną omówione najpierw pod względem pojemności wodorowej. Poniższa dyskusja skupi się na wpływie podstawienia jednego składnika w układach A-B. Wreszcie, artykuł ten będzie dotyczył bardziej praktycznych wodorków, z których niektóre są komercjalizowane.
Termodynamika i struktury krystaliczne materiałów akumulatorowych NiMH
Termodynamika
Wodorki metali zostały po raz pierwszy użyte do przechowywania wodoru w stanie stałym. Stopy wykorzystywane do produkcji wodorków metali w akumulatorach NiMH są głównie typu AB5- i AB2; inne struktury stopów mogą być rozważane, ale nie będą tutaj omawiane. Tabela 1 opisuje niektóre ważne właściwości tych modelowych typów struktur.

Tabela 1.Związki międzymetaliczne i ich właściwości magazynowania wodoru.
Najważniejsze właściwości dla zastosowań w akumulatorach to pojemność wodorowa, ciśnienie izotermiczne, histereza, rozszerzalność objętościowa/kurczliwość, entalpie oraz temperatury uwodnienia/odwodnienia. Dodatkowe właściwości są ważne dla praktycznych zastosowań. Obejmują one aktywację stopów, dekrepitację, kinetykę, przenoszenie ciepła, zanieczyszczenia gazowe w H2, zdolność cykliczną, bezpieczeństwo, metalurgiczne wytwarzanie stopów na dużą skalę, koszty i recykling.
Właściwości termodynamiczne uzyskuje się poprzez pomiar izoterm objętościowych przy użyciu aparatu Sievertsa; są one obecnie dostępne w handlu. Zazwyczaj uzyskujemy izotermy w stałej temperaturze, uzyskując stosunek H/M i % wagowy H. Gdy stop zaczyna absorbować wodór, obserwuje się obszar roztworu stałego, zwany fazą α. W miarę pochłaniania większej ilości wodoru następuje przemiana fazowa α→β, dając fazę wodorkową w obszarze plateau. Schemat tego procesu pokazano na Rysunku 3; osie x i y reprezentują odpowiednio stosunek wodoru do metalu i ciśnienie. Następnie mierzymy wiele izoterm w różnych temperaturach i uzyskujemy ciśnienia w połowie plateau. Ogólnie obserwuje się histerezę w izotermach między desorpcją/absorpcją. Wykreślenie zależności ln P od 1/T(K) daje wykres van′t Hoffa, a nachylenie linii van′t Hoffa daje ΔH/R. Entalpia tworzenia jest dana przez (-ΔH/R). Pożądane właściwości wodorków są szacowane poprzez utworzenie okna działania, f(p,T). Wykresy van′t Hoffa dla wielu ważnych wodorków pokazano na rysunku 4; zostaną one omówione później w kolejnych sekcjach. Przejście fazowe α→β dla materiałów AB5 opisują poniższe równania:

Tutaj M = metal lub stop (np. LaNi5), który najpierw tworzy fazę roztworu stałego z wodorem, MHy, oznaczoną jako faza α. Następnie ta faza α tworzy wodorek, MHx. W przypadku LaNi5 (nr prod. 685933) najpierw tworzy się faza LaNi5-H, a następnie faza LaNi5H7 . Istnieje tylko obszar roztworu stałego powyżej pewnej temperatury (Tcritical). Najważniejsze wodorki metali obejmują kilka materiałów ziem rzadkich, które są wymienione w Tabeli 1.3, 4
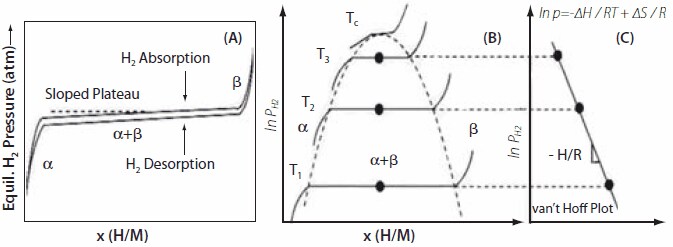
Rysunek 3.(A) Izoterma pokazująca nachylone plateau dla izoterm absorpcji i desorpcji wodoru. Pokazano również histerezę między izotermami absorpcji i desorpcji. (B) Pokazano wpływ temperatury na ciśnienie plateau izotermy i obszary przejść fazowych z α → α + β → β. (C) Wykres van't Hoffa uzyskany z izoterm otrzymanych w różnych temperaturach; którego nachylenie daje entalpię hydratacji.

Rysunek 4.Zestawienie wykresów van't Hoffa wybranych pierwiastkowych, klasycznych i złożonych wodorków. Obszar w ramce reprezentuje pożądany zakres temperatury i ciśnienia dla zastosowań samochodowych.
Jak zostanie omówione później, istnieje wiele podstawionych związków, które wpływają na właściwości termodynamiczne. Niektóre proste przykłady efektów cyklicznych z naszej pracy nad podstawionym LaNi5 pokazują znaczną dysproporcjonację po 10 000 cykli (~ 1 h każdy) sugerując utratę właściwości hydratacyjnych (Rysunek 5). Proste zastąpienie Ni niewielkimi ilościami Sn znacznie poprawiło żywotność; nawet po 10 000 cykli nie ma znaczącej utraty pojemności wodorowej w LaNi4.8Sn0.2 (Rysunek 6). Dalsze szczegóły dotyczące cykli termicznych i starzenia podstawionych stopów LaNi5 można znaleźć w Lambert et al.,15 Chandra et al.,16 i Percheron-Guegan et al.17 Wiedza na temat długoterminowego cyklicznego i termicznego starzenia się wodorków jest niezbędna do oceny wydajności magazynowania wodoru przez pewien okres czasu. Tak więc, właściwa substytucja A lub B w AB5 lub AB2 może poprawić żywotność cyklu, właściwości odporności na korozję, histerezę i właściwości elektrochemiczne. Optymalna stechiometria stopów akumulatorowych zostanie omówiona w kolejnych sekcjach.

Rysunek 5.Izoterma LaNi5.2 wykonana w temperaturze 25 °C po wewnętrznym cyklu P-T dla 10 (aktywacja), 1500 i 10 000 razy, pokazująca poważną degradację tego wodorku.15
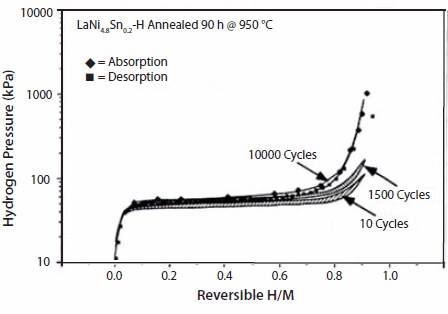
Rysunek 6.Izotermy LaNi0.8Sn0.2 wykonane w temperaturze 25 °C, przed i po cyklu P-T dla 1500 i 10 000 razy, pokazujące praktycznie brak utraty pojemności wodorowej w przypadku LaNi0.8Sn0.2.15
Struktury krystaliczne materiałów akumulatorowych
Ważnymi właściwościami akumulatorów MH są trwałość/cykl życia, pojemność wodorowa oraz wydajność ładowania/rozładowania. Z tego punktu widzenia, wodorki metali ziem rzadkich AB5 i AB2 są najbardziej pożądane do długotrwałego stosowania w pojazdach hybrydowych typu plug-in (PHEV) i pojazdach elektrycznych (EV). Są one określane jako akumulatory NiMH i działają w temperaturze otoczenia. Na przykład Toyota™ Prius (modele II-V) wykorzystuje szczelne akumulatory NiMH, których żywotność szacuje się na 150 000 mil w oparciu o testy laboratoryjne producenta.19 Wraz z dalszym rozwojem żywotności cyklu i gęstości energii akumulatorów NiMH, nadchodzące pojazdy elektryczne mogą wykorzystywać te niezawodne akumulatory o wysokiej gęstości energii. Tego typu wodorki są obecnie nazywane "klasycznymi wodorkami", ale mają niezwykłe właściwości akumulatorów, które uzyskuje się poprzez mikrostopowanie zarówno komponentów A, jak i B, zwiększając elektrochemiczną i cykliczną żywotność akumulatorów.
Struktura krystaliczna materiałów wodorkowych AB5 i AB2
Struktury krystaliczne związków AB5 i AB2 są wymienione w Tabeli 2. Związki AB5 są liniowymi związkami międzymetalicznymi. AB2 są związkami międzymetalicznymi lub pośrednimi (o małym zakresie jednorodności składu) i mogą nie mieć dokładnego składu stechiometrycznego 1:2.
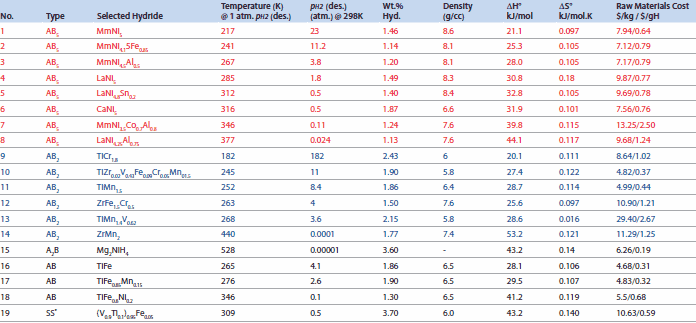
Tabela 2.Wybrane klasyczne wodorki z ich pojemnościami wodorowymi i ciśnieniami plateau (podstawa cen: połowa 1996 r.).3, 4, 8
Struktura AB5 związków
Wiele akumulatorów NiMH jest wykonanych z materiałów o strukturze typu AB5. Głównymi stopami bazowymi są LaNi5 i MmNi5 (stop mischmetal-nikiel, Nr produktu. 685976), a składniki A i B są niezmiennie zastępowane w tych materiałach w celu poprawy właściwości. Modelowy związek, LaNi5, ma heksagonalną strukturę krystaliczną, Strukturbericht D2d (CaCu5-type, P6/mmm, a = 5.0228 Å i c = 3.9826 Å). W strukturze LaNi5 występuje jedno miejsce dla La (miejsce 1a) i dwa różne miejsca dla Ni. Pierwsze miejsce Ni (miejsce 2c) jest otoczone atomami La, a drugie miejsce Ni (miejsce 3g) znajduje się w środkowej warstwie struktury heksagonalnej z samymi atomami Ni. W wielu przypadkach występuje nadmiar Ni (np, LaNi5.2), co zmienia stosunek c/a.20 Struktury zarówno międzymetalicznego LaNi5 jak i wodorku pokazano na Rysunku 7.20-22
.gif)
Rysunek 7.Struktura krystaliczna LaNi5 20, 21 i LaNi5H7.22
Wodorkiem jest LaNi5H7, który jest ogólnie uporządkowany i jest związkiem liniowym. Latriuge opisał strukturę jako heksagonalną podwójną komórkę z grupą przestrzenną P63mc, a = 5,409 Å i c = 8,6 Å.21, 22 Joubert i in...,23 Thompson, Reilly i Hasting,24 i wiele innych grup również zgłosiło tę strukturę.
Praktyczne materiały akumulatorowe oparte są na modelu AB5 . W jednym z optymalnych komercyjnych stopów, miejsce A LaNi5 jest podstawione miszmetalem (Mm), który jest mieszaniną wielu pierwiastków o liczbie atomowej od 51 do 71. Strona B jest zastąpiona przez Co-Al-Mn. Producenci baterii mają swoje własne odmiany podstawień, które są zastrzeżone, ale niektóre obiecujące stopy są wymienione w Tabeli 2 (numery od 1 do 8). Stop MmNi3.5Co0.7Al0.8 (pokazany na Rysunku 4 i Tabeli 2) wydaje się być odpowiedni dla właściwości baterii i ma najwyższy koszt surowców znormalizowany do pojemności odwracalnej. Ze względu na koszty i inne względy, Co nie jest zbyt pożądany, ale jest stopowany w niewielkich ilościach w celu zapewnienia odporności na korozję.
Struktura związków AB2 Compounds
Materiały typu AB2 są generalnie strukturami fazowymi Lavesa (Strukturbericht C14 i C15). Jest to kolejna klasa akumulatorów NiMH; niektóre ważne materiały są wymienione w Tabeli 2 (nr 8 do 14). Materiały te również ładują się/rozładowują w temperaturach zbliżonych do temperatury otoczenia, podobnie jak wodorki AB5 . Materiały C14 mogą mieć strukturę sześcienną, ortogombową lub heksagonalną. Rysunek 8 pokazuje dwa typy wspólnych struktur dla faz C14 i C15. Ważnym przykładem C14 jest ZrMn2, który ma strukturę heksagonalną z Z = 4 (ZrMn2/jednostka formuły) w komórce elementarnej i jest używany do separacji gazów. Struktura C15 AB2 ma Z = 8/jednostkę formuły w komórce elementarnej, jak widać w materiałach typu ZrV2; Yvon poinformował, że atomy H zajmują A2B2 tetraedryczne szczeliny.27 Przykłady związków AB2 obejmują GdMn2, HfV2, CeNi2 i TiCr1.8.
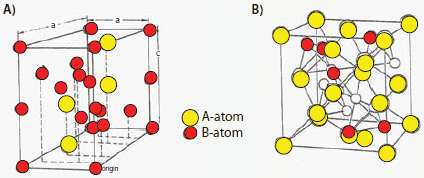
Rysunek 8.(A) Jedna ze struktur faz C14 Laves25 i (B) jedna ze struktur faz C15 Laves.26
W tym przypadku AB2 wspólne pierwiastki dla A to Ti, Zr, Hf i inne pierwiastki ziem rzadkich (z wyłączeniem Lu). Powszechnymi pierwiastkami w miejscu B są Cr, V, Fe i Mn. W celu poprawy wydajności akumulatora można zastosować wiele zamienników pierwiastków A i B. Daimler Benz opracował TiZr0,02V0,43Fe0,09Cr0,05Mn01,5 (Tabela 2, Nr. 10, Product No. 685941), komercyjny stop, który ma rozsądną cenę.28
Trzecia klasa materiałów, które mogą mieć potencjał w akumulatorach NiMH to wodorki AB. Mają one zazwyczaj strukturę typu "CsCl" (Strukturbericht B2, grupa przestrzenna Pm-3m). Libowitz29 po raz pierwszy doniósł o wodorkach ZrNi, które hydratowały w temperaturze około 100 °C, a w 1974 r. Reilly30 opracował stop FeTi (Tabela 2, nr. 17), który tworzył FeTiH i FeTiH1.5 i wykazywał dwa plateau w temperaturze 30 °C. Reilly31 odkrył również TiFe0.7Mn0.2, który wykazuje H/M = 1 w temperaturze 40 °C, a Sandrock32 opracował TiFe1-y Aly (y = 0.04 do 0,10), TiFe0,85Mn0,15 i TiFe0,8Ni0,2 (Tabela 2, nr 17 i 18).32
Podstawienia A i B w AB5 i AB2 związkach
Wodorki związków liniowych to LaNi5, YNi5 (Nr produktu. 693928) , CeNi5, MmNi5 i inne. Składniki A i B są zazwyczaj zastępowane w celu uzyskania najbardziej pożądanych właściwości. Na przykład właściwości izotermy są modyfikowane w celu uzyskania pożądanego ciśnienia plateau, w niektórych przypadkach prawie dwa rzędy wielkości w pobliżu temperatury roboczej. LaNi5 to modelowy związek, który ma ciśnienie plateau 1,5 atm; NdNi5, CeNi5 i inne również mają wysokie ciśnienia plateau. Podstawienia w miejscu A obejmują komercyjne mieszanki stopów mischmetalu (La, Pr, Ce, Nd). W tym przypadku histereza jest zwiększona, ale zdolność magazynowania wodoru nie jest zmniejszona. Możliwe są również częściowe podstawienia w związkach takich jak Mm1-xCaNi5, które dają obniżone ciśnienia plateau, a także histerezę. Podstawienie Ni w miejscu B za pomocą Pt, Cu i innych nie doprowadziło do powstania użytecznych związków. Z drugiej strony, częściowe podstawienie miejsca B doprowadziło do wielu zmian właściwości termodynamicznych. W przypadku zastosowań akumulatorowych ważne jest, aby podczas uwadniania/odwadniania zachodziła minimalna zmiana objętości; wykazano, że dodanie Co zmniejsza zmianę objętości. Sakai poinformował, że w pełni podstawione MmNi5, stosowane w elektrodach akumulatorowych, ma pewną zawartość Co w celu poprawy żywotności elektrody.37 Istnieją inne patenty i cytaty, które nie zostały uwzględnione w tym przeglądzie ze względu na zwięzłość. Komercyjne B-podstawione stopy MmNi5 zawierające Co, Al i Mn wykazują ciśnienie plateau poniżej 1 bara i dobrą odporność na korozję. Sugeruje się, że komercyjny skład stopu elektrodowego wynosi około MmNi3,5Co0,8Mn0,4Al0,3. Stop ten ma dużą wartość komercyjną dla zastosowań akumulatorowych, a także innych stopów do przechowywania wodoru w ogniwach paliwowych i innych stacjonarnych zastosowaniach do przechowywania wodoru. Częściowe podstawienia miejsc B za pomocą Sn, Mn, In i Si również dały wodorki o doskonałych właściwościach. Najciekawsze z nich, które uzyskały optymalne właściwości hydratacyjne, to Al i Sn. Dobrze znany LaNi4.5Al0.5 został użyty do zastosowań Tritum. Przykład pojedynczej substytucji pierwiastkiem B pokazano dla LaNi5.2 i LaNi4.8Sn0.2 (Rysunki 5 i 6). Można zauważyć, że zmiany pierwiastka stopowego mają duży wpływ na żywotność cyklu termicznego. Bowman poprawił właściwości tych stopów, które zostały wykorzystane w pompach ciepła w zastosowaniach kosmicznych.33 Ponadto stwierdzono, że dzięki tym zamianom możliwa jest poprawa żywotności cyklu.34 Metale ziem rzadkich są również podstawiane w związkach AB2 związki takie jak MmMnAl, LaMnAl, TiZr0.02V0.43Fe0.09Cr0.05Mn01.5 i TiMn1.4V0.62 są równie ważne dla naszych zastosowań. Sandrock i Goodell przeprowadzili również cykliczne zmiany ciśnienia otoczenia na Fe0.85Mn0.15Ti0.5 i wykazali wpływ zanieczyszczeń gazowych na cykliczne zmiany ciśnienia.35
Reakcje elektrochemiczne w akumulatorach NiMH
Schemat akumulatora NiMH pokazano na Rysunek 9, gdzie wodorek metalu jest elektrodą ujemną, NiO(OH)/Ni(OH)2 jest elektrodą dodatnią, a KOH jest elektrolitem. Po stronie dodatniej elektroda Ni(OH)2 utlenia się do NiO(OH) podczas ładowania i redukuje z powrotem do Ni(OH)2 podczas rozładowywania. Na elektrodzie ujemnej wodorek metalu redukuje się do stopu podczas rozładowywania. Równania redoks ładowania-rozładowania są również pokazane na Rysunku 9. Należy zauważyć, że w tego typu akumulatorach nie występuje mechanizm wytrącania, jak ma to miejsce w akumulatorach Ni/Cd i innych; mechanizm ładowania/rozładowania odbywa się poprzez przenoszenie protonów między wodorotlenkiem niklu a wodorkiem metalu.

Rysunek 9.Mechanizm ładowania-rozładowania w akumulatorze NiMH.
Przez lata związki AB5 były optymalizowane pod kątem długiej żywotności, integralności strukturalnej, odporności na korozję i niskich kosztów. Należy zauważyć, że zastąpienie wodorków AB5 lub AB2 ma głęboki wpływ na właściwości wodorków, które zostały zoptymalizowane przez producentów akumulatorów. Dekrepitacja AB5 elektrod została poprawiona przez dodanie Co, Mn i Al do LaNi5 (Nr produktu 685968) . Koriyama zgłosił elektrochemiczną trwałość elektrod ze względu na podstawienie różnych pierwiastków w elektrodzie LaNi5, i są one wymienione w Tabeli 3.36
.
Tabela 3.Wpływ zastąpienia La w stopie na bazie LaNi5 innymi pierwiastkami ziem rzadkich.
Zwykle do produkcji akumulatorów stosuje się proszki Mm(Ni,Co,Mn,Al)5 lub blisko spokrewnione kompozycje. Zasięg jazdy Mitsubishi® Libero EV został ustalony na 220 mil przy energii akumulatora 28 kwH na podstawie raportu z 1999 roku.3 Żywotność cykliczna akumulatorów NiMH wynosi zazwyczaj 1000 przy (praktycznym) ładunku właściwym 70-80 Wh/kg, chociaż teoretyczne ładunki mieszczą się w zakresie 220 i 230 Wh/kg odpowiednio dla AB5 i AB2.37 Dla materiału MmNi3.6Al0.4Co0.7Mn0.3 stopu, pojemności rozładowania stopu pozostają na poziomie 250 mAh/g z nominalnym zanikiem pojemności (w zakresie ~20 mAh/g) po dłuższym cyklu. Przeprowadzono również badania na złożonych stopach podstawionych (ze Szwecji) MmNi5 [(La0.58Ce0.29Nd0.08Pr0.05) (Ni3.6Co0.7Mn0.3Al0.4)], które wykazały lepszą aktywację i wysoką wydajność rozładowania dzięki zastosowaniu spiekanych elektrod wodorkowych.38 Inny przykład żywotności LaNi4.7Al0.0.3 w porównaniu do Mm0.95Ti0.05Co0.45Mn0.35Al0.15 pokazano na Rysunku 10.39 Inny przykład elektrochemicznego cyklu LaNi4.8Sn0.1+x pokazał, że LaNi4.8Sn0.2 miał lepszą stabilność cykliczną niż stopy niestechiometryczne, takie jak LaNi4.8Sn0.1 i LaNi4.8Sn0.4 (Rysunek 11).

Rysunek 10.Pojemność rozładowania Mm0.95Ti0.05Co0.45Mn0.35Al0.35 i LaNi4.7iAl0.3.

Rysunek 11.Pojemność rozładowania niestechiometrycznego stopu LaNi4.8iSn0.1+x.
Społeczne skutki stosowania akumulatorów NiMH
Akumulatory wodorkowe NiMH są wykorzystywane w hybrydowych akumulatorach samochodowych, elektrycznych maszynkach do golenia, szczoteczkach do zębów, aparatach fotograficznych, kamerach, telefonach komórkowych, pagerach, instrumentach/sprzęcie medycznym i wielu innych zastosowaniach. Ponieważ technologia akumulatorów litowo-jonowych rozwija się w przyspieszonym tempie, rozwój materiałów do produkcji akumulatorów NiMH musi być kontynuowany, aby technologia ta pozostała konkurencyjna. Wydaje się jednak, że akumulatory NiMH mają nieco lepsze cykle życia niż akumulatory litowo-jonowe (Rysunek 2) w oparciu o MJ/Wh. Należy zauważyć, że Toyota™ Prius z 2010 roku wykorzystuje akumulatory NiMH firmy Sanyo® Electric Co.
Wodorki metali mają kilka innych zastosowań poza technologią akumulatorów. Jednym z nich jest magazynowanie wodoru w samochodowych ogniwach paliwowych i silnikach spalinowych. Ma to ogromny wpływ na środowisko, ponieważ pojazdy napędzane wodorem emitują wodę, a nie CO2. Wiele firm stworzyło prototypy samochodów napędzanych wodorem/ogniwami paliwowymi; Frank Lynch z HCI w Kolorado opracował metalowe zbiorniki w latach 70. do obsługi ciągników Caterpillar® wykorzystujących te wodory. Główną kwestią dla praktycznych nowoczesnych samochodów jest opracowanie niezawodnych lekkich wodorków, które są odwracalne i mają około 10 % mas. pojemności H. Dzięki dodatkowemu rozwojowi i optymalizacji można mieć nadzieję, że niektóre ze stopów akumulatorów wymienionych w Tabeli 2 mogą kiedyś zostać wykorzystane do tego celu.
Referencje
Zaloguj się lub utwórz konto, aby kontynuować.
Nie masz konta użytkownika?