Wichtige Dokumente
MSQC4
SILu™Lite SigmaMAb universeller Antikörperstandard human
Synonym(e):
IgG1-Leichtkette, SILu™Lite SigmaMAb universeller Antikörperstandard, human, SigmaMAb
About This Item
Empfohlene Produkte
Verwandte Kategorien
Allgemeine Beschreibung
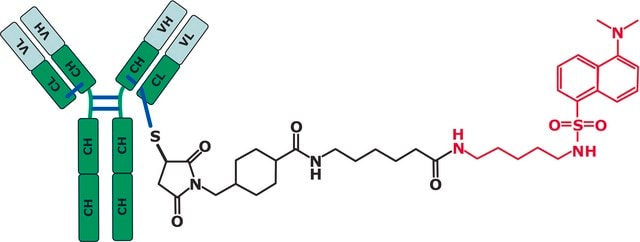
Es besteht aus zwei identischen schweren Ketten und zwei identischen leichten Ketten. Die schweren Ketten und die leichten Ketten sind durch eine Disulfidbrücke verbunden. Die schweren Ketten sind durch zwei Disulfidbrücke in einer Gelenkdomäne verbunden. Die anderen 12 Cysteinbindungen sind intramolekular auf sechs verschiedene globuläre Domänen beschränkt. Die Antikörpersequenz wurde durch Analyse der intakten Masse und Peptid-Mfapping unter Verwendung vier verschiedener Enzyme bewertet: Chymotrypsin, Endoproteinasen Asp-N und Glu-C sowie Trypsin. Eine Sequenzabdeckung von 100 % wurde erreicht.
Anwendung
Leistungsmerkmale und Vorteile
Beschreibung / Zusammensetzung / Modifikation / Durchschnittliche Masse (Da)
Leichtkette, reduziert / C1006H1555N267O333S7 / Pyroglutaminsäure (Q) / 22942,2
Schwerkette, reduziert / C2181H3393N587O663S16 / (keine Modifikation) / 48957,8
C2237H3485N591O702S16 / G0F / 50403,2
C2243H3495N591O707S16 / G1F / 50565,3
C2249H3505N591O712S16 / G2F / 50727,5
Native intakte Masse, nicht reduziert / C6374H9864N1708O1992S46 / 2 x Pyroglutaminsäure (Q) / 143767,7
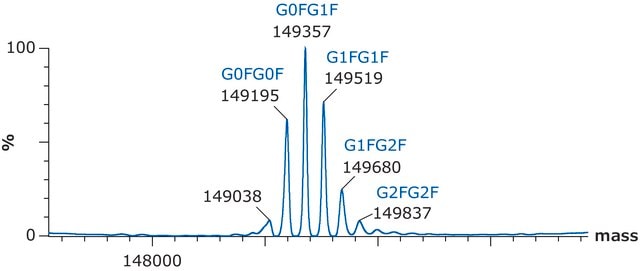
C6486H10048N1716O2070S46 / G0F+G0F / 146658,4
C6492H10058N1716O2075S46 / G0F+G1F / 146820,6
C6498H10068N1716O2080S46 / G1F+G1F / 146982,7
C6504H10078N1716O2085S46 / G1F+G2F / 147144,8
C6510H10088N1716O2090S46 / G2F+G2F / 147307,0
Physikalische Form
Angaben zur Herstellung
Hinweis zur Analyse
EVQLVESGGGLVQPGGSLRLSCVASGFTLNNYDMHWVRQGIGKGLEWVSKI
GTAGDRYYAGSVKGRFTISRENAKDSLYLQMNSLRVGDAAVYYCARGAGRW
APLGAFDIWGQGTMVTVSS|ASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYF
PEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVN
HKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISR
TPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRV
VSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPS
RDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFL
YSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG
SigmaMAb-Leichtkette
QSALTQPRSVSGSPGQSVTISCTGTSSDIGGYNFVSWYQQHPGKAPKLMIY
DATKRPSGVPDRFSGSKSGNTASLTISGLQAEDEADYYCCSYAGDYTPGV
VFGGGTKLTVL|GQPKAAPSVTLFPPSSEELQANKATLVCLISDFYPGAVTV
AWKADSSPVKAGVETTTPSKQSNNKYAASSYLSLTPEQWKSHRSYSCQ
VTHEGSTVEKTVAPTECS
Sonstige Hinweise
Röhrcheninhalte durch Hinzufügen von 500 μL Reinstwasser oder Phosphatpuffer und anschließendes energisches Mischen rekonstituieren. Das aufgelöste Produkt kann nach Bedarf weiter verdünnt werden:
Rechtliche Hinweise
Ergänzung
Ähnliches Produkt
Lagerklassenschlüssel
11 - Combustible Solids
WGK
WGK 1
Flammpunkt (°F)
Not applicable
Flammpunkt (°C)
Not applicable
Hier finden Sie alle aktuellen Versionen:
Analysenzertifikate (COA)
Die passende Version wird nicht angezeigt?
Wenn Sie eine bestimmte Version benötigen, können Sie anhand der Lot- oder Chargennummer nach einem spezifischen Zertifikat suchen.
Besitzen Sie dieses Produkt bereits?
In der Dokumentenbibliothek finden Sie die Dokumentation zu den Produkten, die Sie kürzlich erworben haben.
Kunden haben sich ebenfalls angesehen
Unser Team von Wissenschaftlern verfügt über Erfahrung in allen Forschungsbereichen einschließlich Life Science, Materialwissenschaften, chemischer Synthese, Chromatographie, Analytik und vielen mehr..
Setzen Sie sich mit dem technischen Dienst in Verbindung.