CBILS®
イオン液体合成の画期的なツール
オーストリアproionic社の製品であるCBILS®(Carbonate Based Ionic Liquid Synthesis)は、極めて簡単かつ巧妙なイオン液体の合成法です。1近年、3級アミンのアルキル化、4級アンモニウム塩とルイス酸の反応、メタセシス反応などによる4級アンモニウム塩のアニオン交換2などのさまざまなイオン液体の合成法が数多く報告されています。3
CBILS®を用いれば、1日に20種以上の新規のイオン液体を系統的に合成することも可能です。
CBILS®の反応機構
CBILS®は、1-ethyl-3-methylimidazoliumのような窒素またはリンカチオンと炭酸水素アニオンまたはメチル炭酸アニオンから構成されています。ブレンステッド酸との反応により、CBILS®のアニオンが当量の二酸化炭素と水またはメタノールに分解されます(Scheme 1)。

Scheme 1.Straightforward synthesis of 1-ethyl-3-methylimidazolium acetate using CBILS® EMIM HCO3
この交換反応では、二酸化炭素の発生により化学平衡は常に右に移動しているため、極めて溶解性の低いブレンステッド酸を用いた場合でも反応は定量的に進行します。CO2は反応系から完全に除去されると同時にブレンステッド酸のアニオンが置換され、反応副生成物の蒸留除去により、目的のイオン液体が容易に単離できます。
単純な無機酸からキラル部位や官能基を有する複雑な酸、強酸・弱酸、可溶性・不溶性によらず、数多くの市販のブレンステッド酸をアニオンとして選択できます。さらに、ブレンステッド酸源として、有機・無機酸無水物を用いることも可能です。例えば、水溶液に対する溶解性が極めて低い酸化モリブデンや酸化タングステンを用いて、それぞれイオン液体が合成されました。ゆっくりとした、しかし継続的なCO2の発生により、スラリー状ではあるものの、目的のイオン液体が100%の変換率で生成したことが示されています。
CBILS®の応用例
イオン液体は遊離酸や炭酸塩前駆体に対して不安定な可能性があるため、反応の正確な化学量論が重要です。CBILS®試薬は、各ロットの濃度を製品ラベルに記載しています。アニオンとなる酸も1%以内の精度で滴定し正確な濃度を求めて用いてください。2価のブレンステッド酸の化学量論を調整することにより、容易にScheme 2のようなアニオンを有するイオン液体が得られます。

Scheme 2Formal synthesis of 1-ethyl-2,3-dimethylimidazolium hydrogensulfate using CBILS® EMMIM CH3OCO2 and sulfuric acid as diprotic Brønsted acid
遊離酸が不安定であるなどの理由でブレンステッド酸を用いることができない場合には、相当するアンモニウム塩を用いて目的のイオン液体を得ることができます。たとえば、チオシアン酸アニオン(SCN–)は5%水溶液中0℃以下で安定に存在し市販されていませんが、Scheme 3の例では、反応混合物を穏やかに加温し、60℃で30分以上反応させ、その後70℃で溶媒を除去しています。
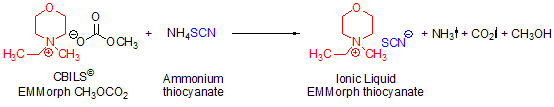
Scheme 3Synthesis of N-ethyl-N-methylmorpholinium thiocyanate using CBILS® EMMorph CH3OCO2 and ammonium thiocyanate as stable equivalent to the not directly accessible thiocyanic acid (HSCN)
CBILS®を用いた反応では、不溶性の炭酸塩を形成するCa, Zn, Mnなどの金属塩もブレンステッド酸の代わりに用いることができます。例えば、チオシアン酸カルシウム(Ca(SCN)2)を用いれば、目的のSCN–を有するイオン液体が得られ、同時に生成する炭酸カルシウムの沈殿は、ろ過もしくは遠心分離により容易に除去できます(Scheme 4)。

Scheme 4Synthesis of 1-butyl-3-methylimidazolium thiocyanate using CBILS BMIM HCO3 and calcium thiocyanate.
1週間に100化合物を合成可能?
CBILS®を用いることにより、10種のCBILS前駆体と10種のブレンステッド酸を組み合わせて、1週間に100種の新規のイオン液体または類縁物質を合成することも可能です。脱水溶媒が不要、ハロゲンの不純物不含、副生成物を伴わない、明確な反応機構、廃棄物がない、などのさまざまな面で利点があり、CBILSカチオン前駆体と酸由来のアニオンの組み合わせを選択するだけで、目的のイオン液体が合成できるようになりました。
操作手順
- 対応するCBILS®前駆体からカチオン種を選択する
- 対応するブレンステッド酸からアニオンを選択する
- 必要な化学量論を求める
- CBILS®前駆体とブレンステッド酸を混合しCO2が発生しなくなるまで攪拌する。基質により反応時間は異なるが、通常は5分~1時間程度要する
- エバポレーターで溶媒と副生成物(水もしくはメタノール)を除去する
私たちは、イミダゾリウム系、アンモニウム系、ホスホニウム系、ピリジニウム系、ピペリジニウム、およびモルフォリニウム系の各種イオン液体の合成に利用できる11種類のCBILS®前駆体のメチル炭酸塩と炭酸水素塩を提供しています。CBILS® イオン液体前駆体はすべて40~60%の水溶液または水/メタノール溶液でお届けしています。
参考文献:
続きを確認するには、ログインするか、新規登録が必要です。
アカウントをお持ちではありませんか?