Studio sui filtri da siringa Millex® per la determinazione di impurezze appartenenti alla classe delle nitrosammine nei farmaci
Determinazione delle impurezze appartenenti alla classe delle nitrosammine
L'individuazione e la quantificazione delle nitrosammine nei medicinali è essenziale per garantire la sicurezza e la qualità dei prodotti farmaceutici. Si sospetta, infatti, che queste sostanze abbiano proprietà cancerogene e genotossiche e che rappresentino, quindi, un rischio per la salute dei pazienti.1-4 Introdotte nei processi di sintesi attraverso molteplici vie difficili da prevedere, le impurezze da nitrosammine sono state rilevate in principi attivi ed eccipienti farmaceutici, il che ha determinato numerosi richiami di prodotti a partire dal 2018, tra cui quello del valsartan.5,6
Requisiti normativi per le analisi delle nitrosammine
Le agenzie di regolamentazione dei prodotti farmaceutici e organizzazioni come l'U.S. Food and Drug Administration (FDA), l’Agenzia Europea per i Medicinali (EMA) e l’International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use (ICH) hanno emanato linee guida e requisiti concernenti le nitrosammine nei prodotti farmaceutici. Una sintesi dei punti fondamentali è riportata in Tabella 1.
Queste autorità di regolamentazione continuano a monitorare attivamente e ad aggiornare le loro linee guida sulle impurezze da nitrosammine per garantire la salute e la sicurezza pubblica. È importante che i produttori farmaceutici si attengano a tali linee guida e a questi requisiti, valutando e mitigando il rischio di contaminazione da nitrosammine nei farmaci.
Metodi analitici per l’analisi delle nitrosammine
Le agenzie di regolamentazione di tutto il mondo, come EMA, U.S. FDA e altre, hanno sottolineato l'importanza di metodi analitici robusti per l'analisi delle nitrosammine nei prodotti farmaceutici. La LC-MS/MS è uno dei metodi analitici comunemente raccomandati dalle agenzie di regolamentazione per l'analisi delle nitrosammine. La combinazione della separazione ottenuta mediante cromatografia liquida ad alte prestazioni (HPLC) con la rivelazione della spettrometria di massa tandem (MS/MS) assicura sensibilità, selettività e accuratezza elevate. La LC-MS/MS è in grado di rilevare e quantificare diverse nitrosammine fino a livelli di tracce in matrici complesse, il che ne fa una tecnica adatta per le analisi di routine e per il rispetto dei limiti stabiliti dalle normative. La Procedura 3 descritta in USP <1469> si avvale della LC-MS/MS per la quantificazione delle nitrosammine.13 Inoltre, U.S. FDA, Farmacopea Europea14, Health Sciences Agency (HSA) di Singapore,15 e Taiwan Food and Drug Administration16 hanno pubblicato metodi LC-MS/MS per la determinazione delle nitrosammine nella ranitidina e in altri medicinali.
L’HPLC accoppiata alla spettrometria di massa ad alta risoluzione (HPLC-HRMS o LC-HRMS) è un’altra tecnica fondamentale per l’analisi delle nitrosammine. La selettività di questo metodo ha consentito di differenziare tra impurezze nitrosammino-simili e nitrosammine effettive, assicurando risultati analitici affidabili. La FDA ha sviluppato e convalidato metodi LC-HRMS17 e anche la Procedura 1 descritta in USP <1469> fa riferimento a questo metodo.7
Per l’analisi delle nitrosammine, si può impiegare anche l’HPLC con rivelazione UV/Vis. Benché questa tecnica possa essere caratterizzato da minore sensibilità rispetto alla LC-MS/MS, essa può costituire un metodo rapido per l’analisi di materie prime, solventi o eccipienti. L’Agence Nationale de Sécurité du Médicament et des Produits de Santé (ANSM) prevede due metodi basati sull’HPLC-UV.18,19
La gascromatografia accoppiata alla spettrometria di massa (GC-MS/MS) è un’altra tecnica comunemente impiegata per l’analisi delle nitrosammine in quanto offre sensibilità e specificità eccellenti nell’individuazione delle nitrosammine ed è particolarmente utile nel caso di nitrosammine volatili. USP <1469>,10 Taiwan FDA,13 e Swissmedic20 si avvalgono di metodi GC-MS/MS per l’analisi delle nitrosammine, mentre l’Health Sciences Agency (HSA) di Singapore ha pubblicato un metodo basato sulla gascromatografia accoppiata alla spettrometria di massa ad alta risoluzione e accuratezza (HRAM-GCMS).21
Requisiti della filtrazione dei campioni per l’analisi delle nitrosammine
La maggior parte dei metodi fin qui menzionati richiede la filtrazione dei campioni prima dell'iniezione. La filtrazione è il modo più semplice per rimuovere prima dell'iniezione le particelle presenti nei campioni e nelle fasi mobili, che potrebbero influenzare significativamente le prestazioni di un HPLC. Nei prodotti farmaceutici come il valsartan le particelle sono molto comuni; esse si originano nel processo di dissoluzione della formulazione. La classificazione di un filtro a membrana sulla base delle dimensione dei suoi pori dà un'indicazione della misura delle particelle che il filtro può trattenere; nei metodi HPLC solitamente si consigliano filtri da 0,45 µm. Quando si utilizzano colonne impaccate con particelle particolarmente fini (ad esempio, inferiori a 2 µm di diametro) e in UHPLC, si raccomandano filtri da 0,2 μm. È importante notare che a parità di dimensione dei pori, i filtri a membrana non presentano sempre la stessa efficienza di ritenzione, come dimostrato in uno studio precedente.22
In Tabella 2 sono elencate le fasi di filtrazione previste in alcuni metodi pubblicati dalle agenzie di regolamentazione di tutto il mondo. Per i metodi analitici delle nitrosammine, si preferisce il ricorso ai filtri da siringa. Due caratteristiche importanti dei filtri da siringa di cui tener conto sono il materiale costitutivo della membrana filtrante e la dimensione dei pori. Il PVDF e il PTFE sono i materiali dei filtri a membrana più comunemente citati nei metodi analitici pubblicati; in alcuni casi vengono citati anche il nylon e il polipropilene idrofilo (ad esempio, la membrana GHP) (Tabella 2). Le dimensioni dei pori suggerite nei diversi metodi sono 0,2, 0,22 e 0,45 μm.
Metodi sperimentali
In questo studio si è utilizzato il metodo USP <1469>, Procedura 3 precedentemente convalidato.31 La Sezione 1 consiste nello studio degli estraibili dei filtri da siringa appartenenti alla classe delle nitrosammine e la Sezione 2 è uno studio sui recuperi condotto su campioni addizionati di valsartan puro (spiked). Le condizioni di esecuzione delle analisi LC-MS/MS sono riportate in Tabella 3, le transizioni MRM in Tabella 4.
Filtri da siringa esaminati Sono state esaminate tre unità per ciascuno di due lotti di (1) filtri Millex® in PVDF da 0,22 µm e (2) filtri Millex® in PTFE da 0,2 µm e tre unità di un lotto per ciascuno dei seguenti filtri: (3) Fornitore P in PVDF da 0,2 µm, (4) Fornitore C in H-PTFE 0,2 µm, (5) Fornitore M in PVDF da 0,2 µm e (6) Fornitore M in PTFE da 0,2 µm.
Sezione 1 - Estraibili. Per determinare se vi fossero livelli di base di nitrosammine di cui tener conto dovuti agli estraibili dei filtri da siringa, un campione costituito da solo diluente (acido formico in acqua, 0,1% v/v) è stato addizionato (spiking) di quattro standard interni (SI) marcati isotopicamente, come previsto dal metodo USP <1469> [10 µg/mL per NDMA-d6 e NMBA-d3 e 1 µg/mL per NDEA-d10/NDBA-d18]. Dopo aver vortexato e centrifugato (10.000 rpm per 10 min) i campioni, si è filtrato il surnatante con filtri da siringa di 13 mm. Il filtrato è stato analizzato per la determinazione di sei nitrosammine mediante LC-MS/MS. Per determinare le concentrazioni corrispondenti ci si è avvalsi di una curva di calibrazione esterna che copriva gli intervalli 1,33 - 90 ng/mL (NDMA, NMBA, NEIPA, NDIPA e NDBA) e 0,66-69,4 ng/mL (NDEA).
Sezione 2 - Recuperi. 40 mg di valsartan dura (dose da 80) sono stati polverizzati, diluiti con acido formico all’1% in acqua e addizionati (spiked) di basse concentrazioni (L2) degli analiti, come descritto in USP <1469>. I campioni sono stati centrifugati, filtrati e analizzati mediante LC-MS/MS.
Esame dei filtri per l'analisi delle nitrosammine
La filtrazione dei campioni prima dell'iniezione è parte integrante di molti metodi per l'analisi delle impurezze da nitrosammine basati su LC-MS e GC-MS. Garantire l'assenza di estraibili nelle unità filtranti è fondamentale ai fini dell'accuratezza e della coerenza dei risultati ottenuti con questi metodi. Inoltre, è essenziale condurre studi sui recuperi, poiché alcune molecole hanno la capacità di legarsi ai componenti dei filtri da siringa e quindi possono influenzare la qualità dei dati generati.
Per valutare i filtri da siringhe ci si è avvalsi di un metodo convalidato basato sulla procedura 3 del metodo USP <1469>27 che descrive l'uso della LC-MS/MS per la quantificazione di NDMA, NDEA, NDIPA, NEIPA, NMBA e NDBA in alcuni sartani (valsartan, losartan potassio, olmesartan medoxomil, candesartan cilexetil e telmisartan). L'ultima parte della sottosezione “Soluzione del campione” del metodo richiede la filtrazione “utilizzando un filtro in politetrafluoroetilene (PTFE) idrofilo con pori di 0,45 μm” dopo la centrifugazione.11
Sezione 1– Estraibili
Il filtrato ottenuto con i filtri da siringa è stato analizzato per determinare le concentrazioni di eventuali estraibili appartenenti alla classe delle nitrosammine utilizzando una curva di calibrazione esterna che copriva gli intervalli 1,33 - 90 ng/ml (NDMA, NMBA, NEIPA, NDIPA e NDBA) e 0,66-69,4 ng/ml (NDEA). In Figura 1 è riportato un cromatogramma d'esempio MRM di questi composti.
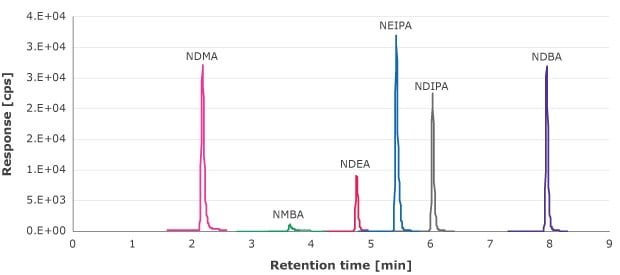
Figura 1.Cromatogramma MRM delle soluzioni standard di nitrosammine (10 ng/ml per NDMA, NMBA, NEIPA, NDIPA e NDBA; 6,6 ng/mL per NDEA).
Si definisce limite di quantificazione (LOQ) la concentrazione che dà luogo a un rapporto S/N di 10. Il valore minimo di concentrazione delle curva di calibrazione di ciascuna nitrosammina presa in esame generava un S/N >10. Nessuna delle nitrosammine allo studio è risultata presente in concentrazione pari o superiore a questo valore in nessuno dei filtri analizzati (Tabella 5).
ABBREVIAZIONI: S/N = rapporto segnale/ rumore di fondo; PVDF = poli(vinilidene) fluoruro idrofilo; PTFE = politetrafluoretilene idrofilo; LOQ = limite di quantificazione; ND = non rilevato
Accertare che le unità filtranti non presentino estraibili chimici che potrebbero interferire con la qualità dei risultati è fondamentale, soprattutto con i metodi che si avvalgono di strumentazione altamente sensibile. Gli estraibili devono essere evitati perché possono co-eluire con i picchi degli analiti o presentarsi come picchi inattesi nelle successive analisi, rendendo più difficile l'interpretazione dei dati. Gli estraibili potrebbero essere originati da materiali distaccatisi dal filtro, da residui chimici del processo produttivo o da sostanze chimiche secondarie che vengono dilavate dal filtro. Nel caso specifico delle nitrosammine, gli estraibili potrebbero essere generati inavvertitamente durante la colata della membrana (casting).
Sezione 2 - Recuperi nel valsartan
Lo studio dei recuperi è stato eseguito mediante spiking dei campione di valsartan con standard di riferimento a bassi livelli di concentrazione (L2). Le soluzioni campione preparate sono state analizzate mediante LC-MS/MS, utilizzando una curva di calibrazione esterna per calcolare la concentrazione dei singoli analiti. Si è proceduto determinando il rapporto tra il segnale dello standard interno e il segnale dell'analita (ad esempio, segnale della NDMA-D6/ segnale della NDMA) nella soluzione campione e nelle soluzioni di calibrazione esterna.
La tabella 6 mostra i recuperi medi per i filtri da siringa in PVDF e in PTFE presi in esame. I tassi di recupero erano compresi nell’intervallo di accettabilità che va dal 70 al 130%31 per tutte le unità e i materiali saggiati, con alcune piccole differenze evidenti al variare delle sostanze e dei materiali delle membrane. Ad esempio, i recuperi risultano relativamente ridotti per la NDBA (ma ancora nell’intervallo di accettabilità), forse a causa delle interazioni idrofobiche con la matrice filtrante o con altri ingredienti del prodotto farmaceutico. I recuperi dei filtri da siringa Millex® sia in PTFE, sia in PVDF idrofilo si mantenevano costanti al variare del lotto.
Un altro fattore da considerare quando si scelgono i materiali di fabbricazione dei filtri da siringa è l’adsorbimento aspecifico (binding) delle molecole di analita sull’unità filtrante, fenomeno che potrebbe provocare recuperi scarsi. L'entità dell’adsorbimento è determinata dalle proprietà fisico-chimiche dell’unità filtrante (membrana e alloggiamento) e dalle caratteristiche chimiche dell'analita. Diverse interazioni secondarie, come le interazioni elettrostatiche, i legami a idrogeno e le interazioni idrofobiche, contribuiscono all’adsorbimento dell'analita sul filtro a membrana e sul suo alloggiamento.32 In questo studio, i recuperi relativamente più bassi per l'NDMA osservati sia con le unità filtranti con membrana in PVDF, sia in PTFE (comunque entro l’intervallo di accettabilità) potrebbero essere il risultato di interazioni idrofobiche tra l'NDMA e la membrana. Nel caso della NDIPA, si è ottenuto un tasso di recupero inferiore con le membrane in PVDF, il che significa che la molecola potrebbe interagire in maniera differente con i due polimeri PTFE e PVDF. Altri polimeri con gruppi funzionali polari e maggiore tendenza all’adsorbimento aspecifico, come il nylon, mostrerebbero probabilmente livelli di adsorbimento più elevati e quindi maggiori perdite di analiti. A vantaggio della massima accuratezza nella determinazione dei recuperi, si suggerisce quindi di scartare il primo ml di filtrato durante la preparazione del campione, come raccomandato dai metodi della U.S. FDA per la determinazione delle nitrosammine.23,24 In questo modo si garantisce che i siti responsabili del binding siano stati saturati dall’analita e non possano causarne ulteriori perdite. Abbiamo osservato questo fenomeno anche con i materiali ad alto tasso di adsorbimento, come il nylon.
Determinazione delle impurezze appartenenti alla classe delle nitrosammine e scelta dei filtri
Tutti i filtri da siringa esaminati, in PVDF e in PTFE, hanno mostrato livelli di estraibili della classe delle nitrosammine inferiori al limite di quantificazione, determinati seguendo la Procedura 3 del metodo USP <1469>. Inoltre, tutti hanno fornito recuperi accettabili degli spike di nitrosammine, mostrando solo minime differenze tra i diversi composti. Ciò dimostra l'idoneità di queste unità filtranti per la preparazione dei campioni nei metodi analitici delle nitrosammine.
Applicazioni correlate
- Analisi e controllo qualità (CQ) di piccole molecole
Disporre di un sistema di analisi e controllo qualità (CQ) che operi in conformità alle specifiche delle farmacopee internazionali è un fattore critico nella ricerca di nuovi farmaci. Le analisi chimiche e microbiologiche garantiscono che le molecole, grandi o piccole, siano sviluppate e prodotte secondo le Norme di buona fabbricazione (GMP).
- Metodi compendiali e orientamenti normativi
L’analisi in base a metodi compendiali è parte integrante della messa in commercio di un prodotto farmaceutico. Le farmacopee internazionali, come la USP e la EP, hanno definito i propri standard qualitativi. L’impiego di test conformi agli standard descritti in dettaglio dai metodi compendiali costituisce un requisito fondamentale per gli ingredienti e i prodotti ad uso farmaceutico.
Bibliografia
Per continuare a leggere, autenticati o crea un account.
Non hai un Account?