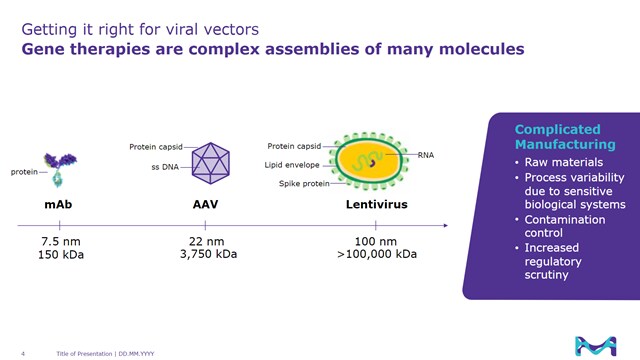
Formulierung, Endfiltration und Abfüllung viraler Vektoren

Die letzten Schritte bei der Herstellung von viralen Vektoren sind die Formulierung, Endfiltration und Abfüllung. Ein optimiertes Formulierungsdesign, das auf einer Verbesserung der Lösungsbedingungen und der Verwendung hochwertiger Hilfsstoffe beruht, kann die Stabilität und Haltbarkeit der viralen Vektoren deutlich erhöhen. Unser umfangreiches Sortiment an qualitativ hochwertigen Puffern, Salzen und Stabilisatoren zeichnet sich durch eine geringe Keim- und Endotoxinbelastung aus. Die Produkte wurden speziell für Anwendungen mit hohem Risiko entwickelt und können dazu beitragen, dass das Downstream Processing und die Formulierung Ihres Gentherapeutikums ein voller Erfolg wird.
In Anbetracht dieser hochwertigen Therapien sollte bei der Konzeption eines effektiven Sterilfiltrationssystems einerseits die Maximierung der Produktrückgewinnung im Mittelpunkt stehen und andererseits sollten verschiedene Filteroptionen, Prozessanforderungen, der Bedarf an Probenahmen und die Frage, ob ein Integritätstest vor der Verwendung/nach der Sterilisation (PUPSIT) durchgeführt werden soll, berücksichtigt werden.
Unsere Mobius® Einwegbaugruppen ermöglichen Ihnen die notwendige Flexibilität und unsere Experten unterstützen Sie beim Design maßgeschneiderter Baugruppen für unser breitgefächertes Portfolio an Filtern und Einwegkomponenten. Diese Systeme sind skalierbar und können problemlos repliziert werden, so dass sie Ihren sich ändernden Anforderungen gerecht werden.
In Verbindung mit unserem Emprove®-Programm erhalten Sie für unsere Hilfsstoffe, Filter und Einwegkomponenten eine umfassende Dokumentation, wodurch regulatorische und qualitätsbezogene Risiken in Ihrer Produktion auf ein Minimum reduziert werden. All dies versetzt Sie in die Lage, die Komplexität Ihrer Lieferantenqualifizierung zu reduzieren, Prozesse zu beschleunigen und somit Ihre Gesamtbetriebskosten zu senken.
- Ein breites Portfolio an Hilfsstoffen, hergestellt entsprechend GMP nach den Richtlinien für pharmazeutische Hilfsstoffe der IPEC/PQG
- Filter in Sterilqualität für die Aufreinigung viraler Vektoren
- Mobius® Einwegbaugruppen für die Aufreinigung viraler Vektoren
- Validierungsleistungen zur Bestätigung der Eignung Ihres Einwegfiltrationssystems für den Downstream-Prozess
Weitere technische Informationen
- Broschüre: Your Fast Track Through Regulatory Challenges – The Emprove® Program
Laden Sie unsere Emprove®-Programm-Broschüre herunter, in der Sie mehr darüber erfahren, wie Sie Ihre regulatorischen Prozesse verbessern können.
- Whitepaper: Identifying Appropriate-Quality Raw Materials in an Evolving Regulatory Environment
Dieses Whitepaper erläutert die Herausforderungen und Erfolgsfaktoren bei pharmazeutischen Herstellungsprozessen und Rohstofflieferketten im Zusammenhang mit der Rohstoffbeschaffung inmitten eines sich ständig weiterentwickelnden regulatorischen Umfelds.
- Broschüre: Pharma Raw and Starting Materials - Satisfy Your Regulatory Requirements
Beschleunigen Sie Ihren Weg durch den regulatorischen Dschungel und bringen Sie Ihren neuen Wirkstoff schneller auf den Markt.
- Broschüre: Emprove® Filter und Einwegkomponenten
Eine solidere Risikobewertungen ermöglichen.
Workflow


Upstream Processing viraler Vektoren
Die richtigen Entscheidungen im Upstream-Prozess haben nicht nur Auswirkungen auf den Virusvektor-Titer, sondern auch auf die Downstream-Prozesse, Zeitpläne und Akzeptanz durch die Zulassungsbehörden

Downstream Processing viraler Vektoren
Durch effiziente Virusaufreinigungsverfahren können die Ausbeute verbessert, die Zeit bis zum Patienten verkürzt und die Herstellungskosten gesenkt werden

Charakterisierung viraler Vektoren und Biosicherheitsprüfungen
Kritische Biosicherheitsprüfungen und die Charakterisierung von Virusvektorprodukten können dabei helfen, die Schlüssel-Qualitätsmerkmale Identität, Wirksamkeit, Sicherheit und Stabilität vollständig zu analysieren

Auftragsentwicklung und -herstellung viraler Vektoren
CDMO-Partnerschaften spielen eine entscheidende Rolle beim Voranbringen klinischer Pipelines und bei der erfolgreichen Kommerzialisierung
Um weiterzulesen, melden Sie sich bitte an oder erstellen ein Konto.
Sie haben kein Konto?