375680
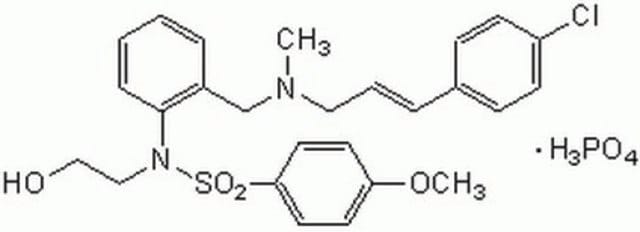
Hesperadin
Hesperadin primarily used in Inhibition.
Synonyme(s) :
Hesperadin, Mammalian Ste20-like Kinase 4 Inhibitor, MST4 Inhibitor, Aurora Kinase Inhibitor X, AMPK Inhibitor II
About This Item
Produits recommandés
Niveau de qualité
Pureté
≥95% (HPLC)
Forme
solid
Fabricant/nom de marque
Calbiochem®
Conditions de stockage
OK to freeze
protect from light
Couleur
yellow
Solubilité
DMSO: 50 mg/mL
Conditions d'expédition
ambient
Température de stockage
−20°C
Description générale
Conditionnement
Avertissement
Reconstitution
Autres remarques
Knowlton, A.L., et al. 2006. Curr. Biol.16, 1705.
Kapoor, T.M., et al. 2006. Science311, 388.
Hirota, T., et al. 2005. Nature438, 1176.
Sessa, F., et al. 2005. Mol. Cell.18, 379.
Lampson, M.A., et al. 2004. Nat. Cell Biol.6, 232.
Hauf, S., et al. 2003. J. Cell Biol.161, 281.
Informations légales
Code de la classe de stockage
11 - Combustible Solids
Classe de danger pour l'eau (WGK)
WGK 2
Point d'éclair (°F)
Not applicable
Point d'éclair (°C)
Not applicable
Certificats d'analyse (COA)
Recherchez un Certificats d'analyse (COA) en saisissant le numéro de lot du produit. Les numéros de lot figurent sur l'étiquette du produit après les mots "Lot" ou "Batch".
Déjà en possession de ce produit ?
Retrouvez la documentation relative aux produits que vous avez récemment achetés dans la Bibliothèque de documents.
Notre équipe de scientifiques dispose d'une expérience dans tous les secteurs de la recherche, notamment en sciences de la vie, science des matériaux, synthèse chimique, chromatographie, analyse et dans de nombreux autres domaines..
Contacter notre Service technique