17-10409
Biocapteur lentiviral, contrôle RFP LentiBrite
Synonyme(s) :
RFP Lentiviral Biosensor
Se connecterpour consulter vos tarifs contractuels et ceux de votre entreprise/organisme
About This Item
Code UNSPSC :
12352207
eCl@ss :
34360190
Nomenclature NACRES :
NA.51
Produits recommandés
Fabricant/nom de marque
Chemicon®
LentiBrite
Niveau de qualité
Technique(s)
cell based assay: suitable
immunocytochemistry: suitable
immunofluorescence: suitable
transfection: suitable
Méthode de détection
fluorometric
Conditions d'expédition
dry ice
Description générale
Lisez note d'application dans Nature Methods !
http://www.nature.com/app_notes/nmeth/2012/121007/pdf/an8620.pdf
(cliquez ici !)
Découvrez les avantages de nos biocapteurs lentiviraux LentiBrite ! Cliquez ici
Les biocapteurs peuvent être utilisés pour détecter la présence ou l'absence d'une protéine donnée, ainsi que la localisation subcellulaire de cette protéine dans une cellule vivante. Les marqueurs fluorescents sont souvent prisés comme moyen de visualiser la protéine d'intérêt dans une cellule par microscopie à fluorescence ou par capture vidéo par intervalles (time-lapse). Visualiser les cellules vivantes sans les perturber permet aux chercheurs d'observer les conditions cellulaires en temps réel.
Les systèmes du type vecteur lentiviral constituent un outil de recherche populaire qui permet d'introduire des produits génétiques dans les cellules. La transfection lentivirale présente certains avantages par rapport aux méthodes non virales telles que la transfection par voie chimique, notamment une plus grande efficacité de transfection vis-à-vis des cellules en division ou non, une expression stable du transgène sur le long terme, et une faible immunogénicité.
EMD Millipore présente les biocapteurs lentiviraux LentiBrite, une nouvelle gamme de particules lentivirales pré-conditionnées codant pour des protéines importantes et fondamentales de l'autophagie, de l'apoptose et de la structure cellulaire, pour la visualisation de cellules vivantes dans différents états cellulaires/pathologiques et l'analyse in vitro.
Les particules lentivirales de contrôle LentiBrite RFP de EMD Millipore offrent une fluorescence intense pour permettre l'analyse de cellules vivantes dans des types cellulaires difficiles à transfecter.
http://www.nature.com/app_notes/nmeth/2012/121007/pdf/an8620.pdf
(cliquez ici !)
Découvrez les avantages de nos biocapteurs lentiviraux LentiBrite ! Cliquez ici
Les biocapteurs peuvent être utilisés pour détecter la présence ou l'absence d'une protéine donnée, ainsi que la localisation subcellulaire de cette protéine dans une cellule vivante. Les marqueurs fluorescents sont souvent prisés comme moyen de visualiser la protéine d'intérêt dans une cellule par microscopie à fluorescence ou par capture vidéo par intervalles (time-lapse). Visualiser les cellules vivantes sans les perturber permet aux chercheurs d'observer les conditions cellulaires en temps réel.
Les systèmes du type vecteur lentiviral constituent un outil de recherche populaire qui permet d'introduire des produits génétiques dans les cellules. La transfection lentivirale présente certains avantages par rapport aux méthodes non virales telles que la transfection par voie chimique, notamment une plus grande efficacité de transfection vis-à-vis des cellules en division ou non, une expression stable du transgène sur le long terme, et une faible immunogénicité.
EMD Millipore présente les biocapteurs lentiviraux LentiBrite, une nouvelle gamme de particules lentivirales pré-conditionnées codant pour des protéines importantes et fondamentales de l'autophagie, de l'apoptose et de la structure cellulaire, pour la visualisation de cellules vivantes dans différents états cellulaires/pathologiques et l'analyse in vitro.
- Pré-conditionnés, marqués par fluorescence avec de la GFP et de la RFP
- Transfection plus efficace que les méthodes traditionnelles de transfection par voie chimique et autres méthodes non virales
- Possibilité de transfecter des cellules en division, non en division, et les types de cellules difficiles à transfecter, tels que les cellules primaires ou les cellules souches
- Ne perturbent pas les fonctions cellulaires
Les particules lentivirales de contrôle LentiBrite RFP de EMD Millipore offrent une fluorescence intense pour permettre l'analyse de cellules vivantes dans des types cellulaires difficiles à transfecter.
L'utilisation de protéines fluorescentes codées génétiquement a révolutionné la biologie cellulaire en permettant l'imagerie en temps réel des cellules et des structures subcellulaires. Il existe une large palette de protéines fluorescentes, mais elles ne sont pas toutes adaptées à l'imagerie des cellules vivantes. Le biocapteur lentiviral de contrôle RFP LentiBrite™ de EMD Millipore emploie la TagRFP, une protéine fluorescente rouge (orange) monomérique générée par la RFP de l'anémone de mer Entacmaea quadricolor. Il présente une fluorescence avec des maxima d'excitation et d'émission à 555/584 nm respectivement, et une luminosité près de trois fois supérieure à celle de la mCherry, ce qui en fait l'une des protéines fluorescentes rouges monomériques les plus lumineuses disponibles. Les particules lentivirales de contrôle LentiBrite RFP de EMD Millipore offrent une fluorescence intense pour permettre l'analyse des cellules vivantes dans les types cellulaires difficiles à transfecter.
Application
Microscopie à fluorescence
Imagerie :
(voir la Figure 1 de la fiche technique)
Des cellules HeLa ont été déposées sur une lame à chambre de culture et ont été soumises à une transduction avec des particules lentivirales à une valeur de MOI de 40 pendant 24 heures. Après remplacement du milieu et 48 heures d'incubation supplémentaires, les cellules ont été fixées au formaldéhyde puis montées sur lame. Les images ont été obtenues par microscopie à fluorescence à champ large avec immersion dans l'huile. Le témoin RFP affiche une répartition uniforme de la fluorescence rouge dans les cellules.
Comparaison en immunocytochimie :
(voir la Figure 2 de la fiche technique)
Comme pour la Figure 1 (voir la fiche technique), des cellules U2OS ont été déposées sur une lame compartimentée et ont été soumises à une transduction avec des particules lentivirales à une valeur de MOI de 40 pendant 24 heures. Au bout de 24 heures, le milieu a été remplacé et les cellules ont ensuite été incubées pendant 48 heures supplémentaires.
Types de cellules difficiles à transfecter :
(voir la Figure 3 de la fiche technique)
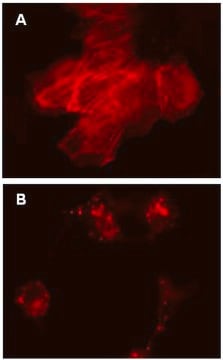
Des cellules primaires du type HUVEC ou HuMSC ont été déposées sur une lame compartimentée, puis ont été soumises à une transduction avec des particules lentivirales avec témoin RFP à une valeur de MOI de 40 pendant 24 heures.
Autres types cellulaires :
(voir la Figure 4 de la fiche technique)
Des cellules primaires de neurones corticaux de rat ont été traitées comme dans la Figure 1 (voir la fiche technique).
Pour une visualisation optimale de la fluorescence et une analyse optimale sur cellules vivantes, il est recommandé d'analyser le niveau d'expression de la cible dans les 24 à 48 heures qui suivent la transfection / l'infection, car l'intensité de la fluorescence peut diminuer au fil du temps, en particulier dans les lignées cellulaires difficiles à transfecter. Les cellules infectées peuvent être congelées après une transfection/infection réussie, puis décongelées et mises en culture de façon à conserver leur expression fluorescente positive au-delà de 24-48 heures. La durée et l'intensité de l'expression fluorescente varient d'une lignée cellulaire à l'autre. Des MOI supérieures peuvent être nécessaires pour les lignées cellulaires difficiles à transfecter.
Imagerie :
(voir la Figure 1 de la fiche technique)
Des cellules HeLa ont été déposées sur une lame à chambre de culture et ont été soumises à une transduction avec des particules lentivirales à une valeur de MOI de 40 pendant 24 heures. Après remplacement du milieu et 48 heures d'incubation supplémentaires, les cellules ont été fixées au formaldéhyde puis montées sur lame. Les images ont été obtenues par microscopie à fluorescence à champ large avec immersion dans l'huile. Le témoin RFP affiche une répartition uniforme de la fluorescence rouge dans les cellules.
Comparaison en immunocytochimie :
(voir la Figure 2 de la fiche technique)
Comme pour la Figure 1 (voir la fiche technique), des cellules U2OS ont été déposées sur une lame compartimentée et ont été soumises à une transduction avec des particules lentivirales à une valeur de MOI de 40 pendant 24 heures. Au bout de 24 heures, le milieu a été remplacé et les cellules ont ensuite été incubées pendant 48 heures supplémentaires.
Types de cellules difficiles à transfecter :
(voir la Figure 3 de la fiche technique)
Des cellules primaires du type HUVEC ou HuMSC ont été déposées sur une lame compartimentée, puis ont été soumises à une transduction avec des particules lentivirales avec témoin RFP à une valeur de MOI de 40 pendant 24 heures.
Autres types cellulaires :
(voir la Figure 4 de la fiche technique)
Des cellules primaires de neurones corticaux de rat ont été traitées comme dans la Figure 1 (voir la fiche technique).
Pour une visualisation optimale de la fluorescence et une analyse optimale sur cellules vivantes, il est recommandé d'analyser le niveau d'expression de la cible dans les 24 à 48 heures qui suivent la transfection / l'infection, car l'intensité de la fluorescence peut diminuer au fil du temps, en particulier dans les lignées cellulaires difficiles à transfecter. Les cellules infectées peuvent être congelées après une transfection/infection réussie, puis décongelées et mises en culture de façon à conserver leur expression fluorescente positive au-delà de 24-48 heures. La durée et l'intensité de l'expression fluorescente varient d'une lignée cellulaire à l'autre. Des MOI supérieures peuvent être nécessaires pour les lignées cellulaires difficiles à transfecter.
Domaine de recherche
Structure cellulaire
Structure cellulaire
Sous-domaine de recherche
Tous
Tous
Composants
Lentivirus TagRFP :
un flacon contenant 25 µl de particules lentivirales correspondant à au moins 3 × 10E8 unités infectieuses (UI) par ml.
Pour connaître le titre spécifique d'un lot, consulter le “}Titre viral” figurant dans les caractéristiques du produit sur la fiche technique.
Promoteur
EF-1 (facteur d'élongation 1)
Multiplicité d'infection (MOI)
MOI = rapport entre le nombre de particules lentivirales infectieuses (UI) et le nombre de cellules infectées.
Les valeurs de MOI permettant d'obtenir une grande efficacité de transduction et un signal de forte intensité pour les neurones se situent généralement dans le plage de 20 à 40. Pour cette cible, certains types cellulaires peuvent nécessiter des valeurs de MOI plus faibles (p. ex. : HT-1080, HeLa, U2OS, cellules souches mésenchymateuses humaines (HuMSC)), tandis que d'autres peuvent nécessiter des valeurs de MOI plus élevées (p. ex. : cellules endothéliales de la veine ombilicale humaine (HUVEC)).
REMARQUE : La valeur de MOI doit être titrée et optimisée par l'utilisateur final pour chaque type de cellule et chaque cible lentivirale, afin d'atteindre l'efficacité de transduction et l'intensité de signal souhaitées.
un flacon contenant 25 µl de particules lentivirales correspondant à au moins 3 × 10E8 unités infectieuses (UI) par ml.
Pour connaître le titre spécifique d'un lot, consulter le “}Titre viral” figurant dans les caractéristiques du produit sur la fiche technique.
Promoteur
EF-1 (facteur d'élongation 1)
Multiplicité d'infection (MOI)
MOI = rapport entre le nombre de particules lentivirales infectieuses (UI) et le nombre de cellules infectées.
Les valeurs de MOI permettant d'obtenir une grande efficacité de transduction et un signal de forte intensité pour les neurones se situent généralement dans le plage de 20 à 40. Pour cette cible, certains types cellulaires peuvent nécessiter des valeurs de MOI plus faibles (p. ex. : HT-1080, HeLa, U2OS, cellules souches mésenchymateuses humaines (HuMSC)), tandis que d'autres peuvent nécessiter des valeurs de MOI plus élevées (p. ex. : cellules endothéliales de la veine ombilicale humaine (HUVEC)).
REMARQUE : La valeur de MOI doit être titrée et optimisée par l'utilisateur final pour chaque type de cellule et chaque cible lentivirale, afin d'atteindre l'efficacité de transduction et l'intensité de signal souhaitées.
Qualité
Évaluée par transduction de cellules HT-1080 et imagerie en fluorescence afin d'estimer l'efficacité de transduction.
Forme physique
Précipitation au PEG
Stockage et stabilité
Manipulation et stockage
Stocké à -80 °C, le lentivirus est stable pendant au moins 4 mois à compter de la date de réception. Après la première décongélation, placer immédiatement sur de la glace et congeler sous forme d'aliquotes de travail à -80 °C. Les aliquotes congelées peuvent être conservées au moins 2 mois. D'autres congélations/décongélations peuvent entraîner une baisse du titre viral et de l'efficacité de transduction.
REMARQUE IMPORTANTE CONCERNANT LA SÉCURITÉ
Les vecteurs lentiviraux à réplication défaillante, tels que le vecteur de 3e génération fourni dans ce produit, ne sont pas connus pour causer des maladies, que ce soit chez l'Homme ou chez l'animal. Cependant, les lentivirus peuvent s'intégrer dans le génome de la cellule hôte, et ainsi présenter un certain risque de mutagenèse par insertion. Ce produit fait partie du groupe de risque de niveau 2 et doit être manipulé dans un laboratoire de niveau de sécurité biologique 2 (LSB2). Une discussion détaillée sur la biosécurité des vecteurs lentiviraux est disponible dans la référence bibliographique suivante : Pauwels, K. et al. (2009). State-of-the-art lentiviral vectors for research use: Risk assessment and biosafety recommendations. Curr. Gene Ther. 9: 459-474
Stocké à -80 °C, le lentivirus est stable pendant au moins 4 mois à compter de la date de réception. Après la première décongélation, placer immédiatement sur de la glace et congeler sous forme d'aliquotes de travail à -80 °C. Les aliquotes congelées peuvent être conservées au moins 2 mois. D'autres congélations/décongélations peuvent entraîner une baisse du titre viral et de l'efficacité de transduction.
REMARQUE IMPORTANTE CONCERNANT LA SÉCURITÉ
Les vecteurs lentiviraux à réplication défaillante, tels que le vecteur de 3e génération fourni dans ce produit, ne sont pas connus pour causer des maladies, que ce soit chez l'Homme ou chez l'animal. Cependant, les lentivirus peuvent s'intégrer dans le génome de la cellule hôte, et ainsi présenter un certain risque de mutagenèse par insertion. Ce produit fait partie du groupe de risque de niveau 2 et doit être manipulé dans un laboratoire de niveau de sécurité biologique 2 (LSB2). Une discussion détaillée sur la biosécurité des vecteurs lentiviraux est disponible dans la référence bibliographique suivante : Pauwels, K. et al. (2009). State-of-the-art lentiviral vectors for research use: Risk assessment and biosafety recommendations. Curr. Gene Ther. 9: 459-474
Informations légales
CHEMICON is a registered trademark of Merck KGaA, Darmstadt, Germany
Code de la classe de stockage
10 - Combustible liquids
Classe de danger pour l'eau (WGK)
WGK 2
Certificats d'analyse (COA)
Recherchez un Certificats d'analyse (COA) en saisissant le numéro de lot du produit. Les numéros de lot figurent sur l'étiquette du produit après les mots "Lot" ou "Batch".
Déjà en possession de ce produit ?
Retrouvez la documentation relative aux produits que vous avez récemment achetés dans la Bibliothèque de documents.
Notre équipe de scientifiques dispose d'une expérience dans tous les secteurs de la recherche, notamment en sciences de la vie, science des matériaux, synthèse chimique, chromatographie, analyse et dans de nombreux autres domaines..
Contacter notre Service technique