F4505
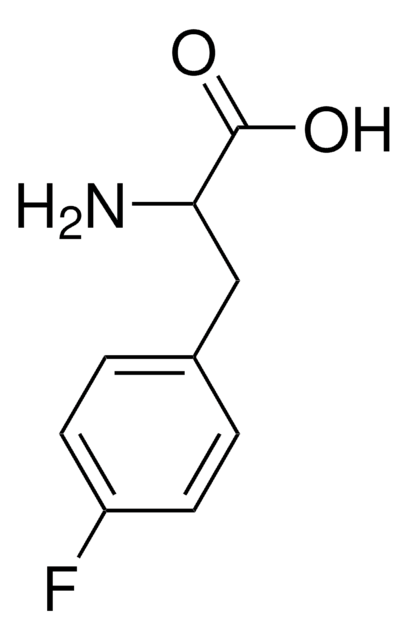
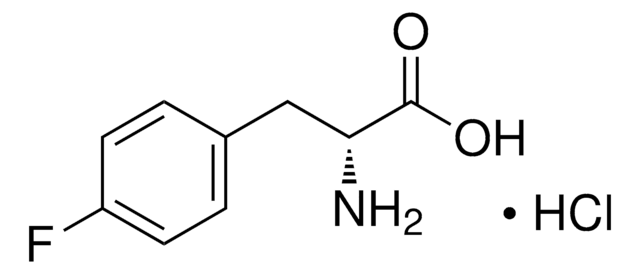
m-Fluoro-DL-tyrosine
≥98%, suitable for ligand binding assays
Sinónimos:
3-fluoro-tyrosine
About This Item
Productos recomendados
Nombre del producto
m-Fluoro-DL-tyrosine,
Ensayo
≥98%
Nivel de calidad
Formulario
powder
técnicas
ligand binding assay: suitable
color
white
mp
280 °C (dec.) (lit.)
temp. de almacenamiento
2-8°C
cadena SMILES
NC(Cc1ccc(O)c(F)c1)C(O)=O
InChI
1S/C9H10FNO3/c10-6-3-5(1-2-8(6)12)4-7(11)9(13)14/h1-3,7,12H,4,11H2,(H,13,14)
Clave InChI
VIIAUOZUUGXERI-UHFFFAOYSA-N
¿Está buscando productos similares? Visita Guía de comparación de productos
Categorías relacionadas
Acciones bioquímicas o fisiológicas
Palabra de señalización
Warning
Frases de peligro
Consejos de prudencia
Clasificaciones de peligro
Acute Tox. 4 Dermal - Acute Tox. 4 Inhalation - Acute Tox. 4 Oral
Código de clase de almacenamiento
11 - Combustible Solids
Clase de riesgo para el agua (WGK)
WGK 3
Punto de inflamabilidad (°F)
Not applicable
Punto de inflamabilidad (°C)
Not applicable
Equipo de protección personal
dust mask type N95 (US), Eyeshields, Gloves
Elija entre una de las versiones más recientes:
¿Ya tiene este producto?
Encuentre la documentación para los productos que ha comprado recientemente en la Biblioteca de documentos.
Nuestro equipo de científicos tiene experiencia en todas las áreas de investigación: Ciencias de la vida, Ciencia de los materiales, Síntesis química, Cromatografía, Analítica y muchas otras.
Póngase en contacto con el Servicio técnico