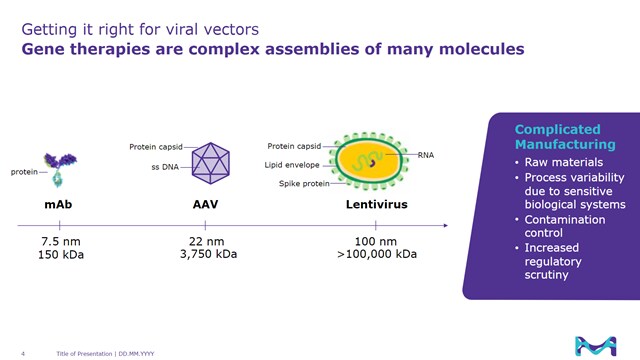
Formulación de vectores víricos, filtración final y llenado

La formulación, la filtración final y el llenado son los últimos pasos en la producción de vectores víricos. Un diseño racional de la formulación desarrollado mediante la optimización de las condiciones de disolución y el empleo de excipientes de gran calidad puede aumentar significativamente la estabilidad del vector vírico y la vida útil. Nuestra amplia gama de disoluciones tampón, sales y estabilizadores de gran calidad, con bajo contenido de biocarga y endotoxinas, se ha desarrollado específicamente para aplicaciones de alto riesgo y puede asegurar un procesamiento último y una formulación satisfactorios de su producto de genoterapia final.
El diseño de un sistema de esterilización por filtración de un solo uso satisfactorio debe centrarse en maximizar la recuperación de esos tratamientos de alto valor y considerar diferentes opciones de filtración, requisitos de proceso, necesidades de muestreo y si se realizarán pruebas de integridad posesterilización (PUPSIT) previas al uso.
Nuestros montajes de un solo uso Mobius® le ofrecen flexibilidad y nuestros especialistas pueden ayudarle a diseñar un montaje personalizado a partir de nuestra amplia gama de filtros y componentes de un solo uso. Estos sistemas son escalables y se pueden replicar fácilmente para satisfacer sus necesidades cambiantes.
Respaldados por nuestro programa Emprove®, nuestros excipientes, filtros y componentes de un solo uso cuentan con una amplia documentación, lo que minimiza los riesgos normativos y asociados a la calidad en su fabricación. Todo esto simplifica la complejidad de la cualificación de su proveedor y acelera los procesos, reduciendo así el coste total de propiedad.
- Una amplia cartera de productos, fabricados de acuerdo con las directrices de GMP del IPEC PQG
- Filtros de calidad esterilizante para la purificación de vectores víricos
- Montajes Mobius® de un solo uso para la purificación de vectores víricos
- Servicios de validación para confirmar que su sistema de filtración de un solo uso es adecuado para el procesamiento
Recursos técnicos relacionados
- Folleto: Su vía rápida a través de los desafíos normativos: el programa Emprove®
Descargue nuestro folleto del programa Emprove® para obtener más información sobre cómo mejorar sus procesos normativos.
- Libro blanco: Identificación de materias primas apropiadas y de calidad en un entorno normativo en evolución
Este informe técnico explica los desafíos y las claves del éxito en los procesos de fabricación farmacéutica y las cadenas de suministro de materias primas cuando se trata de obtener materias primas en un entorno normativo en continua evolución.
- Folleto: Materias primas y materiales iniciales Pharma: satisfaga sus requisitos normativos
Acelere con confianza su paso por el laberinto normativo y el lanzamiento rápido de su nuevo fármaco al mercado.
- Folleto: Filtros y componentes de un solo uso Emprove®
Permitir una evaluación de riesgos más sólida.
Procedimiento de trabajo


Procesado inicial de vectores víricos
Tomar las decisiones correctas en los procesos upstream no sólo afecta a la concentración del vector vírico, sino también a los procesos downstream, los plazos y la aceptación normativa

Procesado final de vectores víricos
Procesos eficientes de purificación de los virus pueden mejorar el rendimiento, reducir el tiempo hasta el paciente y reducir los costes de fabricación

Caracterización de vectores víricos y ensayos de bioseguridad
Las pruebas de bioseguridad cruciales y la caracterización de los vectores víricos producidos pueden contribuir a analizar por completo los atributos de calidad fundamentales: identidad, potencia, seguridad y estabilidad

Desarrollo y fabricación por contrato de viroterapias
Las asociaciones para CDMO (desarrollo y fabricación por contrato) desempeñan un papel fundamental en el avance de los productos clínicos en fase de desarrollo y en la consecución de una comercialización satisfactoria
Para seguir leyendo, inicie sesión o cree una cuenta.
¿No tiene una cuenta?