03449
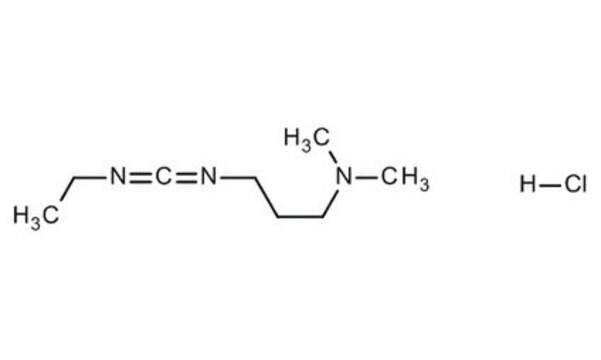
N-(3-Dimethylaminopropyl)-N′-ethylcarbodiimid -hydrochlorid
≥99.0% (AT)
Synonym(e):
N-Ethyl-N′-(3-dimethylaminopropyl)-carbodiimid -hydrochlorid, EDAC, EDC, WSC -hydrochlorid
About This Item
Empfohlene Produkte
Qualitätsniveau
Assay
≥99.0% (AT)
Form
powder
Methode(n)
bioconjugation: suitable
mp (Schmelzpunkt)
110-115 °C (lit.)
112-116 °C
Löslichkeit
H2O: soluble 0.2 g/L
Lagertemp.
−20°C
SMILES String
Cl.CCN=C=NCCCN(C)C
InChI
1S/C8H17N3.ClH/c1-4-9-8-10-6-5-7-11(2)3;/h4-7H2,1-3H3;1H
InChIKey
FPQQSJJWHUJYPU-UHFFFAOYSA-N
Suchen Sie nach ähnlichen Produkten? Aufrufen Leitfaden zum Produktvergleich
Allgemeine Beschreibung
Zudem fungiert EDAC-HCl als Brücke für Biomoleküle, indem es als Crosslinker fungiert, der aminreaktive NHS-Ester aus Biomolekülen mit Carboxylgruppen verbindet. Diese Technik erweist sich als wertvoll bei der Proteinkonjugation und ermöglicht die Erzeugung von Hybridmolekülen mit neuartigen Eigenschaften und Funktionen. Der zugrunde liegende Mechanismus umfasst die Reaktion von EDAC-HCl mit einer Carboxylgruppe, die ein instabiles Zwischenprodukt bildet, das aktiv einen Aminpartner sucht. Das empfindliche Gleichgewicht dieser Reaktion unterstreicht die Bedeutung der Optimierung von Bedingungen für eine effiziente Konjugation. Durch die Unterstützung von N-Hydroxysuccinimid (NHS) werden die Fähigkeiten von EDAC-HCl weiter verbessert, das Zwischenprodukt zu stabilisieren und Konjugationsverfahren in zwei Schritten zu ermöglichen. Diese zusätzliche Funktion bietet eine größere Flexibilität und Kontrolle, insbesondere bei komplexen Biomolekülen.
Anwendung
Biochem./physiol. Wirkung
Leistungsmerkmale und Vorteile
Sonstige Hinweise
Vergleichbares Produkt
Signalwort
Danger
Gefahreneinstufungen
Acute Tox. 3 Dermal - Acute Tox. 4 Oral - Aquatic Acute 1 - Aquatic Chronic 1 - Skin Irrit. 2 - Skin Sens. 1 - STOT RE 2 Oral
Zielorgane
Stomach,large intestine,lymph node
Lagerklassenschlüssel
6.1C - Combustible acute toxic Cat.3 / toxic compounds or compounds which causing chronic effects
WGK
WGK 3
Flammpunkt (°F)
Not applicable
Flammpunkt (°C)
Not applicable
Persönliche Schutzausrüstung
dust mask type N95 (US), Eyeshields, Gloves
Analysenzertifikate (COA)
Suchen Sie nach Analysenzertifikate (COA), indem Sie die Lot-/Chargennummer des Produkts eingeben. Lot- und Chargennummern sind auf dem Produktetikett hinter den Wörtern ‘Lot’ oder ‘Batch’ (Lot oder Charge) zu finden.
Besitzen Sie dieses Produkt bereits?
In der Dokumentenbibliothek finden Sie die Dokumentation zu den Produkten, die Sie kürzlich erworben haben.
Kunden haben sich ebenfalls angesehen
Unser Team von Wissenschaftlern verfügt über Erfahrung in allen Forschungsbereichen einschließlich Life Science, Materialwissenschaften, chemischer Synthese, Chromatographie, Analytik und vielen mehr..
Setzen Sie sich mit dem technischen Dienst in Verbindung.








![1-[3-(Dimethylamino)propyl]-3-ethylcarbodiimidmethiodid](/deepweb/assets/sigmaaldrich/product/structures/414/134/4eb9c126-d7f9-4e12-9e3a-95cb077824fd/640/4eb9c126-d7f9-4e12-9e3a-95cb077824fd.png)



