高盐裂解配合耐高盐核酸内切酶优化AAV生产工艺
腺相关病毒(AAV)载体生产工艺的中游是细胞裂解和核酸酶消化的结合步骤。该步骤先用去垢剂破坏细胞的脂双层并释放载体病毒,再用核酸内切酶消化宿主细胞DNA和残余质粒,以确保患者安全性并提高下游工艺效率。根据美国FDA 2020年的《基因治疗新药临床试验申请指南》(Guidance for Gene Therapy Investigational New Drug Applications),残留DNA需少于10 ng/dose,片段大小需小于约200碱基对。
本文梳理了细胞裂解的关键考虑因素,并进一步介绍了如何结合高盐条件和耐高盐核酸内切酶来提高病毒载体的滴度和感染性。
细胞裂解考虑因素
细胞裂解听上去是不是很简单?但它在实际操作上却会遭遇多个难题。首先裂解常用的去垢剂,比如TRITON™ X-100(聚乙二醇辛基苯基醚),本身就是个问题。从2021年1月起,欧盟委员会开始禁止名列《化学品注册、评估、许可和限制法规》(REACH)清单的TRITON™ X-100在欧盟的未授权使用。TRITON™ X-100被列入清单并受到欧盟严格使用限制是因为它的降解产物会引起内分泌和基因变化,对患者和环境有害。
选择去垢剂时,还要注意它不能破坏病毒颗粒及其感染性,也不能干扰下游工艺,比如聚山梨酯就有这个问题。另外,还要方便后续工艺对去垢剂的清除和检测。
最后,务必要了解盐浓度对细胞裂解和载体产量的影响。过去,用来释放AAV衣壳的裂解缓冲液使用生理盐浓度(150mM NaCl)。但最近有文献报道,盐浓度增至500mM后,可增加病毒颗粒和感染滴度,并减少AAV聚集。然而,之前说过,在AAV载体生产流程中高盐环境会影响用于DNA消化的传统内切核酸酶活性。
中游步骤中高盐度对AAV产量的影响
通过研究定量分析了细胞裂解时盐度增加对最终产量的影响。使用HEK293细胞生产AAV5载体,分别用TRITON™ X-100、聚山梨酯20、Deviron® C16或Deviron® 13-S9裂解细胞。将使用150mM NaCl+聚山梨酯20的裂解缓冲液生产的衣壳量设为基线。使用500mM盐浓度的裂解缓冲液后,AAV5衣壳滴度平均提高29%(图1)。

图 1.高盐裂解对AAV5滴度的影响。
中游步骤中高盐度对AAV感染性的影响
通过类似研究检测了500mM NaCl对AAV感染性的影响。用HEK293细胞生产AAV2载体。基线使用的裂解缓冲液是150mM NaCl和聚山梨酯20。盐浓度提升至500mM后,无论使用哪种去垢剂,感染性都至少提高10倍(图2)。上面提过,高盐裂解还会减少AAV聚集。
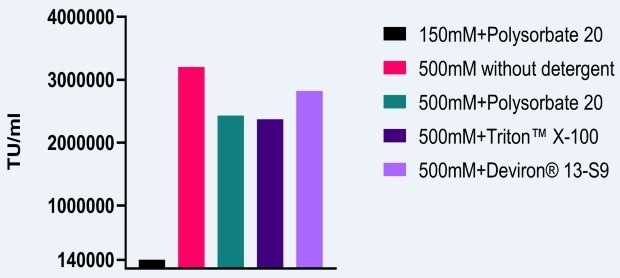
图 2.高盐裂解对AAV5感染性的影响。
DNA消化考虑因素
紧随细胞裂解的DNA消化同样面临多项挑战。最重要的一项是要采购质量符合监管要求的材料,并确保供应链稳健。除了GMP要求,还要考虑材料酶的纯度、糖基化水平和微生物负荷。酶对高盐度的耐受性也是一个关键因素,否则会导致AAV生产时无法应用高盐条件。
AAV生产用酶的选择要素
- IPEC PQG GMP级或同等级别,FDA DMF/BBMF
- >99%纯品
- 无翻译后修饰
- 支原体检测
- 外源病毒检测
- 内毒素检测
- 提供测试小样(Tailgate sample)
- 强大物流和稳健供应
- 提供申报相关问题的技术支持
- 精准的检测方法
DNA消化用酶还需要能被下游工艺有效去除,还要考虑其发挥活性适合的盐浓度范围。尽管使用高盐条件能提高载体产量,但在这种高离子强度下,传统的核酸内切酶将不能与DNA相互作用从而消化核酸。也就是说,传统做法需要对高盐条件和核酸酶活性进行权衡取舍。
AAV载体生产用耐高盐核酸内切酶开发
为了在高盐细胞裂解后核酸内切酶能有效发挥活性,我们利用先进的蛋白工程技术开发了耐高盐的Benzonase®核酸内切酶。这款核酸内切酶无动物源成分,可在高达1000mM的盐浓度下消化DNA和RNA,为IPEC PQG GMP级和Emprove® Expert级产品。
Benzonase®耐高盐核酸内切酶通过细菌表达系统生产,确保其分子大小一致,无翻译后修饰,并且具有高度的批次间重复性。下列数据证明了Benzonase®耐高盐核酸内切酶的活性和优点。
蛋白性质
Benzonase®耐高盐核酸内切酶通过细菌表达系统生产,确保其分子大小一致,无翻译后修饰,并且具有高度的批次间重复性。这款高度均一的酶蛋白可通过ELISA等免疫分析法准确鉴定,与通过酵母表达的高度糖基化、批次间翻译后修饰差异极大的酶形成鲜明对比。

图 3.还原性SDS-PAGE下,Benzonase®耐高盐核酸内切酶和竞品A的一致性和纯度对比。

图 4.非还原性SDS-PAGE下,Benzonase®耐高盐核酸内切酶和竞品A的一致性和纯度对比。
Benzonase®耐高盐核酸内切酶(Emprove® Expert级)通过大肠杆菌生产,因而:
- 蛋白纯净
- 无翻译后修饰
- 批次间高度一致
图3和4的结论说明,Benzonase®耐高盐核酸内切酶(Emprove® Expert级)的分子量高度一致。一般的耐高盐核酸内切酶(竞品A)没有做到这一点。
核酸内切酶活性
核酸内切酶活性依赖于镁离子。图5对比了不同镁离子浓度下的Benzonase®耐高盐核酸内切酶和非耐高盐核酸内切酶活性。Benzonase®耐高盐核酸内切酶(STB)在高盐条件下活性更强,500mM盐度下,在1-10mM Mg2+范围内活性始终稳定。图6表明,10mM Mg2+时,在150mM和500mM盐度下,Benzonase®耐高盐核酸内切酶的活性与标准核酸酶类似。
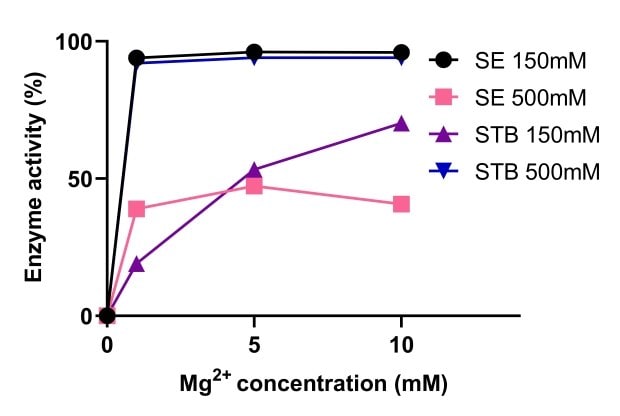
图 5.Benzonase®耐高盐核酸内切酶和非耐高盐核酸内切酶的活性对比。
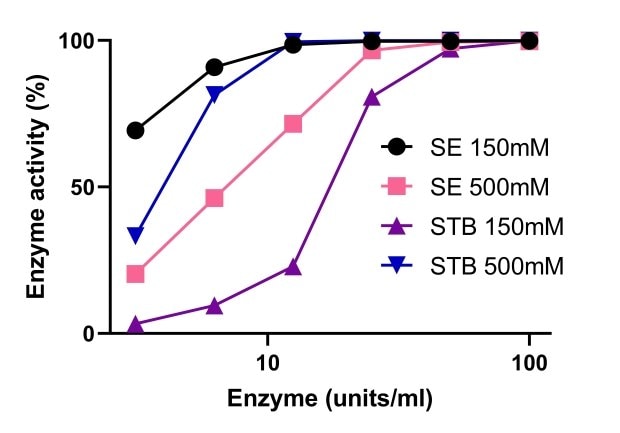
图 6.Benzonase®耐高盐核酸内切酶和非耐高盐核酸内切酶的活性对比。
如图7所示,在500mM和1M NaCl下,用Benzonase®耐高盐核酸内切酶与其他市售盐活性和盐失活核酸内切酶消化DNA(37 °C、1小时)。结果Benzonase®耐高盐核酸内切酶在500mM和1M盐度下均能完全消化DNA,相比其他核酸内切酶,性能相近或更加优越。

图 7.Benzonase®耐高盐核酸内切酶与其他市售盐活性和盐失活核酸内切酶对DNA消化(37 °C、1小时)情况对比。
图例
M – DNA低分子量标准品,GeneRuler Ultra Low Range DNA Ladder,货号SM1213
Comp A ** – 盐活性核酸内切酶竞品
SE – 标准核酸内切酶,货号103773
STB – Benzonase®耐高盐核酸内切酶(Emprove® Expert级)
核酸片段大小
Benzonase®耐高盐核酸内切酶将DNA消化至10 bp以下、无检出的水平。图8为使用低分子量DNA标准品,在4%琼脂糖凝胶上跑胶的DNA片段。150mM盐度时,未充分消化DNA,500mM盐度时,消化后无DNA片段残留。

图 8.在37°C、30分钟条件下,DNA经Benzonase®耐高盐核酸内切酶(25U/ml)消化后的片段大小。
AAV载体生产中Benzonase®耐高盐核酸内切酶与去垢剂的相容性
研究与4种细胞裂解去垢剂共用时,Benzonase®耐高盐核酸内切酶的活性影响:TRITON™ X-100、聚山梨酯20,以及因TRITON™ X-100禁用而开发的两种替代品Deviron® C16和13-S9。如图9所示,Benzonase®耐高盐核酸内切酶的活性不受任意一种去垢剂影响。在TRITON™ X-100、聚山梨酯20和Deviron® 13-S9 (7B)存在下,DNA在500mM NaCl裂解缓冲液中被完全消化。
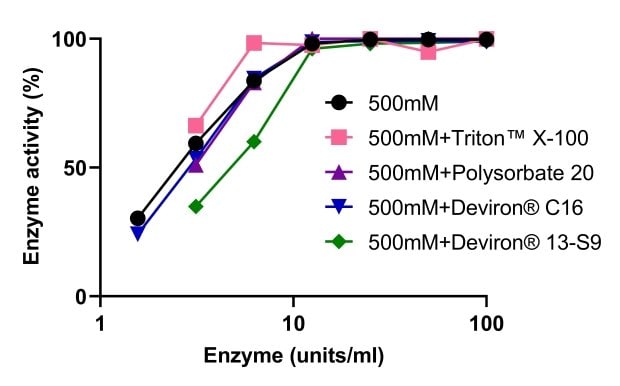
图 9.与不同去垢剂共用时的Benzonase®耐高盐核酸内切酶活性变化。

图 10.与不同去垢剂共用时,Benzonase®耐高盐核酸内切酶对DNA的消化情况。
根据应用选择最适宜的Benzonase®
Benzonase® 耐高盐核酸内切酶适合用于盐浓度大于等于200mM的应用。在500mM盐度时,DNA会被完全消化,如上所述,这种条件下AAV滴度可增加29%,感染性提高近2,000%。在该中游步骤使用高盐条件,还可防止AAV聚集并有效去除病毒衣壳的DNA,提高患者安全性。Benzonase®耐高盐核酸内切酶的无翻译后修饰使蛋白无糖基化且易于检测,适合用于制药生产。
对于盐浓度低于200mM的应用,则应选用Benzonase® Safety Plus(加强安全型)标准核酸内切酶。
表3归纳总结了我们3种GMP级Benzonase®核酸内切酶的性能参数。Benzonase®耐高盐核酸内切酶属于我们的Emprove®计划产品。这项计划帮助药企在从开发转向生产时将颠覆性活动减至最低,并能实行全面的风险评估。该计划提供按照行业领先标准严格检验的原材料和起始材料。这些材料均附带全面的文档包,满足药企原料检验、风险评估和生产优化时的各种资料需要。
Benzonase®常见问题解答
定义
什么是Benzonase®核酸内切酶?
Benzonase®核酸内切酶是Merck拥有的核酸内切酶品牌,适合研究和生物工艺用途。
该品牌有哪些酶?
Benzonase®核酸内切酶系列目前有两种酶。
- 经典Benzonase®核酸内切酶产品线。例如Benzonase® Safety Plus核酸内切酶,来自粘质沙雷菌, 并通过大肠杆菌K12 W3110菌株重组生产。蛋白分子量30 kDa,等电点(PI)6.85。
- 新型Benzonase®耐高盐核酸内切酶(1.4445)。一流蛋白工程技术制造,确保高盐条件下酶活性最高。
蛋白为单体形式,分子量约27 kDa,等电点(PI)9.68。这篇常见问题解答有专门章节介绍这款酶。
作用机制
Benzonase® 核酸酶适用于哪些核酸类型?分离 RNA 时可以使用吗?
Benzonase®核酸酶是一种广谱核酸内切酶,可攻击并降解所有形式的DNA和RNA(单链、双链、线形或环形)。
Benzonase®核酸酶完全降解核酸的最终结果是什么?
Benzonase®核酸酶将核酸完全酶解成长度2-5个碱基的5'-单磷酸末端寡核苷酸。
抑制与去除
Benzonase®核酸酶如何灭活?如何去除?
使用 EDTA 螯合必需金属离子可以实现可逆抑制。不可逆失活仅可在极端条件下完成(100 mM NaOH,70 °C,30 分钟)。可通过层析法从目标产物中分离Benzonase核酸酶。但这种核酸内切酶较为稳健——如果需要无核酸酶的终产物,我们不建议使用Benzonase。
Benzonase®核酸内切酶的使用条件?抑制因素有哪些?
Benzonase®核酸内切酶的应用条件广泛(参见酶特性章节),但是1–2 mM的Mg2+是保证Benzonase®核酸内切酶活性的必要条件。
虽然Mg2+可用Mn2+替代,但是最佳活性还是依靠Mg2+。含有以下物质时,核酸酶的活性会降低约50%:> 300 mM一价阳离子,>100 mM磷酸盐,>100 mM硫酸铵。此外,> 1 mM EDTA也会抑制Benzonase®核酸内切酶活性。
为什么我的酶失活了?
Benzonase®核酸内切酶性能通常十分稳定,但在极个别情况下也会失活。不可逆失活可能是因为样品中存在变性剂(如蛋白酶),也可能是保存不当造成的。可逆失活通常是因为存在螯合剂(如EDTA),反应去除了必需的镁离子。
在生物工艺中,要如何去除Benzonase®核酸内切酶?
Benzonase®核酸内切酶可通过多种下游处理技术去除,包括深层过滤(澄清)、切向流过滤(浓缩和洗滤)和层析(IEX、SEC、HIC)。详情可参阅附录章节二《去除Benzonase® 核酸内切酶》(36页)。
稳定性和使用条件
我的Benzonase®核酸内切酶忘在实验台上了,它还能用吗?
我们对Benzonase®核酸内切酶进行了广泛的稳定性测试,发现它非常稳定。即使在37 °C条件下长时间孵育,Benzonase®核酸内切酶仍能在数月内保持> 90%的活性。
我想使用其它缓冲液。Benzonase® 核酸内切酶发挥完整活性需要满足哪些条件?哪些因素会导致其活性下降?
Benzonase®核酸内切酶需要1‒2 mM的Mg2+才能发挥活性。在单价阳离子浓度 >50%、磷酸盐浓度 >20 mM 和硫酸铵浓度 >25 mM 的情况下,Benzonase 活性会受到抑制(维持大约 50% 的活性)
低温使用时,需要多加多少Benzonase®核酸内切酶?
Benzonase®核酸内切酶发挥活性需要1‒2 mM的Mg2+。在单价阳离子浓度 >50%、磷酸盐浓度 >20 mM 和硫酸铵浓度 >25 mM 的情况下,Benzonase 活性会受到抑制(维持大约 50% 的活性)
蛋白质提取应用
Benzonase®核酸内切酶与蛋白酶抑制剂复合物兼容吗?
兼容。但仍需谨慎行事,毕竟许多蛋白酶抑制剂混合物都含 EDTA。1 mM以上的EDTA会抑制Benzonase®核酸内切酶活性。
我的蛋白质不溶,需要在变性条件下进行纯化。Benzonase®核酸内切酶能在尿素环境消化核酸吗?
实际上,当尿素浓度未达到6 M时,Benzonase®核酸内切酶活性会增加。尿素为6 M时,酶活性首先增加,然后随着时间的推移逐渐下降。尿素达到7 M时,Benzonase®核酸内切酶在15分钟后变性,并且失去活性。但在核酸酶失活之前,核酸会先明显降解。提高Benzonase®核酸内切酶初始浓度可部分补偿7 M尿素的影响。
Benzonase®核酸内切酶为什么具有那么多的选型?HC 代表什么? 90% 与 99% 纯度各有何影响?
为满足尽可能广泛的工艺和成本要求,Benzonase®核酸内切酶提供两种纯度等级:I 级(>99% 纯度)和 II 级(>90% 纯度)。两个纯度级均以 25 U/μL 或高浓度 (HC)(定义为 250 U/μL)形式提供。如需批量购买,请联系定制服务部门。
如需了解Benzonase®所有产品及其区别,请访问我们的核酸内切酶页面(https://www.sigmaaldrich.cn/CN/zh/products/pharma-and-biopharma-manufacturing/bioprocessing-formulation-raw-materials/endonuclease)。
Benzonase®核酸内切酶完全降解核酸的最终结果是什么?
Benzonase®核酸内切酶将核酸完全酶解成长度2-5个碱基的5'-单磷酸末端寡核苷酸。
生物工艺应用
实际使用时,该如何确定适合的Benzonase®核酸内切酶品质和用量?
有好几个参数都会影响Benzonase®核酸内切酶的活性。因此,不同工艺中酶的最佳使用条件并不相同,需要实验测定。用于降低粘度时,II级纯度(≥ 90%)的Benzonase®核酸内切酶足以。在标准分析条件下,1单位的Benzonase®核酸内切酶约相当于在30分钟内完全消化37 µg DNA的用量。
我应该在工艺流程中的哪个步骤中加入Benzonase®核酸内切酶?
答案不是唯一的,具体要看你需要拿Benzonase®核酸内切酶做什么。希望它的应用实例会有所帮助。不过,一般来说,最好在培养后捕获前加入Benzonase®核酸内切酶。
Benzonase®核酸内切酶是否安全?
是的,Benzonase®核酸内切酶已通过毒理学检验(可提供内部报告)。对小鼠和大鼠进行一次接触的全身毒性试验,即使极高剂量也未造成毒性损害。此外,极高剂量的Benzonase®核酸内切酶静脉注射小鼠也没有出现基因诱变现象。
5百万单位(U)的管子为什么没有标示体积?
不同批次的Benzonase®核酸内切酶活性(U/mL)不尽相同,因此我们只标明每管产品的单位酶量(U),不标示体积。通过质检报告(CoA)上的活性信息可轻松计算每管体积。
Benzonase®耐高盐核酸内切酶
与其他经典的Benzonase®产品相比,比如Benzonase® Safety Plus,序列相近吗?
Benzonase®耐高盐核酸内切酶是由一流蛋白工程技术制造,确保高盐条件下酶活性最高的全新核酸酶。与其他经典Benzonase®酶相比,氨基酸序列并不相同。
与Benzonase®经典产品相比,使用条件有何区别?
作为核酸内切酶,Benzonase®耐高盐核酸内切酶的使用条件和Benzonase®经典产品一致。除了单价阳离子浓度,建议不要低于300mM NaCl。
如何灭活?
加入EDTA或加热均可灭活。
如何去除?
参见上述“在生物工艺中,要如何去除Benzonase®核酸内切酶?”问答。
如何检测微量酶?
我们为经典Benzonase®酶提供专用的Elisa检测试剂盒,可用于稳健检测Benzonase®耐高盐核酸内切酶。
为什么我要使用这款酶,而不是其他标准核酸酶?
市面上所有适合生物工艺的标准核酸酶,它们的氨基酸序列其实都差不多。这代表它们在高盐条件下的核酸消化能力也差不多,并非最佳选择。
它们适合的单价阳离子浓度范围是0-200mM,与生物工艺中的生理盐浓度相近。
同时,在HEK细胞裂解中使用高于生理盐浓度的高盐环境确实能提高最终工艺产量,500mM NaCl的AAV感染性和回收率远高于150mM盐。
而在这些高盐条件下只有使用耐高盐的核酸酶才能去除核酸。
在>200mM盐度下,我能使用普通的核酸酶吗?
高于生理盐浓度下,普通核酸酶的活性会大幅降低,需要增加用量并且后续纯化麻烦。导致工艺的使用成本增加,效益减少。因此最好还是使用耐高盐核酸酶。
能用其他供应商的检测试剂盒检测Benzonase®耐高盐核酸内切酶吗?比如,像其他“盐活性”核酸酶专用的试剂盒一样吗?
Benzonase® 耐高盐核酸内切酶是全新的改造酶,除了我们自己的检测试剂盒,市场上其他试剂盒都不能用来检测。
注意:市面上所有非Merck官方渠道售卖且没有标示“Benzonase®”品牌名的产品,均应视为假冒伪劣产品。
为什么表达宿主对于酶生产这么重要?
蛋白表达可通过多个生产平台实现。最常用的是酵母和细菌表达平台。但不同平台的蛋白产物及翻译后修饰都不相同。
酵母表达蛋白的高度糖基化和修饰在使用时会带来各种问题,例如抗体法检测准确度低。
市面上主要的盐活性核酸内切酶就是用酵母表达的。
为什么核酸酶的翻译后修饰会影响检测的准确和效率?
糖基化蛋白的性质不均(如图2所示),不同批次产品性质不同。标准的免疫法检测中,用来检测目标蛋白的抗体无法覆盖酵母表达系统带来的全部修饰,导致抗体检测法(如ELISA试剂盒)的准确率不高。
这款酶的毒理学性质如何?
Benzonase®耐高盐核酸内切酶的毒理学性质与其他Benzonase®产品一致。
能根据我的工艺,帮我选择最经济的一款核酸酶吗?要同时考虑总体工艺效率和产量。
我们有一整套的核酸酶可以满足您的各种监管和工艺条件要求。无任欢迎您就工艺开发问题咨询我们的MSAT(生产科技)支持团队。我们的专家覆盖从上游到最终灌装的一整条生产线。
Deviron®常见问题解答
如果我不在欧洲,能继续使用TRITON™ X-100吗?
TRITON™ X-100限用令是ECHA1根据REACH2法规颁布的。主要原因是这种产品具有危害人类健康和环境的高毒性。因此,禁止生物工艺使用该产品是行业大势。非欧盟监管机构同样会评估产品的使用性,未来会颁布类似的禁令。
为什么生物制造不能使用研究级别的去垢剂?
一般来说,去垢剂是通过连续的有机化学反应大批量生产的。为了降低成本,通常使用品质较差的原料。导致终产物(如,二噁英或亚硝胺)含有极度危险的有害杂质。研究级的去垢剂只能用于清洁用途,绝对不能用于药物制剂。
在工艺中改用Deviron®有哪些重要措施?
Deviron®系列有3批GMP EXCiPACT认证产品。可先索取这些批次的样品用于验证。产品附带的Emprove®档案包含向监管机构申报需要的所有资料。毒理学资料同样可方便获取。
我想试试Deviron®,但是没有经验,怎么办?
我们的生物制造专家团队可为您提供应用相关支持,指导您的试用。欢迎与您的默克联系人联系获得免费支持。
产品等级中,MQ400/Emprove® Evolve和MQ500/Emprove® Expert (GMP)有什么差别?
为了监管申报方便,我们建立了不同产品等级的文件和质量计划,您可按应用量身选择适合的产品。欢迎点击链接了解Emprove®和M-Clarity®计划详情。Deviron® C16 Emprove® Evolve和Deviron® 13-S9 Emprove® Expert是我们提供的最高质量等级的产品。
各种应用中,产品的使用浓度是多少?
对于病毒灭活,TRITON™ X-100的ASTM3 E3042-16标准目前依然是单克隆抗体生产的首选文件。行业应用的浓度范围在0,5和1%之间,具体视应用而定。
对于细胞裂解,应用的浓度范围广泛,不同工艺各不相同。建议在工艺开发期间同时试验多个浓度。Deviron®去污剂的效率至少可媲美TRITON™ X-100或聚山梨酯。
可以开发GMP级的Deviron®检测方法吗?
我们的研发团队已经开发了可以转移给客户的Deviron®系列检测方法。不过,GMP级检测方法的开发首选还是我们的Bioreliance®实验室。如有任何疑问,请随时与我们联系。
在细胞裂解中,Deviron®系列是否与Benzonase®兼容?
Benzonase®是AAV4生产中DNA消化的金标准。Deviron®系列专门开发以全面适配Benzonase®核酸内切酶。这两个系列产品联用时不会有任何的酶活性或去垢剂性能损失。应用数据参见Deviron®系列的产品手册。
Deviron®系列的产能有多少?
Deviron®系列在我们的德国达姆施塔特基地制造,每年产出超过100吨产品。如您有任何意向,请尽早与我们联系以便商议交货期。
1欧洲化学品管理局
2《化学品注册、评估、许可和限制法规》*
3美国标准试验方法
4腺相关病毒
TRITON是陶氏化学(“Dow”)或其附属公司的商标,获得许可使用。
参考文献
我们尽最大努力向我们的客户提供就我们所知的资料和建议,但是不承担任何义务或责任。任何情况下,客户均须遵守现行法律和法规。该规定在第三方的任何权利方面同样适用。我们提供的资料和建议并不免除我们的客户检查我们的产品是否适合预期用途的责任。
如要继续阅读,请登录或创建帐户。
暂无帐户?