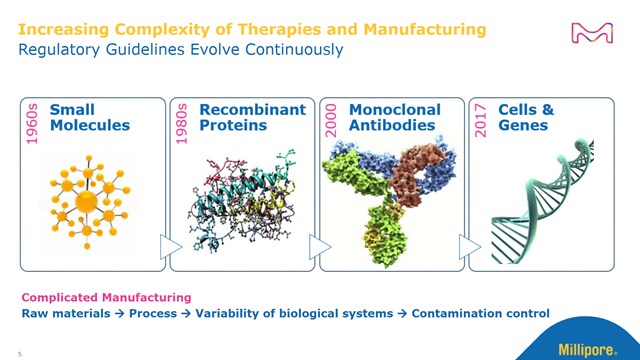
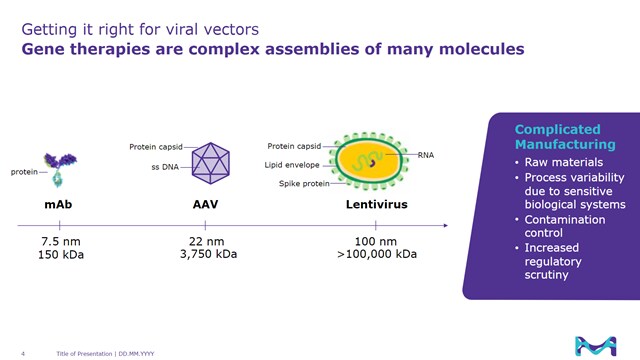
Formulation de vecteurs viraux, et filtration et remplissage finaux

La formulation, la filtration finale et le remplissage final sont les trois dernières étapes de la production de vecteurs viraux. Une conception rationnelle de la formulation, développée en optimisant les conditions de la solution et les excipients de haute qualité, peut augmenter de manière significative la stabilité et la durée de conservation des vecteurs viraux. Notre large gamme de tampons, de sels et de stabilisateurs de haute qualité, à faible teneur en biocharge et en endotoxines, est spécialement conçue pour les applications à haut risque et peut garantir le succès du downstream processing et de la formulation de votre produit de thérapie génique final.
Concevoir un système de filtration stérilisante à usage unique efficace nécessite de mettre l'accent sur une récupération maximal de ces thérapies à forte valeur ajoutée et d'envisager différentes options de filtres et de prendre en compte les exigences du procédé, les besoins en matière d'échantillonnage et la nécessité ou non de réaliser un test d'intégrité après stérilisation/avant utilisation (PUPSIT pour "Pre-Use Post-Sterilization Integrity Testing").
Nos ensembles à usage unique Mobius® vous offrent une grande souplesse d'utilisation et nos spécialistes peuvent vous aider à concevoir un ensemble sur mesure à partir de notre offre étendue de filtres et de composants à usage unique. Ces systèmes sont transposables à l'échelle supérieure et peuvent être facilement répliqués pour répondre à l'évolution de vos besoins.
Pris en charge par notre programme Emprove®, nos excipients, filtres et composants à usage unique incluent une documentation complète, minimisant les risques réglementaires et les risques liés à la qualité lors de la production. Tout cela simplifie la complexité de la qualification des fournisseurs et accélère les procédés, réduisant ainsi le coût total de possession.
- Une large gamme d'excipients fabriqués conformément au Guide des bonnes pratiques de fabrication des excipients à usage pharmaceutique publié conjointement par l'IPEC et le PQG.
- Filtres de grade stérilisant pour la purification des vecteurs viraux
- Ensembles à usage unique Mobius® pour la purification des vecteurs viraux
- Services de validation pour confirmer que votre système de filtration à usage unique est adapté au traitement
Documentation technique apparentée
- Brochure : Your Fast Track Through Regulatory Challenges – The Emprove® Program
Téléchargez notre brochure sur le programme Emprove® pour en savoir plus sur la manière d'améliorer vos procédures réglementaires.
- Livre blanc : Identifying Appropriate-Quality Raw Materials in an Evolving Regulatory Environment
Ce livre blanc explique les défis et les clés de la réussite des procédés de fabrication pharmaceutique et des chaînes d'approvisionnement en matières premières lorsqu'il s'agit de sourcer des matières premières dans un environnement réglementaire en constante évolution.
- Brochure : Pharma Raw and Starting Materials - Satisfy Your Regulatory Requirements
Accélérez votre parcours réglementaire et la mise sur le marché de votre produit en toute confiance.
- Brochure : Filtres et composants à usage unique Emprove®
Enabling a More Robust Risk Assessment.
Workflow


Upstream processing de vecteurs viraux
Prendre les bonnes décisions pour les procédés en amont (upstream processing) se répercute non seulement sur le titre en vecteur viral, mais aussi sur les procédés en aval (downstream processing), les délais et l'homologation

Downstream processing de vecteurs viraux
Des procédés de purification virale efficaces peuvent améliorer le rendement, réduire les délais de mise à disposition au patient et diminuer les coûts de production

Caractérisation de vecteurs viraux et contrôles de biosécurité
La caractérisation des vecteurs viraux et les contrôles de biosécurité essentiels permettent d'effectuer une analyse complète des principaux attributs de qualité : identité, puissance, sécurité et stabilité

Développement et fabrication en sous-traitance de vecteurs viraux
Les partenariats noués avec les CDMO jouent un rôle clé dans la progression des pipelines cliniques et la réussite des mises sur le marché
Pour continuer à lire, veuillez vous connecter à votre compte ou en créer un.
Vous n'avez pas de compte ?