216143
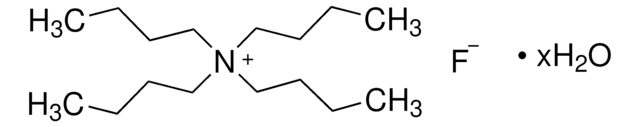
Fluorure de tétrabutylammonium solution
1.0 M in THF
Synonyme(s) :
TBAF solution
About This Item
Produits recommandés
Forme
liquid
Niveau de qualité
Concentration
1.0 M in THF
Impuretés
~5 wt. % water
Densité
0.903 g/mL at 25 °C
Température de stockage
2-8°C
Chaîne SMILES
[F-].CCCC[N+](CCCC)(CCCC)CCCC
InChI
1S/C16H36N.FH/c1-5-9-13-17(14-10-6-2,15-11-7-3)16-12-8-4;/h5-16H2,1-4H3;1H/q+1;/p-1
Clé InChI
FPGGTKZVZWFYPV-UHFFFAOYSA-M
Vous recherchez des produits similaires ? Visite Guide de comparaison des produits
Application
- déprotection des groupements silyle et N-sulfonyle
- réactions de fluoration
- synthèse d'indoles substitués en position 2 par la cyclisation de plusieurs 2-ethynylanilines avec des alcynes terminaux en présence d'un catalyseur au palladium ; ou comme activateur dans la synthèse d'alcynes arylés ou alcénylés par le couplage d'halogénures d'aryle et d'alcényle avec des alcynes terminaux en présence d'un catalyseur au palladium
- les triples inhibiteurs de la recapture des monoamines, comme antidépresseurs de nouvelle génération
- les alcools, par l′hydrolyse des éthers de silyle de type alkyle à pH neutre dans des solutions tamponnées mixtes organiques-aqueuses
- les oligoribonucléotides à liaisons phosphonates modifiées
- les alcools alkyliques aryliques, par alkylation de Nozaki-Hiyama catalysée par des ligands de bipyridyldiol chiral et trichlorure de chrome
- les esters conjugués d′acide diénoïque, par réactions de couplage de Suzuki
- l′inhibiteur de Hsp90 o-aminobenzamide macrocyclique présentant une activité antitumorale
- les inhibiteurs doubles de PI3K (phosphoinositide 3-kinase)/mTOR (mammalian target of rapamycin)
- les glucosides polyacétylènes (antidiabétiques)
Mention d'avertissement
Danger
Mentions de danger
Classification des risques
Acute Tox. 4 Oral - Aquatic Chronic 3 - Carc. 2 - Eye Irrit. 2 - Flam. Liq. 2 - Repr. 2 - Skin Irrit. 2 - STOT SE 3
Organes cibles
Central nervous system, Respiratory system
Risques supp
Code de la classe de stockage
3 - Flammable liquids
Classe de danger pour l'eau (WGK)
WGK 3
Point d'éclair (°F)
1.4 °F - closed cup
Point d'éclair (°C)
-17 °C - closed cup
Certificats d'analyse (COA)
Recherchez un Certificats d'analyse (COA) en saisissant le numéro de lot du produit. Les numéros de lot figurent sur l'étiquette du produit après les mots "Lot" ou "Batch".
Déjà en possession de ce produit ?
Retrouvez la documentation relative aux produits que vous avez récemment achetés dans la Bibliothèque de documents.
Les clients ont également consulté
Articles
Click chemistry, and the copper(I)-catalyzed azide-alkyne cycloaddition (CuAAC) in particular, is a powerful new synthetic tool in polymer chemistry and material science.
Click chemistry, and the copper(I)-catalyzed azide-alkyne cycloaddition (CuAAC) in particular, is a powerful new synthetic tool in polymer chemistry and material science.
Click chemistry, and the copper(I)-catalyzed azide-alkyne cycloaddition (CuAAC) in particular, is a powerful new synthetic tool in polymer chemistry and material science.
Click chemistry, and the copper(I)-catalyzed azide-alkyne cycloaddition (CuAAC) in particular, is a powerful new synthetic tool in polymer chemistry and material science.
Notre équipe de scientifiques dispose d'une expérience dans tous les secteurs de la recherche, notamment en sciences de la vie, science des matériaux, synthèse chimique, chromatographie, analyse et dans de nombreux autres domaines..
Contacter notre Service technique